| ** | Latin American Journal of Clinical Sciences and Medical Technology is an open access magazine. To read all published articles and materials you just need to register Registration is free of charge. Register now If you already have registered please Log In | ** |
aHospital Country 2000, Guadalajara, Jalisco, México; bDepartamento de Disciplinas Filosófico, Metodológicas e Instrumentales, Centro Universitario de Ciencias de la Salud, Instituto Nacional del Aprendizaje, Habilidades e Investigación de las Ciencias, S.C. (INAHIC), Zapopan, Jalisco, México, Universidad de Guadalajara, Guadalajara, Jalisco, México; cUniversidad del Futbol y Ciencias del Deporte, Pachuca, Hidalgo, México, Instituto Nacional del Aprendizaje, Habilidades e Investigación de las Ciencias, S.C. (INAHIC), Zapopan, Jalisco, México; dUniversidad de Guanajuato, Cámara de Diputados LXVI Legislatura, México; eInstituto Nacional del Aprendizaje, Habilidades e Investigación de las Ciencias, S.C. (INAHIC), Zapopan, Jalisco, México, Federación Mexicana de Patología Clínica, A.C. (FEMPAC), Academia Mexicana de Cirugía, A.C..
Autor para correspondencia: , . Números telefónicos: ; e-mail: juevesm@gmail.com
Lat Am J Clin Sci Med Technol. 2025 Oct;7:80-89.
Recibido: 01 de agosto, 2025
Aceptado: 10 de octubre, 2025
Publicado: 31 de octubre, 2025
Vistas: 1909
Descargas: 7
Introducción. Las infecciones asociadas a la atención de la salud (IAAS) representan uno de los principales problemas de salud pública a nivel mundial y también constituyen un riesgo creciente para la salud global. El objetivo de este trabajo fue identificar IAAS y frecuencia relativa (FR) de bacterias aisladas en un hospital de alta especialidad en el año 2024. Material y métodos. Estudio observacional, transversal y retrospectivo de resultados de cultivos de pacientes internados entre el 1 de enero y 31 de diciembre de 2024. Se registró el servicio hospitalario, tipos de muestra y bacterias aisladas. Se utilizó conteo simple y estadística descriptiva para presentar el número total de especies aisladas y su FR. Resultados. En 967 cultivos de diferentes tipos de muestra de 221 hombres y 213 mujeres (n=434), se identificaron 64 especies bacterianas, siete de la lista prioritaria de la Organización Mundial de la Salud (OMS) y dos relacionadas con brotes de infecciones severas. Las FR mayores corresponden a Escherichia coli (0.267), Pseudomonas aeruginosa (0.115), Staphylococcus epidermidis (0.097), Klebsiella pneumoniae (0.056) y Staphylococcus aureus (0.041). Setenta y cuatro casos de IAAS se asociaron con 23 de las 64 especies aisladas. Conclusiones. Se identificaron patógenos bacterianos de importancia en la salud pública, cuyas FR requieren de un análisis amplio para establecer estrategias de vigilancia y control de las IAAS que incluyan patrones y evolución de resistencia antimicrobiana en todos los niveles de atención de la salud.
Introduction. Healthcare-associated infections (HAIs) represent one of the primary global public health concerns and pose an increasing threat to global health. This study aimed to identify HAIs and the relative frequency (RF) of bacterial isolates in a tertiary care hospital during 2024. Materials and Methods. This was an observational, cross-sectional, descriptive, and retrospective study of culture results from hospitalized patients between January 1st and December 31st, 2024. Hospital services, sample types, and isolated bacteria were recorded. Simple counting and descriptive statistics were used to present the total number of isolated species and their RF. Results. A total of 967 cultures from various sample types were collected from 221 men and 213 women (n = 434), identifying 64 bacterial species, including seven from the World Health Organization's priority pathogen list and two associated with outbreaks of severe infections. The highest RFs corresponded to Escherichia coli (0.267), Pseudomonas aeruginosa (0.115), Staphylococcus epidermidis (0.097), Klebsiella pneumoniae (0.056), and Staphylococcus aureus (0.041). Seventy-four HAI cases were associated with 23 of the 64 isolated species. Conclusions. Bacterial pathogens of public health importance were identified, and their RFs highlight the need for comprehensive analysis to establish effective HAI surveillance and control strategies, including the monitoring of antimicrobial resistance patterns and trends at all levels of healthcare.
Las infecciones asociadas a la atención de la salud (IAAS), según la Organización Mundial de la Salud (OMS), son las infecciones que afectan a un paciente durante el proceso de atención hospitalaria o en un centro de salud, que no estaban presentes ni en período de incubación al momento del ingreso, y que incluso podrían manifestarse después del alta del paciente.1
Las IAAS representan uno de los principales problemas de salud pública a nivel mundial y también constituyen un riesgo creciente para la salud global. Sus tasas de prevalencia son de 5% en América del Norte y algunas partes de Europa y de hasta 40% en ciertas regiones de Asia, Latinoamérica y África.2
Entre los agentes causantes de IAAS destacan patógenos bacterianos prioritarios incluidos en la lista de la OMS, clasificados en tres grupos:
- Grupo 1, prioridad crítica. Enterobacterias resistentes a carbapenémicos, enterobacterias resistentes a cefalosporinas de tercera generación, Acinetobacter baumannii resistente a carbapenémicos y Mycobacterium tuberculosis resistente a rifampicina.
- Grupo 2, prioridad alta.Salmonella typhi resistente a fluoroquinolonas, Shigella spp. resistente a fluoroquinolonas, Enterococcus faecium resistente a vancomicina, Pseudomonas aeruginosa resistente a carbapenémicos, Salmonella no typhi resistente a fluoroquinolonas, Neisseria gonorrhoeae resistente a cefalosporinas y/o fluoroquinolonas de tercera generación y Staphylococcus aureus resistente a meticilina.
- Grupo 3, prioridad media. Estreptococos del grupo A resistentes a macrólidos, Streptococcus pneumoniae resistente a macrólidos, Haemophilus influenzae resistente a ampicilina y estreptococos del grupo B resistentes a penicilina.3
Las IAAS representan una de las principales causas de mortalidad y los costos de atención son elevados debido al incremento en la duración de la hospitalización de los pacientes afectados.4 En México, el promedio es de 9.7 días de hospitalización en estos pacientes, lo cual se traduce en un gasto significativo en el sector salud.5
Por lo tanto, los objetivos de este estudio son analizar la frecuencia de las IAAS en un hospital de alta especialidad, identificar las especies de microorganismos causantes que ayuden a caracterizar la resistencia bacteriana mediante el análisis de registros hospitalarios y bases de datos oficiales del año 2024, así como describir el sitio de infección, servicio hospitalario y la tendencia inicial de las frecuencias relativas (FR).
Se realizó un estudio observacional, transversal y retrospectivo con los resultados de cultivos microbiológicos solicitados a pacientes internados entre el 1 de enero y el 31 de diciembre de 2024 en el hospital participante. Se realizó una posterior comparación con años previos.
Se incluyeron hombres o mujeres de cualquier edad, referidos para uno o más cultivos microbiológicos por cualquier servicio hospitalario, con reporte positivo, identificación de microorganismos aislados e información sobre el tipo de muestras biológicas.
Se excluyeron los resultados de identificación de hongos, aquellos de pacientes ambulatorios, cultivos contaminados o no concluyentes, así como los reingresos de once pacientes en el período de estudio.
En una base de datos de Excel se registraron, sistemáticamente, los datos del servicio hospitalario, el tipo de muestra, sitio de obtención y microorganismos aislados, así como el número de cultivos solicitados por paciente. Se distinguió entre cultivos con crecimiento de un solo microorganismo y aquellos con dos o más (considerados polimicrobianos).
Para el cultivo inicial, se emplearon distintos medios según el tipo de muestra y la sospecha clínica. Para su identificación se siguieron los procedimientos estandarizados en el equipo MicroScan (Beckman Coulter®). La información se analizó por conteo simple y estadística descriptiva para presentar los datos de porcentaje y FR de las bacterias más prevalentes.
El proyecto fue aprobado por el Comité de Ética e Investigación, con dispensa de carta de consentimiento informado, y en todos los casos, los datos sensibles de los pacientes fueron disociados para garantizar la confidencialidad y anonimato de los participantes.
Durante el período de estudio (del 1 de enero al 31 de diciembre de 2024), se hospitalizó a un total de 434 pacientes que cumplió con los criterios de inclusión (221 hombres y 213 mujeres), con edades que abarcaron desde recién nacidos hasta 101 años. Los pacientes fueron atendidos en diversos servicios del hospital (Tabla 1). Se excluyeron 22 pacientes que continuaban hospitalizados al momento del corte de datos.
| Tabla 1. Servicio hospitalario y número de pacientes a los que se les practicó cultivo microbiológico entre el 1 de enero y el 31 de diciembre de 2024 | ||||
|---|---|---|---|---|
| Servicio hospitalario | Pacientes | Servicio hospitalario | Pacientes | |
| Medicina interna | 135 | Neumología | 8 | |
| Cirugía | 51 | Oncología | 8 | |
| Traumatología | 34 | Hematología | 6 | |
| Pediatría | 32 | Medicina general | 5 | |
| Nefrología | 28 | Neurología | 5 | |
| Neurocirugía | 23 | Geriatría | 4 | |
| Terapia intensiva | 16 | Infectología | 4 | |
| Urología | 16 | Otorrinolaringología | 3 | |
| Urgencias | 15 | Medicina crítica | 2 | |
| Gastroenterología | 13 | Radiología | 2 | |
| Cardiología | 12 | Otro | 2 | |
| Ginecología | 9 | Anestesiología | 1 | |
| TOTAL | 434 | |||
El promedio de días de hospitalización para los 412 pacientes restantes fue de 11 (rango: 1-141). A 272 pacientes se les solicitó un cultivo, mientras que a 162 (90 hombres y 72 mujeres) se les practicaron dos o más cultivos (rango: 2-32; total: 695 cultivos). En total, se analizaron los resultados de 967 cultivos de diferentes muestras biológicas con base en las manifestaciones clínicas de los pacientes, principalmente orina (40%), secreciones (21%) y sangre (12%).
Microorganismos aislados
Se identificaron 64 especies bacterianas; de las cuales 33 correspondieron a Gram-positivas y 31 a Gram-negativas. Entre ellas, siete están en la lista prioritaria de la OMS: Acinetobacter baumannii (prioridad crítica); Pseudomona aeruginosa, Staphylococcus aureus, Enterococcus faecium y género Salmonella (prioridad alta); Streptococcus pyogenes (Grupo A) y Streptococcus agalactiae (Grupo B, prioridad media).
Además, se aislaron tres especies de importancia clínica por su relación con brotes de infecciones hospitalarias severas y en pacientes inmunosuprimidos (Klebsiella pneumoniae, Klebsiella oxytoca y Stenotrophomona maltophilia).
FR de bacterias y cultivos polimicrobianos
La FR de las 20 especies bacterianas más prevalentes se presenta en la Tabla 2. Se identificaron 161 cultivos con dos o más bacterias (polimicrobianos) de 71 mujeres y 90 hombres (37% de los sujetos de estudio).
| Tabla 2. Especies bacterianas aisladas con mayor frecuencia relativa | |||
|---|---|---|---|
| Bacteria | FR | Bacteria | FR |
| Escherichia coli | 0.267 | Enterobacter cloacae | 0.015 |
| Pseudomonas aeruginosa** | 0.115 | Enterococcus faecium** | 0.012 |
| Staphylococcus epidermidis | 0.097 | Streptococcus mitis | 0.012 |
| Klebsiella pneumoniae* | 0.056 | Klebsiella oxytoca* | 0.012 |
| Staphylococcus aureus** | 0.041 | Citrobacter freundii | 0.012 |
| Enterococcus faecalis | 0.033 | Staphylococcus hominis | 0.011 |
| Stenotrophomonas maltophilia+ | 0.024 | Morganella morganii | 0.006 |
| Burkholderia cepacia complex | 0.023 | Serratia marcescens | 0.006 |
| Staphylococcus haemolyticus | 0.016 | Acinetobacter baumannii** | 0.005 |
| Proteus mirabilis | 0.015 | Streptococcus agalactiae** | 0.001 |
| * Bacterias descritas en brotes de infecciones severas. ** Bacterias en la lista prioritaria de la OMS. + Patógeno multirresistente que se está aislando con frecuencia creciente de pacientes predispuestos. | |||
Asimismo, en diferentes tipos de muestra de 22 pacientes se aislaron dos o más especies bacterianas, en las cuales se identificaron agentes prioritarios de relevancia clínica como E. faecium, P. aeruginosa, A. baumannii, S. aureus y K. pneumoniae.
IAAS y bacterias identificadas como causantes
Se detectaron IAAS en 74 pacientes (17%), que adquirieron la infección durante su estancia hospitalaria; y fueron más frecuentes en la Unidad de Cuidados Intensivos de Adultos (UCIA) (28, 32%). Las principales localizaciones de IAAS fueron el tracto urinario, el respiratorio inferior y el torrente sanguíneo (Gráficas 1 y 2).
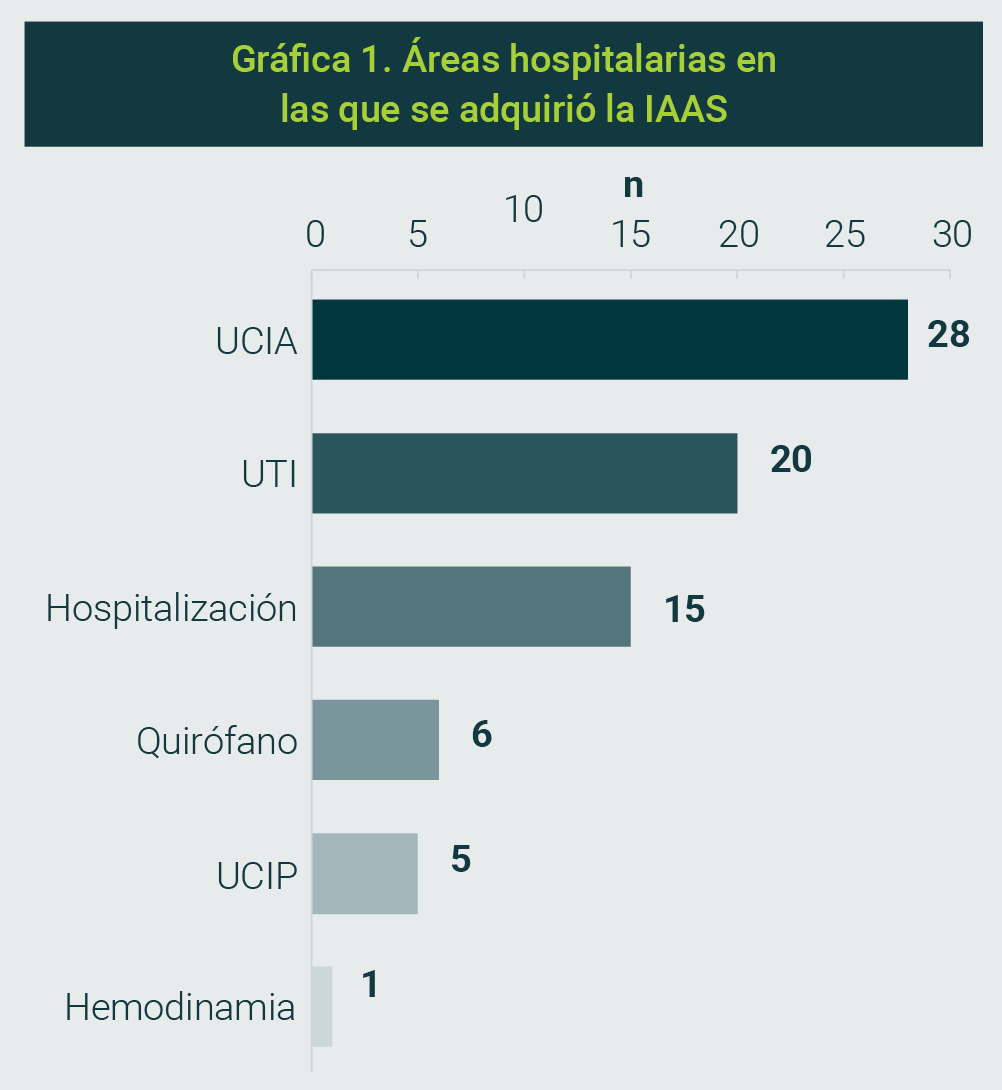
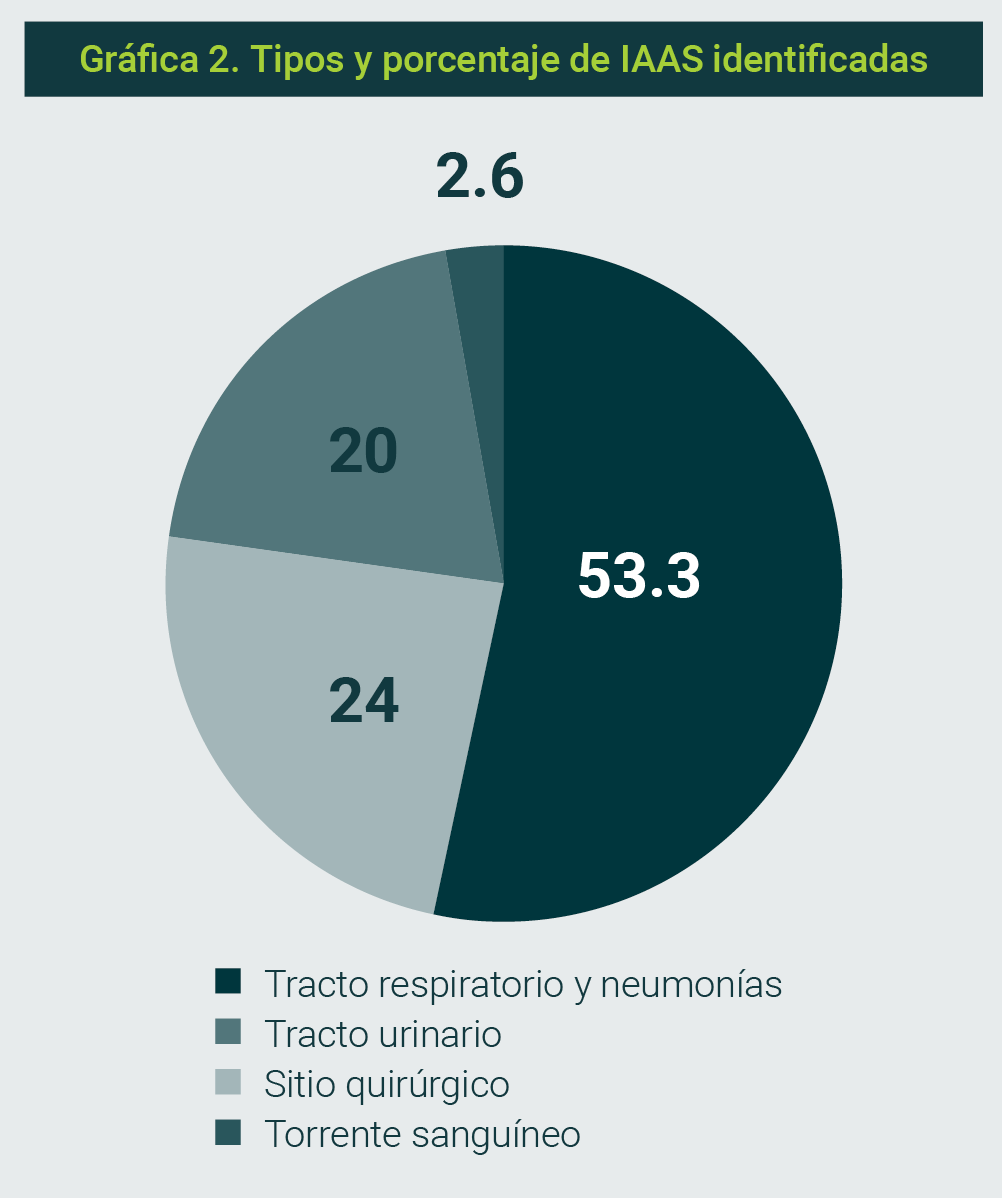
En 51 de los 74 casos de IAAS se identificó la presencia de bacterias prioritarias de la OMS. De los 74 pacientes con IAAS, 49 presentaron un solo agente etiológico y 25 infecciones polimicrobianas (Tabla 3). El promedio de días de hospitalización en pacientes con IAAS fue de 27 días, rango de 8 a 83 días (X̄=27, d=1), con una diferencia significativa respecto a los pacientes sin IAAS, quienes presentaron una estancia media de 11 días (p <0.01).
| Tabla 3. Relación de 23 bacterias identificadas como causantes de IAAS (n = 74) y su frecuencia relativa | |||||
|---|---|---|---|---|---|
| Bacteria aislada como causante de IAAS | Casos | FR | Bacteria aislada como causante de IAAS | Casos | FR |
| Pseudomonas aeruginosa** | 16 | 0.21 | Escherichia coli | 13 | 0.17 |
| Klebisella pneumoniae | 8 | 0.10 | Burkholderia cepacia complex | 6 | 0.08 |
| Stenotrophomonas maltophilia+ | 5 | 0.07 | Staphylococcus aureus** | 4 | 0.05 |
| Staphylococcus epidermidis | 3 | 0.04 | Acinetobacter baumannii complex / haemolyticus** | 2 | 0.03 |
| Klebsiella oxytoca* | 2 | 0.03 | Staphylococcus haemolyticus | 2 | 0.03 |
| Streptococcus agalactiae | 2 | 0.03 | Acinetobacter iwoffii | 1 | 0.01 |
| Bordetella bronchiseptica | 1 | 0.01 | Elizabethkingia meningoseptica | 1 | 0.01 |
| Enterebacter cloacae | 1 | 0.01 | Enterococcus faecalis | 1 | 0.01 |
| Enterococcus faecium** | 1 | 0.01 | Globicatalla sanguinis | 1 | 0.01 |
| Proteus mirabilis | 1 | 0.01 | Serratia marcescens | 1 | 0.01 |
| Staphylococcus sciuri | 1 | 0.01 | Staphylococcus xylosus | 1 | 0.01 |
| Streptococcus pneumoniae | 1 | 0.01 | |||
| Total de bacterias 23 | Total 75 | ||||
| n | % | n | % | ||
|---|---|---|---|---|---|
| Gram - positivo | 7 | 30.4 | Gram - negativo | 16 | 69.6 |
| *Bacterias descritas en brotes de infecciones severas. **Bacterias en la lista prioritaria de la OMS. +Patógeno multirresistente que se está aislando con frecuencia creciente de pacientes predispuestos. | |||||
Para el análisis comparativo de FR se realizaron pruebas de x2 para bacterias prioritarias o de importancia clínica y para bacterias no prioritarias con los datos del mismo hospital de cuatro años: 2019, 2020, 20216 y 2024. En ningún caso hubo diferencias significativas. En las Gráficas 3, 4 y 5 se muestra el análisis global de tendencias lineales de FR de 16 bacterias identificadas en los cuatro años, así como la tendencia de patógenos prioritarios y no prioritarios seleccionados.
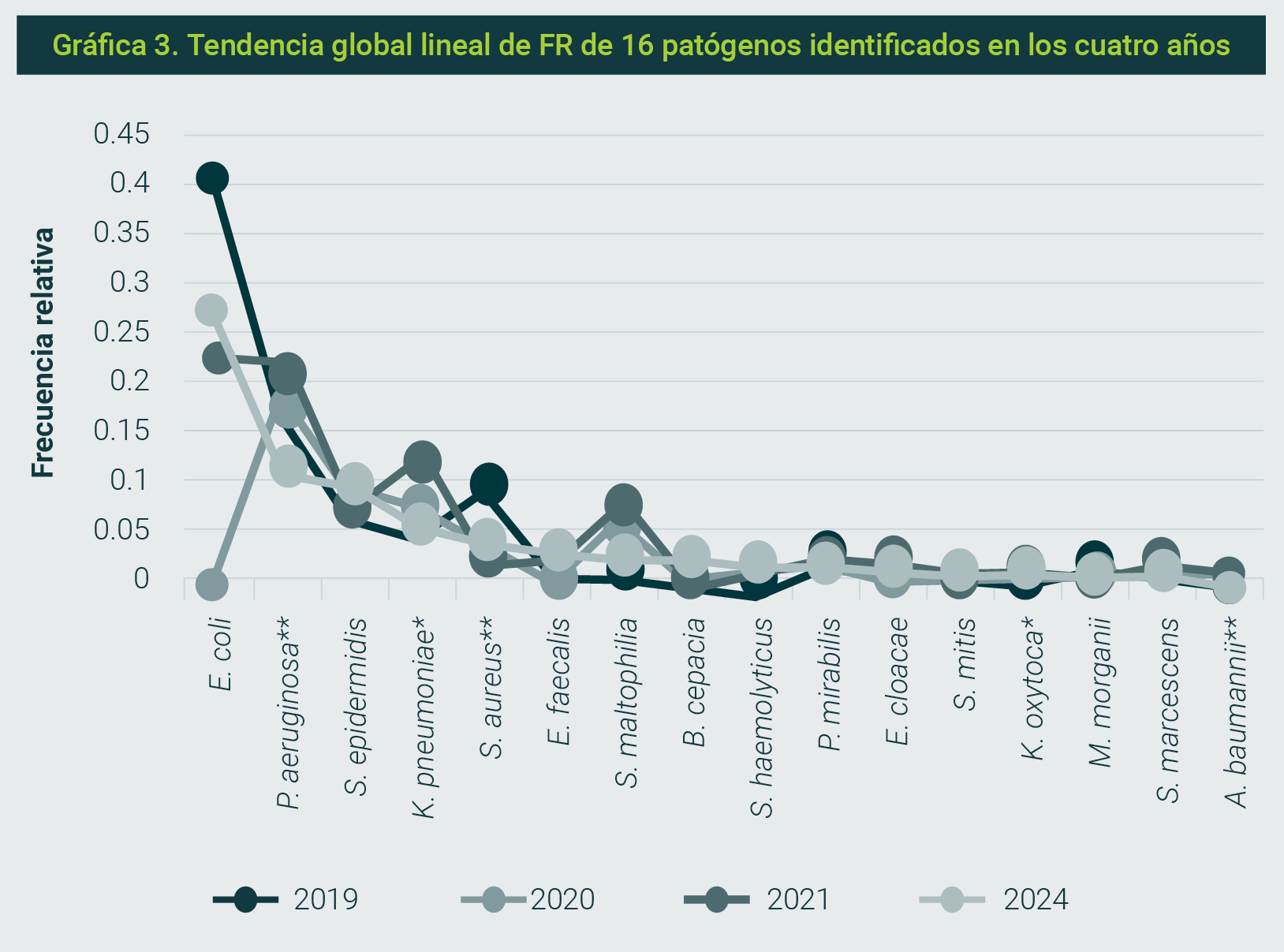
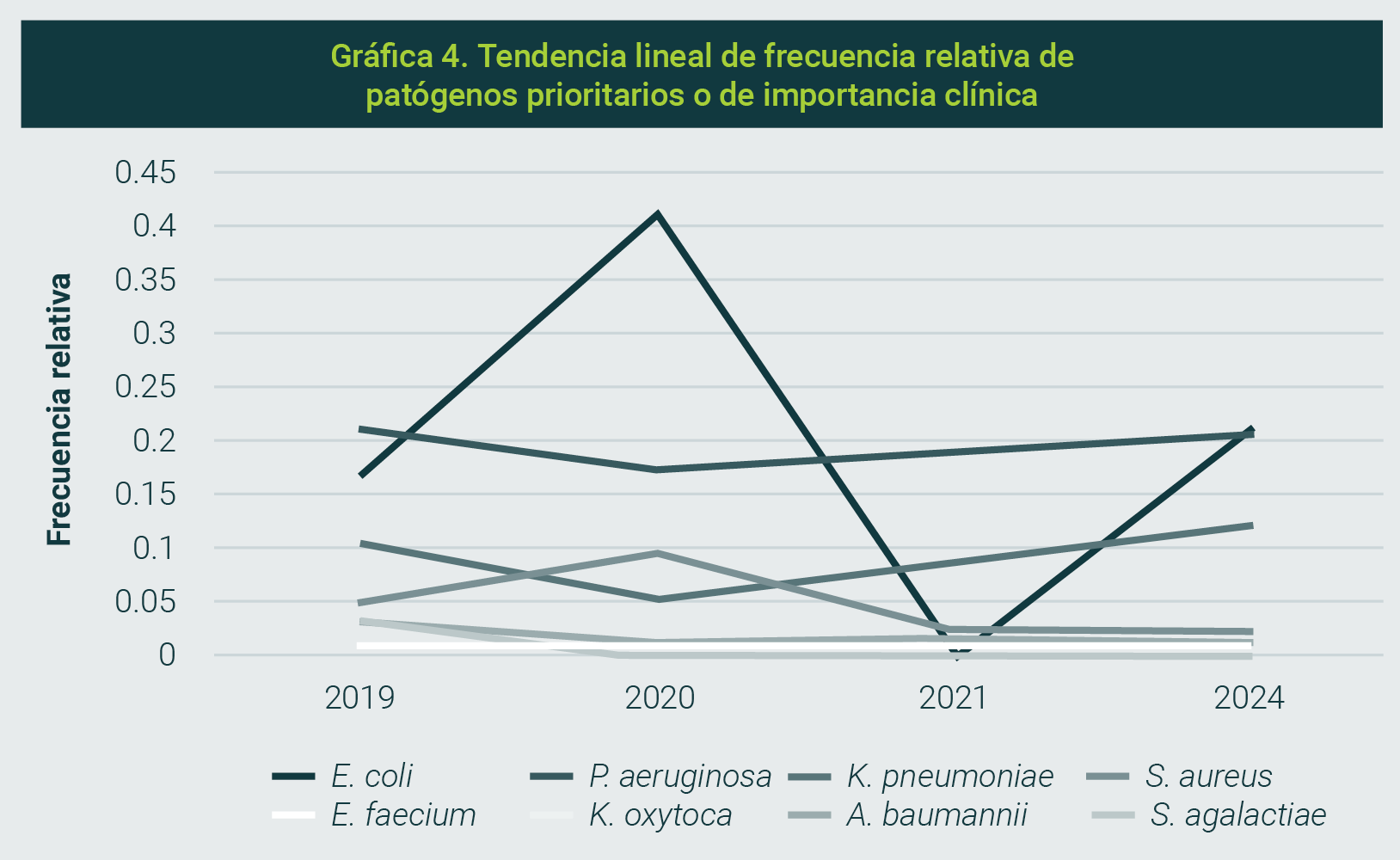
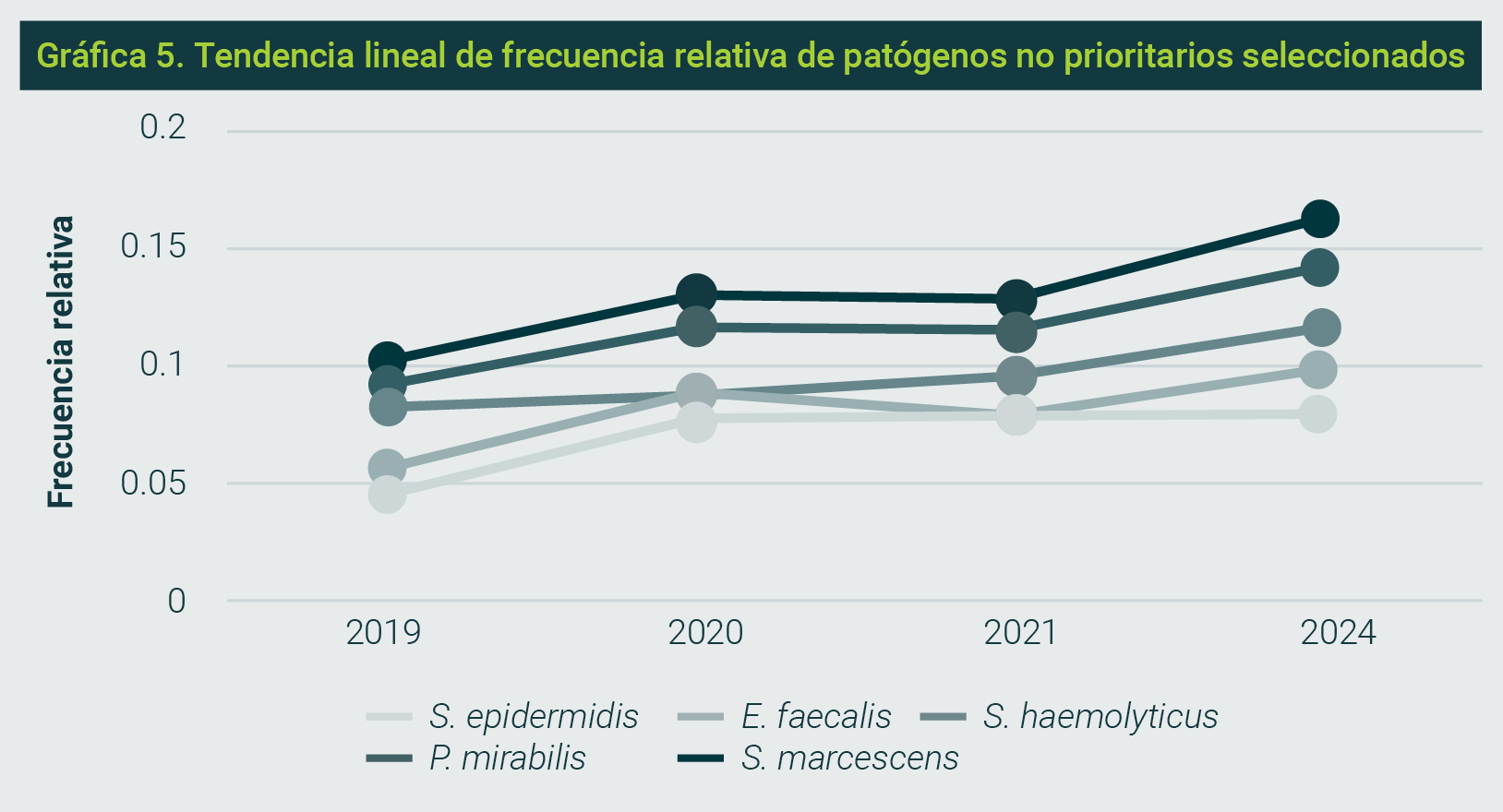
La FR de las bacterias identificadas en cultivos de pacientes hospitalizados, como se describe en este estudio, ofrece una visión más precisa del comportamiento tanto de bacterias prioritarias —o de importancia clínica por su papel en brotes hospitalarios— como de aquellas no prioritarias, además de su participación en IAAS.
Las 64 especies bacterianas identificadas pueden diferir de las reportadas en otros hospitales y regiones, lo cual subraya la importancia de monitorear las tendencias locales para ajustar tratamientos antibióticos, fortalecer las medidas de limpieza, optimizar la intervención de los comités de infecciones y mejorar la seguridad de los pacientes en cada institución.
Asimismo, el conocimiento de las FR resulta esencial para documentar la influencia y el comportamiento de las bacterias comunitarias, lo que requiere de instrumentos de recolección de información apropiados, así como del registro sistemático y verificado de los datos (tal cual fue realizado en el presente estudio).
La comparación de nuestros resultados con los años previos no mostró diferencias significativas en la FR, incluso en el período pospandémico de COVID-19, durante el cual se modificaron los esquemas empíricos de tratamiento antimicrobiano. Se observó una tendencia a la disminución de la FR en 2021, atribuible al confinamiento poblacional de ese año. Sin embargo, en 2023 y 2024 se detectó incremento —no significativo, pero constante— de bacterias no prioritarias, lo que podría reflejar mayor sensibilidad y especificidad de los métodos bacteriológicos empleados o bien mayor participación de bacterias comunitarias en la generación de infecciones.
Estudios internacionales7-10 y nacionales6,11-18 han reportado la FR de bacterias causantes de IAAS, que en algunos casos muestran tendencias similares y en otros divergentes, respecto a nuestros hallazgos, especialmente en lo relativo a bacterias prioritarias o de relevancia clínica.
En 2023, se notificaron 58,604 casos de IAAS en México, los cuales integraron datos sobre los principales patógenos causantes19, mismos que se integraron al análisis comparativo de las frecuencias de E. coli, P. aeruginosa, K. pneumoniae y S. aurus de los resultados de estudios seleccionados (Tabla 4).
| Tabla 4. Comparación de frecuencias con resultados de estudios seleccionados | ||||||
|---|---|---|---|---|---|---|
| Referencia | Estado/País | Año | E. coli | P. aeruginosa | K. pneumoniae | S. aureus |
20 | Tamaulipas | 2002 | 0.099 (↓) | 0.24 (↑) | 0.153 (↑) | 0.144 (↑) |
| x2 | 29.8817 | 16.7085 | 23.3263 | 32.0867 | ||
| p | <0.00001 | 0.00004 | <0.00001 | <0.00001 | ||
22 | CDMX | 2006 | 0.25 | SD | SD | SD |
| x2 | 0.156014 | - | - | - | ||
| p | 0.6929 | - | - | - | ||
19 | CDMX | 1999 | 0.218 | SD | SD | 0.092 (↑) |
| x2 | 1.45284 | - | - | 12.0277 | ||
| p | 0.2281 | - | - | 0.0005 | ||
| SD: Sin datos. (↑) y (↓): Frecuencias mayores o menores comparadas con las del presente estudio. | ||||||
Las diferencias observadas pueden explicarse por la diversidad de microorganismos responsables de infecciones nosocomiales, que varía entre instituciones y regiones, y está estrechamente relacionada con factores como la gravedad clínica, el estado inmunológico del paciente, el uso de antibióticos de amplio espectro y la intensidad de los procedimientos diagnósticos y terapéuticos.9
Las técnicas microbiológicas utilizadas, los métodos de toma de muestra, las políticas de limpieza, la disponibilidad de antibióticos, los protocolos institucionales y las comorbilidades de los pacientes (en particular los tratamientos previos) también contribuyen a estas variaciones.
Además de las bacterias prioritarias, y otras de importancia clínica, es fundamental considerar el comportamiento de patógenos emergentes como Stenotrophomonas maltophilia, caracterizado por su baja virulencia y elevada resistencia a antimicrobianos de amplio espectro. Este microorganismo, cada vez más frecuente, puede causar infecciones nosocomiales y comunitarias en pacientes susceptibles, principalmente adultos.20
Se han descrito factores de virulencia y mecanismos de resistencia de S. maltophilia, incluidos su capacidad para sobrevivir, colonizar, formar biopelículas y persistir en ambientes hospitalarios, lo que facilita la transferencia de genes de resistencia. El cambio climático podría modificar la colonización, supervivencia y formación de biopelículas de este patógeno en individuos y superficies hospitalarias.21
En nuestro estudio, S. maltophilia presentó una FR de 0.024, superior a la de 2019 (0.012), pero menor a la de 2021 (0.076), lo que puede reflejar el alcance de la pandemia por SARS-CoV-2, la prevalencia de comorbilidades como la diabetes mellitus y los cambios en la terapéutica de las infecciones.
En la última década, los avances en genómica bacteriana han permitido identificar mecanismos de resistencia, como las bombas de eflujo, que reducen la concentración intracelular de fármacos antimicrobianos.22
Recientemente, Kuznetsova y colaboradores describieron los determinantes génicos de cuatro familias de bombas de eflujo (RND, SMR, MFS y MATE) y se ha encontrado que bacterias multirresistentes como E. coli, K. pneumoniae y P. aeruginosa presentan mayor número de genes asociados a estos mecanismos, especialmente en pacientes renales trasplantados.23 Estos hallazgos subrayan la necesidad de incorporar la investigación molecular y la vigilancia genómica en las estrategias de control de la resistencia antimicrobiana.
El conocimiento de la FR de los patógenos según el tipo de muestra o sitio anatómico es esencial para orientar el tratamiento empírico, mientras se identifica el agente etiológico específico.
La localización de los principales focos de infección nosocomial es clave para implementar estrategias terapéuticas eficaces, ya que las IAAS siguen siendo una causa relevante de morbilidad y mortalidad hospitalaria9; sin embargo, la utilidad de la FR de los agentes aislados es poco reconocida como una herramienta epidemiológica clave para proteger la salud de los pacientes, optimizar el uso de antibióticos e implementar programas de optimización del uso de antimicrobianos (PROA).24
En muchos hospitales, públicos o privados, la vigilancia microbiológica se percibe como una actividad secundaria o exclusiva de los laboratorios de microbiología. Ello se suma a la poca comunicación entre los equipos clínicos, de laboratorio y de control de infecciones.25 Se priorizan actividades asistenciales urgentes para la toma de decisiones individuales de tratamiento, sin un análisis agregado que permita una evaluación objetiva de las tendencias en la distribución microbiana y su resistencia, lo que ayudaría a distinguir si los cambios observados se deben a modificaciones en las prácticas clínicas, a la introducción de nuevas cepas resistentes o a fallas en las medidas de prevención y control.
Para un control efectivo de estas infecciones es indispensable fomentar el trabajo multidisciplinario, expandir la capacidad y protocolos de los laboratorios de microbiología clínica y de investigación e integrar multidisciplinariamente a farmacéuticos, epidemiólogos, químicos, laboratoristas e infectólogos.
La utilización de sistemas avanzados de recopilación y análisis de datos [big data, Explainable Artificial Intelligence (XAI), Machine learning] y el establecimiento de programas integrales de control de infecciones y administración adecuada de antimicrobianos —incluido su uso profiláctico cuando esté indicado— son componentes fundamentales. Además, se requieren sistemas de vigilancia robustos, con evaluaciones periódicas que garanticen la efectividad y sostenibilidad de las intervenciones implementadas.6,26
La prevención de infecciones es una tarea colectiva y multidisciplinaria, liderada por epidemiólogos y microbiólogos hospitalarios, en colaboración con el personal de enfermería, equipos de prevención y especialistas involucrados.27
La participación de los especialistas en enfermedades infecciosas es crucial para vigilar el cumplimiento de las directrices sobre el uso óptimo de antibióticos —en cuanto a indicación, duración y dosis— y coordinar los esfuerzos del equipo multidisciplinario de gestión de antimicrobianos y las autoridades de salud pública, con el objetivo de combatir la resistencia antimicrobiana (RAM). La colaboración activa de estos especialistas se asocia con mejor adherencia a prácticas clínicas basadas en la evidencia y menor mortalidad.28
Finalmente, ante el limitado desarrollo de nuevos antibióticos y el aumento de la resistencia en los patógenos asociados a la atención médica, resulta imprescindible analizar y comprender los factores que influyen en la variación de su frecuencia, así como los mecanismos moleculares de resistencia, con el fin de adaptar las estrategias de control de infecciones y fortalecer con equipos interdisciplinarios los programas de optimización del diagnóstico microbiológico.29
Conocer la FR de las bacterias es fundamental para orientar la investigación y el desarrollo (I+D), que de acuerdo con la Organización para la Cooperación y Desarrollo Económico (OCDE)30 son actividades sistemáticas de indagación y/o experimentación dirigidas a crear nuevos conocimientos y aplicarlos en la creación y mejora de productos, procesos o servicios.
De igual manera, conocer la FR de las bacterias es esencial para optimizar las inversiones y las políticas globales dirigidas a enfrentar las amenazas más urgentes de la RAM, que actualmente limita el uso de antibióticos de última generación y de amplio espectro a los casos estrictamente necesarios. Asimismo, la FR es necesaria para nutrir de información los PROA de cada centro hospitalario.
La información disponible en México aún es insuficiente, por lo que resulta indispensable conocer la FR específica de cada región y sitio de atención para mejorar la vigilancia y ofrecer atención adecuada a los pacientes con IAAS, quienes representan un reto epidemiológico comparable al de países desarrollados y a la vez similar al de naciones de ingresos medios y bajos, donde la calidad de los servicios de salud es un indicador clave.
Para reducir la incidencia de IAAS es imprescindible analizar de manera integral los diversos factores involucrados, entre ellos la edad del paciente, las comorbilidades, la realización de procedimientos invasivos y los tratamientos médicos administrados durante la hospitalización.
Las prácticas y políticas institucionales desempeñan un papel relevante, así como las condiciones del entorno hospitalario y el acceso a tecnologías innovadoras para la identificación de microorganismos, lo que permite generar actuaciones coordinadas y orientadas a optimizar el uso de las técnicas diagnósticas de manera interdisciplinaria para la toma de decisiones terapéuticas, clínicas y preventivas.
El control efectivo de las IAAS exige a todos los centros hospitalarios una vigilancia rigurosa y precisa, además de considerar la incorporación de patógenos emergentes, como los hongos, que pueden modificar significativamente el perfil etiológico de las IAAS.
Se deberán realizar futuros estudios en cada hospital público o privado, de segundo y tercer nivel, y en grupos etarios específicos para el fortalecimiento de los laboratorios de microbiología y su estandarización.
Igualmente, es menester robustecer los Comités para la Detección y Control de Infecciones Nosocomiales, los sistemas de vigilancia microbiológica y la actualización constante de los protocolos institucionales porque ello no sólo permitirá adaptar las estrategias de prevención y control a los cambios epidemiológicos, sino que contribuirá a mejorar la calidad y la seguridad de la atención en salud.
Ninguno declarado.
Los autores declaran no tener ningún conflicto de intereses.
Ninguno declarado.
| 1. | U.S. Department of Health and Human Services (HHS). Health care associated infections.[Retrieved on October 13th, 2025] Available from URL: https://www.hhs.gov/oidp/topics/health-care-associated-infections/index.html |
| 2. | Raoofi S, Pashazadeh Kan F, Rafiei S, Hosseinipalangi Z, Noorani Mejareh Z, Khani S, et al. Global prevalence of nosocomial infection: A systematic review and meta-analysis. PLoS One. 2023;18(1):e0274248. |
| 3. | World Health Organization. WHO bacterial priority pathogens list, 2024: Bacterial pathogens of public health importance to guide research, development and strategies to prevent and control antimicrobial resistance. [Retrieved on October 13th, 2025] Available from: https://www.who.int/publications/i/item/9789240093461 |
| 4. | Wilson T, Nolte D, Omar S. Bed occupancy and nosocomial infections in the intensive care unit: A retrospective observational study in a tertiary hospital. South Afr J Crit Care. 2024;40(2):e1906. |
| 5. | Álvarez-Hernández G, Amaro-Ortega C. Attributable costs and risk factors for nosocomi infection in a pediatric hospital of Sonora, Mexico: 2008. Bol Med Hosp Infant Mex. 2010;67:118-27. Available from URL: https://www.medigraphic.com/pdfs/bmhim/hi-2010/hii102e.pdf |
| 6. | Sánchez González JM, Rodríguez Arias EA, Rivera Cisneros AE, Portillo Gallo JH, Jiménez Umbarila RA, Ramírez Barba ÉJ, et al. Reporte de frecuencias relativas sobre infecciones bacterianas asociadas a IAAS, análisis 2019 a 2021 de un hospital de tercer nivel. Rev Mex Patol Clin Med Lab. 2022;69:11-17. Disponible en URL: https://www.medigraphic.com/pdfs/patol/pt-2022/pt221c.pdf |
| 7. | Weber DJ, Rutala WA, Samsa GP, Wilson MB, Hoffmann KK. Relative frequency of nosocomial pathogens at a university hospital during the decade 1980 to 1989. Am J Infect Control. 1992;20(4):192-7. |
| 8. | Tresoldi AT, Branchini ML, Moreira Filho DC, Padoveze MC, Dantas SP, Reginato L, et al. Relative frequency of nosocomial microorganisms at UNICAMP University Hospital from 1987 to 1994. Rev Inst Med Trop Sao Paulo. 1997;39(6):333-6. |
| 9. | Kang J, Sickbert-Bennett EE, Brown VM, Weber DJ, Rutala WA. Relative frequency of health care-associated pathogens by infection site at a university hospital from 1980 to 2008. Am J Infect Control. 2012;40(5):416-20. |
| 10. | Atici S, Kilic S, Karadeniz Cerit K, Kiyan G, Soysal A. Healthcare-associated infections in the first four years of a pediatric surgical intensive care unit. J Infect Dev Ctries. 2025;19(4):576-81. |
| 11. | Alonso-Aguilar NM, Juarez-Enriquez SR, Castro-Escarpulli G, Rivera G, Bocanegra-Garcia V, Guo X, et al. Aetiology and significance of hospital-acquired infections in Mexico. Clin Lab. 2017;63(2):207-218. |
| 12. | Cruz-Lopez F, Villarreal-Trevino L, Morfin-Otero R, Martinez-Melendez A, Camacho-Ortiz A, Rodriguez-Noriega E, et al. Dynamics of colonization in patients with health care-associated infections at step-down care units from a tertiary care hospital in Mexico. Am J Infect Control. 2020;48(11):1329-35. |
| 13. | Vilar-Compte D, Sandoval S, Gordillo P, de la Rosa M, Sánchez-Mejorada G, Volkow P. Vigilancia de las infecciones de herida quirúrgica. Experiencia de 18 meses en el Instituto Nacional de Cancerología. Salud Publica Mex. 1999;41(Suppl 1):S44-50. |
| 14. | Camacho-Ramírez RI, Ávila-Reyes R, Sánchez-Zapata MH, Montoya-Razzo NA, Yunes-Zárraga JL, Velázquez-Quintana NI. Epidemiology of nosocomial infections in a high specialty pediatric hospital. Enf Infec Microbiol. 2002;22(4):200-5. Disponible en URL: https://www.medigraphic.com/pdfs/micro/ei-2002/ei024e.pdf |
| 15. | Valenzuela-Flores AA, Rangel-Frausto MS, Gutiérrez-García JN, Valenzuela-Flores AG, Tabal-Galan N. [Nosocomial infection surveillance: experience at a cardiology hospital in Mexico]. Cir Cir. 2004;72(1):41-6. |
| 16. | Morayta Ramírez A, Granados Galván EM, Pérez Peláez GC, Domínguez Viveros W. Incidencia de infecciones nosocomiales en la Coordinación de Pediatría del CMN “20 de noviembre”. Revista de enfermedades infecciosas en pediatría. 2006;19:69-70. Disponible en URL: https://www.medigraphic.com/pdfs/revenfinfped/eip-2006/eip061b.pdf |
| 17. | López-Herrera JR, Méndez-Cano AF, Bobadilla-Espinosa RI, Zacate-Palacios J. Infecciones nosocomiales, mortalidad atribuible y sobre estancia hospitalaria. Rev Enferm Inst Mex Seguro Soc. 2012;20:85-90. Available from URL: https://www.medigraphic.com/pdfs/enfermeriaimss/eim-2012/eim122e.pdf |
| 18. | Arias-Flores R, Rosado-Quiab U, Vargas-Valerio A, Grajales-Muñiz C. Los microorganismos causantes de infecciones nosocomiales en el Instituto Mexicano del Seguro Social. Rev Med Inst Mex Seguro Soc. 2016;54:20-4. Disponible en URL: https://www.medigraphic.com/pdfs/imss/im-2016/im161d.pdf |
| 19. | Gobierno de México. Secretaría de Salud. Acciones y programas. Boletín Epidemiológico RHOVE 2023. [Consultado el 13 de octubre, 2025]. Disponible en URL: https://www.gob.mx/salud/acciones-y-programas/boletin-epidemiologico-rhove-2023-341707 |
| 20. | del Toro MD, Rodriguez-Baño J, Martinez-Martinez L, Pascual A, Perez-Canoa R, Perea EJ, et al. [Epidemiology, clinical features and prognosis of infections due to Stenotrophomonas maltophilia]. Enferm Infecc Microbiol Clin. 2006;24(1):4-9. |
| 21. | Brooke JS. Advances in the microbiology of Stenotrophomonas maltophilia. Clin Microbiol Rev. 2021;34(3):e0003019. |
| 22. | Alghamdi A, Hafiz T, Almaghrabi R, Al-Qahtani A, Hammad E, Obeid D, et al. Multidrug resistance efflux pump expression in uropathogenic Gram-negative bacteria in organ transplant recipients. J Infect Dev Ctries. 2025;19(5):641-8. |
| 23. | Kuznetsova MV, Nesterova LY, Mihailovskaya VS, Selivanova PA, Kochergina DA, Karipova MO, et al. Nosocomial Escherichia coli, Klebsiella pneumoniae, Pseudomonas aeruginosa, and Staphylococcus aureus: Sensitivity to chlorhexidine-based biocides and prevalence of efflux pump genes. Int J Mol Sci. 2025;26(1):355. |
| 24. | Moreno MV, Amador R, Vargas J, Bugarin G, Flores. Análisis cuantitativo del estado de implementación de programas de uso racional de antimicrobianos en instituciones públicas de Chile. Rev chil infectol. 2025;42(1):7-20. Disponible en URL: https://www.scielo.cl/pdf/rci/v42n1/0716-1018-rci-42-01-0007.pdf |
| 25. | Skodvin B, Aase K, Brekken AL, Charani E, Lindemann PC, Smith I. Addressing the key communication barriers between microbiology laboratories and clinical units: A qualitative study. J Antimicrob Chemother. 2017;72(9):2666-2672. |
| 26. | Al Rawas NSH, Al Aqil SM, Alageel AM, Alshugaih AHA, Amer AH, Almansour FSH, et al. Nosocomial infections: Prevention, control and surveillance. Advances in Clinical and Experimental Medicine. 2023;10:812-18. |
| 27. | Sosa-Hernández O. Papel actual del epidemiólogo hospitalario en México. Hosp Med Clin Manag. 2019;12:176-7. Disponible en URL: https://biblat.unam.mx/hevila/Hospitalmedicineandclinicalmanagement/2019/vol12/no4/7.pdf |
| 28. | Dalai AS, Monti EB, Mallesho R, Obeda M, Evans GA, Perez-Patrigeon S, et al. Increasing evidence-based care practices for patients with Staphylococcus aureus bacteraemia through required infectious diseases consultation in a tertiary care hospital: A quality improvement initiative. BMJ Open Qual. 2025;14(2):e003243. |
| 29. | Bou G, Cantón R, Martínez-Martínez L, Navarro D, Vila J. Fundamentals and implementation of Microbiological Diagnostic Stewardship Programs. Enferm Infecc Microbiol Clin (Engl Ed). 2021;39(5):248-251. |
| 30. | OECD, Fundación Española para la Ciencia y la Tecnología. Medición de las actividades científicas, tecnológicas y de innovación.Manual de Fascati 2015. Guía para la recopilación y presentación de información sobre la investigación y el desarrollo experimental. Editorial MIC, 2018. [Consultado el 16 de octubre de 2025] Disponible en URL:https://www.oecd.org/content/dam/oecd/es/publications/reports/2015/10/frascati-manual-2015_g1g57dcb/9789264310681-es.pdf |
All Rights Reserved® 2019
Latin American Journal of Clinical Sciences and Medical Technology,Publicación contínua • Editor responsable: Gilberto Castañeda Hernández. • Reserva de Derechos al Uso Exclusivo: 04-2019-062013242000-203; ISSN: 2683-2291; ambos otorgados por el Instituto Nacional del Derecho de Autor. • Responsable de la última actualización de este número, Web Master Hunahpú Velázquez Martínez,
Calle Profesor Miguel Serrano #8, Col. Del Valle, Alcaldía Benito Juárez, CP 03100, Ciudad de México, México. Número telefónico: 55 5405 1396 • Fecha de última modificación, 28 de agosto de 2024.
All Rights Reserved® 2019
Publicación contínua • Editor responsable: Gilberto Castañeda Hernández. • Reserva de Derechos al Uso Exclusivo: 04-2019-062013242000-203; ISSN: 2683-2291; ambos otorgados por el Instituto Nacional del Derecho de Autor. • Responsable de la última actualización de este número, Web Master Hunahpú Velázquez Martínez,
Calle Profesor Miguel Serrano #8, Col. Del Valle, Alcaldía Benito Juárez, CP 03100, Ciudad de México, México. Número telefónico: 55 5405 1396 • Fecha de última modificación, 28 de agosto de 2024.