| ** | Latin American Journal of Clinical Sciences and Medical Technology is an open access magazine. To read all published articles and materials you just need to register Registration is free of charge. Register now If you already have registered please Log In | ** |
aOncología Médica, Instituto Nacional de Cancerología, Ciudad de México, México; bOncología Médica, Centro Médico Nacional “Siglo XXI”, IMSS, Ciudad de México, México; cMedicina Nuclear, Instituto Nacional de Cancerología, Ciudad de México, México; dDepartamento de Tumores de Cabeza y Cuello, Instituto Nacional de Cancerología, Ciudad de México, México; eOncología Médica, Centro Médico Nacional “20 de Noviembre”, ISSSTE, Ciudad de México, México.
Autor para correspondencia: , . Números telefónicos: ; e-mail: eduardo.cardenasc@issste.gob.mx
Lat Am J Clin Sci Med Technol. 2023 Feb;5:28-35.
Recibido: 07 de diciembre, 2022
Aceptado: 23 de enero, 2023
Publicado: 01 de febrero, 2023
Vistas: 2013
Descargas: 27
El cáncer de la vía aerodigestiva superior incluye un grupo heterogéneo de neoplasias. Aproximadamente el 90% de ellas está constituido por células escamosas, y en su conjunto ocupan el sexto lugar en incidencia a nivel mundial. El tabaquismo, la ingesta de alcohol y la infección por virus de papiloma humano son los principales factores de riesgo asociados. Ante la sospecha diagnostica se requiere la confirmación histopatológica mediante biopsia. La tomografía es el principal método de imagen para la estadificación por TNM. El manejo requiere de un equipo multidisciplinario con estrecha comunicación entre los diferentes miembros. En general, podemos dividir el tratamiento de acuerdo con el estadio al diagnóstico en: enfermedad temprana, localmente avanzada y recurrente o metastásica. La cirugía es la mejor opción de tratamiento curativo en enfermedad temprana, además del uso de radioterapia adyuvante y quimiorradioterapia adyuvante en pacientes de alto riesgo. En los casos donde se busca la preservación de órgano, la quimiorradioterapia es una opción, así como en casos de tumor irresecable, lo que es frecuente en estadios localmente avanzados de la enfermedad. La quimioterapia de inducción es cuestionable; sin embargo, en pacientes con alto volumen tumoral o si los tiempos de inicio de tratamiento de radioterapia son prolongados (principalmente en laringe), puede ser una alternativa. La recurrencia de la enfermedad es frecuente. Aunque la presentación con enfermedad metastásica es rara, el objetivo de tratamiento será paliativo. La inmunoterapia ha conseguido prolongar la supervivencia global en la primera y segunda línea de tratamiento de la enfermedad recurrente o metastásica. La quimioterapia en combinación con cetuximab (ya sea en primera o segunda línea) sigue siendo de utilidad en estos pacientes. La decisión de tratamiento dependerá de la expresión de PDL1 y las características clínico-patológicas del caso.
Cancer of the upper aerodigestive tract includes a heterogeneous group of neoplasms. About 90% are squamous cells and rank sixth in incidence worldwide. Smoking, alcohol intake, and human papillomavirus infection are the main risk factors. Given the suspected diagnosis, histopathological confirmation by biopsy is required. Tomography is the primary imaging method for TNM staging. Management requires a multidisciplinary team with close communication between the different members. In general, we can divide the treatment according to the stage at diagnosis into: early, locally advanced, and recurrent or metastatic disease. Surgery is the best curative treatment option in early disease with the use of adjuvant radiotherapy and chemoradiotherapy in high-risk patients. When organ preservation is the objective and in unresectable tumors (common in locally advanced stages of the disease), chemoradiotherapy is an option. Induction chemotherapy is controversial; however, in patients with high tumor volume or if the initiation times of radiotherapy treatment are prolonged (mainly in the larynx), it could be an alternative. The recurrence of the disease is frequent. Even though the presentation with metastatic disease is rarer, the treatment objective will be palliative. Immunotherapy has improved overall survival in the first and second lines of treatment of recurrent or metastatic disease. Chemotherapy in combination with cetuximab (either first or second line) continues to be useful in these patients. The treatment decision will depend on the expression of PDL1 and the clinicopathological characteristics of the case.
Los carcinomas de células escamosas de las vías aerodigestivas superiores (VADS) son un grupo heterogéneo de neoplasias, también conocido como cáncer de cabeza y cuello; sin embargo, evitamos este término en favor de un concepto más preciso. Este grupo incluye a los carcinomas de las fosas nasales, senos paranasales, nasofaringe, cavidad bucal, bucofarínge, laringe e hipofaringe. La proporción varía de acuerdo con el sitio específico, pero hasta 92% de ellos es carcinoma de células escamosas o epidermoides. El 10% restante pertenece a adenocarcinomas y otras estirpes histológicas, como sarcomas, melanomas y linfomas.1
Esta oncoguía incluye sugerencias y recomendaciones para el manejo de pacientes en condiciones ideales con diagnóstico de cáncer de la vía aerodigestiva superior. Su objetivo es proporcionar una guía para el tratamiento del cáncer de las VADS mediante recomendaciones que no sustituyen el juicio clínico.
Incidencia
En el mundo, los carcinomas de las VADS representan la séptima neoplasia con mayor incidencia; alrededor de 705,781 casos fueron diagnosticados en 2018 y hubo 358,144 muertes asociadas. Se espera que la incidencia global incremente 17% entre 2012 y 2022.2 En México, estas neoplasias representan la décima segunda neoplasia de mayor incidencia y la décima causa de muerte por cáncer.3 En 2020 se diagnosticaron 3,782 nuevos casos, de acuerdo con GLOBOCAN.2
En Estados Unidos, alrededor del 40% de los pacientes será diagnosticado en etapas localmente avanzadas; las etapas localizadas se presentarán en aproximadamente 50% de los pacientes y las etapas metastásicas en el 10% de éstos.4,5 Según datos internos del Instituto Nacional de Cancerología (INCan), hasta el 82% de los pacientes es diagnosticado en etapas localmente avanzadas (III y IV). Ello es relevante porque hasta dos terceras partes de los últimos y 20% de los primeros recaerán antes de 5 años.6
En pacientes con enfermedad localizada, la cirugía y la radioterapia son los tratamientos primarios. Sin embargo, en la enfermedad localmente avanzada, el tratamiento multimodal y multidisciplinario con quimioterapia, terapias blanco e inmunoterapia son cruciales ya que se asocian con mejor supervivencia global (SG), y mejor calidad de vida, en especial cuando se asocian con radioterapia.7,8 Los pacientes con enfermedad metastásica a la presentación o al momento de la recaída rara vez son candidatos a terapias locales (a diferencia de los portadores de enfermedad oligometastásica). En la mayoría de los restantes se requiere la combinación de la terapia blanco con cetuximab o inmunoterapia, cada una con sus indicaciones específicas; ambas han demostrado prolongar la supervivencia y mejorar la calidad de vida de los pacientes respecto la quimioterapia sola.9-12
Al ser una enfermedad heterogénea (y para fines de tratamiento y pronóstico), conviene clasificarla como enfermedad relacionada con el virus del papiloma humano (VPH) y no relacionada con la infección. No obstante, hay que agregar que otra neoplasia (por fortuna rara en nuestro medio), el carcinoma de nasofaringe,también tiene un comportamiento biológico, respuesta al tratamiento y pronóstico distinto a las restantes neoplasias; por tanto, se trata de forma separada.
Factores de riesgo
Se han identificado distintos factores de riesgo asociados con el carcinoma escamoso de las VADS, entre los que se encuentran la edad (la mediana de presentación de estos tumores es de 60 años) y el género masculino.1 Adicionalmente, dos factores fuertemente asociados son el tabaquismo y el consumo de alcohol.
Al menos 75% de los carcinomas escamosos de las VADS son atribuibles a los efectos carcinógenos del tabaco y el alcohol.13 Otro factor identificado recientemente es el VPH. Alrededor del 25 a 35% de los casos de carcinoma escamosos de las VADS están asociados con una infección viral. Esto es de mayor importancia en los pacientes con carcinomas de la bucofarínge, en quienes hasta el 70% de los casos está asociado con infección por VPH 16 y 18.14 En años recientes se ha documentado que estos pacientes suelen tener mejor pronóstico respecto los pacientes debido a los efectos del tabaco y el alcohol.15
El diagnóstico presuntivo de un carcinoma escamoso de las VADS surge de la sospecha clínica. El estándar en el diagnóstico es el estudio histopatológico de una biopsia incisional representativa.16 Una correcta evaluación del paciente evita complicaciones médicas o quirúrgicas; muchos de estos pacientes son neumópatas, hepatópatas o tienen desnutrición severa. Además, es muy importante la evaluación precisa de la extensión de la enfermedad, ya que una resección incompleta (márgenes histopatológicos positivos) se asocia con riesgo elevado de recaída, que no es eliminado por la administración del tratamiento adyuvante.
Ante la sospecha se practica una anamnesis completa y una minuciosa exploración de las VADS y cuello. Si existe una lesión compatible con un primario accesible, se toma una biopsia incisional, pero también se incluye la biopsia por aspiración con aguja fina (BAAF) de las adenopatías de dudosa naturaleza; si el resultado cambia el plan terapéutico. Si la lesión no es accesible, la biopsia se pospone hasta después de practicar los estudios de imagen.16
Las adenopatías fijas a planos tisulares profundos suelen ser irresecables. Las biopsias incisionales de ganglios cervicales están proscritas porque esto contamina los tejidos y entorpece el control de la enfermedad. A las biopsias de CE-BF (carcinoma bucofaringeo) se les practica el análisis de p16 por inmunohistoquímica, que indica causalidad por VPH. La evaluación se complementa con los estudios necesarios para evaluar la salud general, cardiovascular, comorbilidades, función hepática, respiratoria y el estado nutricional.17
Una radiografía de tórax tiene sensibilidad limitada para M+, pero alto valor predictivo positivo, además complementa la evaluación cardiovascular.18 La tomografía computada (TC) contrastada de macizo facial, cuello y tórax es el estudio inicial de elección para las neoplasias de las VADS (pero es prescindible en T1 glóticos y lesiones superficiales de la cavidad bucal).
La TC es útil para evaluar la invasión ósea y de cartílagos laríngeos, pero la imagen por resonancia magnética (IRM) es superior para evaluar carcinomas invasores profundos de lengua, piso de boca, encía (para examinar el canal medular) y tumores sinunasales debido al mejor contraste entre la neoplasia y los tejidos blandos circundantes, menos artefactos por materiales dentales, porque detecta diseminación perineural, evalúa mejor la base del cráneo y distingue secreciones en los senos paranasales de neoplasia en la misma región.18
Ambos estudios de imagen evalúan los ganglios regionales, pero son inferiores a la ultrasonografía (USG) y BAAF practicada por expertos, ya que es más sensible para detectar ganglios metastásicos. La TC e IRM son útiles para examinar la extensión extranodal macroscópica que se asocia con pronóstico pobre debido a dificultades para obtener el control local mediante cirugía.18
Los estudios endoscópicos de las VADS se usan en forma selectiva para complementar la evaluación previa y establecer el diagnóstico tisular mediante la obtención de biopsias, pero son más útiles para descartar segundos tumores primarios (STP) sincrónicos (15%). La broncoscopía se indica si hay fuerte sospecha de enfermedad broncopulmonar, pero se omite si la TC torácica es normal y el paciente está asintomático del área broncopulmonar. La laringoscopia de suspensión puede obtener tejido para diagnóstico en bucofaríngeo, laríngeo e hipofaringe, pero también posibilita la resección endoscópica con fines curativos, o simplemente para aliviar la obstrucción respiratoria, lo cual permite un mejor tratamiento definitivo.19
El PET/CT con 18-FDG es sensible para valorar el tumor primario y el estado ganglionar, pero su mayor utilidad radica en descartar metástasis y segundos primarios, comunes en carcinomas muy avanzados y recurrentes. Es el estudio inicial de elección cuando se planea tratamiento definitivo con quimioterapia (QT) y radioterapia (RT) en bucofaringe y otros sitios porque apoya el proceso de planificación de la RT, delimita mejor las áreas de mayor riesgo y evalúa mejor la respuesta al tratamiento.1
El tratamiento dependerá del estadio con base en el TNM, que podemos dividirlo en estadios tempranos (I y II), avanzados (III y IVA) y enfermedad recurrente o metastásica. El tratamiento debe individualizarse también respecto a las expectativas del paciente, su estado funcional y las características clinicopatológicas.
Todos los pacientes deben ser evaluados por el equipo multidisciplinario con experiencia en todas las opciones disponibles de tratamiento.20 Dicho equipo debe estar conformado por cirujanos oncólogos, radiólogos diagnósticos, radiólogos intervencionistas, cirujanos maxilofaciales, otorrinolaringólogos, endoscopistas, oncólogos médicos, radioncólogos, nutriólogos, neurocirujanos, patólogos y medicina física y rehabilitación.20
Antes de iniciar tratamiento debe asegurarse la vía aérea y vía de alimentación. La caquexia asociada a cáncer en pacientes con carcinoma escamoso de las VADS es muy frecuente y se asocia con mal pronóstico, por lo cual la valoración nutricional es fundamental; en pacientes con riesgo alto deben valorarse intervenciones como la gastrostomía. 21
Enfermedad temprana
La Figura 1 muestra el algoritmo de tratamiento de los pacientes con enfermedad temprana. El objetivo de tratamiento debe ser curativo y tratar de conservar la función. En este sentido, la cirugía es la mejor opción, salvo en algunos casos como es el cáncer de laringe donde la preservación de órgano puede ser prioritario con resultados similares en SG con el uso de RT.22
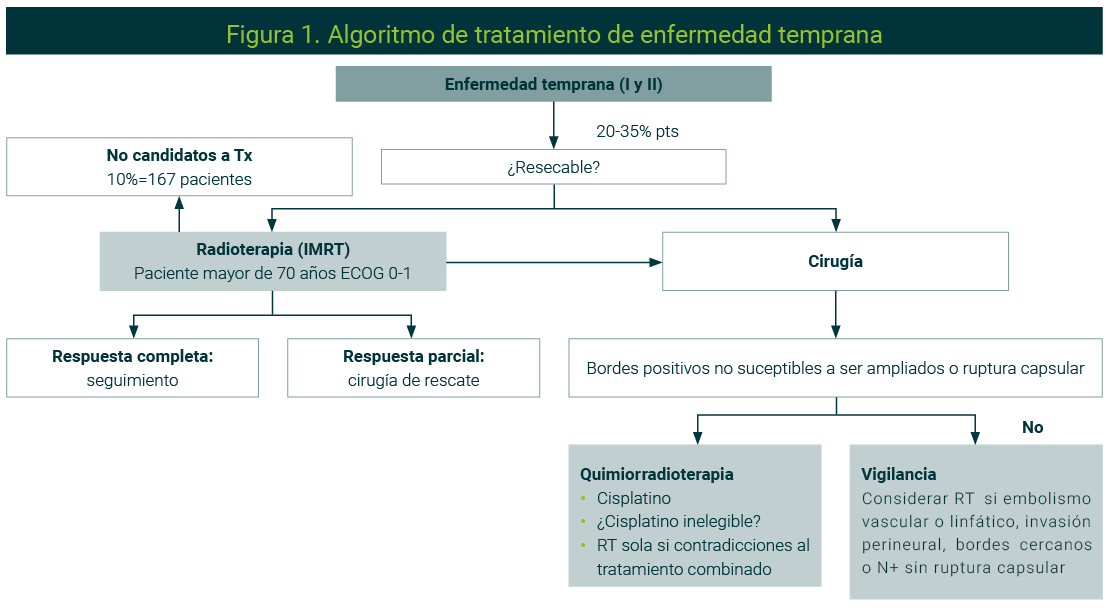
La figura es propiedad de los autores.
Es importante evaluar el uso de QT y RT adyuvante después de tratamiento con cirugía en pacientes de riesgo alto. El mayor beneficio se observó en pacientes con bordes positivos y/o ruptura capsular ganglionar, pero cada caso de ser individualizado.23
Enfermedad localmente avanzada
En la enfermedad avanzada, la cirugía sigue siendo el principal tratamiento con objetivo curativo, pero el volumen tumoral y la extensión de la enfermedad pueden hacer irresecable al tumor. Después de la cirugía siempre se debe considerar el uso de quimiorradioterapia adyuvante en pacientes de riesgo alto.23
En caso de considerarse enfermedad irresecable, la opción de tratamiento es la quimiorradioterapia concomitante con cisplatino trisemanal.24 En los pacientes no elegibles para platino deberá considerarse el uso de cetuximab concomitante con radioterapia.9
En enfermedad voluminosa o en casos de tiempos prolongados para inicio de RT, la QT de inducción puede ser útil. Cuando se considere el uso de inducción, la recomendación es el triplete con esquema TPF (docetaxel, sal platinada y 5-fluorouracilo). Después de la inducción, en caso de respuesta al tratamiento debe seguir quimiorradioterapia con cisplatino, en caso de que la dosis acumulada y eventos adversos lo toleren o con carboplatino o cetuximab en caso necesario. La mayor evidencia del uso de QT de inducción es en cáncer de laringe.25
El riesgo de recurrencia en estos pacientes es alto. Al término del tratamiento con quimiorradioterapia concomitante deberá evaluarse la respuesta con PET-CT después de 12 semanaspara evitar falsos positivos por los efectos de la radioterapia.26 Si hay persistencia de la enfermedad, se debe valorar llevar a cabo cirugía de rescate o manejar como enfermedad recurrente/metastásica. Idealmente, la enfermedad persistente o recurrente debe ser confirmada histopatológicamente.27
En la Figura 2 se muestra el algoritmo de tratamiento de la enfermedad localmente avanzada.
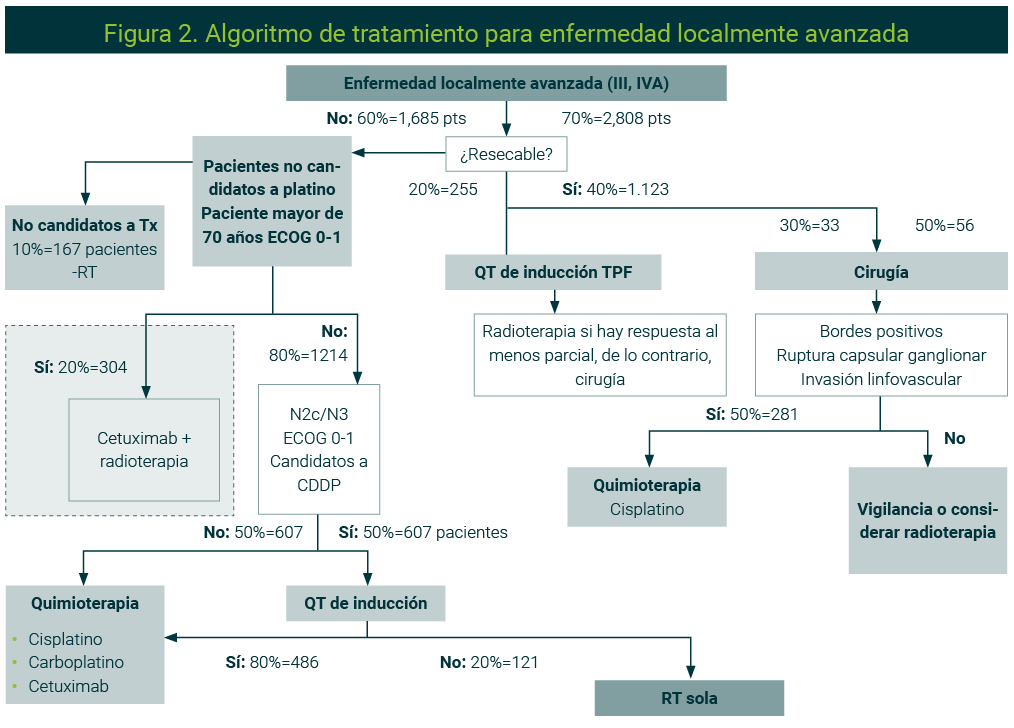
pts: pacientes; Tx: tratamiento; ECOG: estado funcional por Eastern Collaborative Oncology Group; QT: quimioterapia; TPF: docetaxel, sal platinada y 5-fluorouracilo; CDDP: cis-dicloro-diamino-platino o cisplatino; RT: radioterapia. Algoritmo realizado por los autores.
Enfermedad recurrente o metastásica
Cuando hay recurrencia de la enfermedad y el paciente no es candidato a cirugía de rescate ni RT o debuta con enfermedad metastásica, el objetivo del tratamiento es paliativo. La decisión de tratamiento dependerá de la expresión o no de PDL1, el estado funcional del paciente, el volumen tumoral y la velocidad de avance de la enfermedad.28 La Figura 3 resume el tratamiento de estos pacientes.
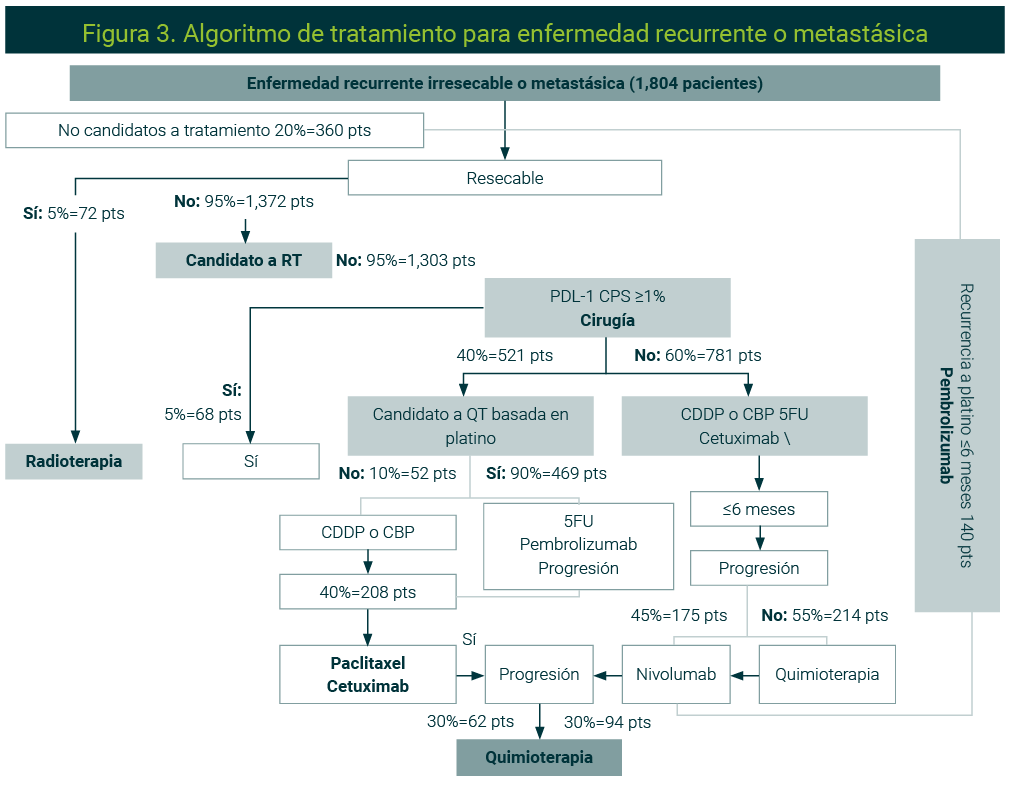
Algoritmo realizado por los autores.
La inmunoterapia sola o en combinación con QT ha mostrado beneficio en SG en pacientes con expresión de PDL1 mayor al 1%. El uso de pembrolizumab monodroga puede considerarse en altos expresores con PDL1 >20% o pacientes que no se espere toleren quimioterapia.12
En pacientes con expresión de PDL1 menor al 1%, la primera línea de tratamiento se implementará con esquemas como EXTREME o TPEX.29,30
En segunda línea de tratamiento ante progresión a QT combinada con cetuximab o pacientes previamente expuestos a QT con recurrencia o progresión dentro de los primeros seis meses de terminar tratamiento para enfermedad temprana o localmente avanzada, nivolumab ha mostrado beneficio en SG.11
Ante progresión a inmunoterapia, las opciones de tratamiento son QT combinada con cetuximab, dependiendo de los tratamientos previos que ha recibido el paciente.31
Es importante mantener la comunicación entre los miembros del equipo multidisciplinario en estos casos, ya que la cirugía y la RT pueden ser útiles en el control de síntomas de la enfermedad y el apoyo en el manejo paliativo del paciente.20 Finalmente, es necesario recordar que los pacientes con estado funcional ECOG mayor 2 difícilmente se benefician del tratamiento sistémico.
Carcinoma de nasofaringe
Dentro de los carcinomas de las VAD, el carcinoma de nasofaringe requiere una sección propia. Su incidencia es mayor en países del sureste asiático, como en China, donde es endémico.32 En México, representa menos del 1% de los cánceres de la cabeza y cuello.2
Es diferente a otros sitios de la cabeza y cuello porque tiene una biología molecular distinta. Asociado principalmente a infección por virus de Epstein Bar, es un tumor altamente radio y quimio sensible, por lo que son los pilares de tratamiento, además que por su localización anatómica con cirugía, es difícil garantizar márgenes libres.33
En etapas muy tempranas (estadio I por TNM) la radioterapia por si sola es el estándar de tratamiento. A partir del estadio II, la quimiorradioterapia logra el intento curativo. Cuando la enfermedad es localmente avanzada por la extensión del tumor primario o metástasis ganglionares, la QT de inducción ha mostrado beneficio. En este contexto, dobletes con gemcitabina y sal platinada se prefieren por su perfil de toxicidad y beneficio en SG.34,35
Ante la recurrencia o enfermedad metastásica, el tratamiento es similar al resto de los carcinomas de las VAD en otros sitios. La inmunoterapia ha mostrado extender la SG de los pacientes con carcinoma nasofaríngeo en ensayos clínicos fase III, en primera línea con expresión mayor a 1% de PDL1.
En el estudio de aprobación de pembrolizumab se excluyeron los carcinomas de nasofaringe; sin embargo, ante el hecho de que debido a su baja incidencia en población occidental no se espera tener evidencia de estudios fase III en estos pacientes con las inmunoterapias disponibles, es válido extrapolar los resultados de las inmunoterapias usadas en población asiática.36
En pacientes que no expresan PDL1, el estándar de tratamiento es QT basada en platino. No se ha mostrado beneficio con el uso de cetuximab, por lo que no se recomienda.
En segunda línea, los pacientes tratados previamente con inmunoterapia serán candidatos a tratamiento con QT. De acuerdo con estudios de mundo real, nivolumab ha mostrado beneficio en este subgrupo de pacientes.37
La Figura 4 muestra el algoritmo de tratamiento del cáncer de nasofaringe.
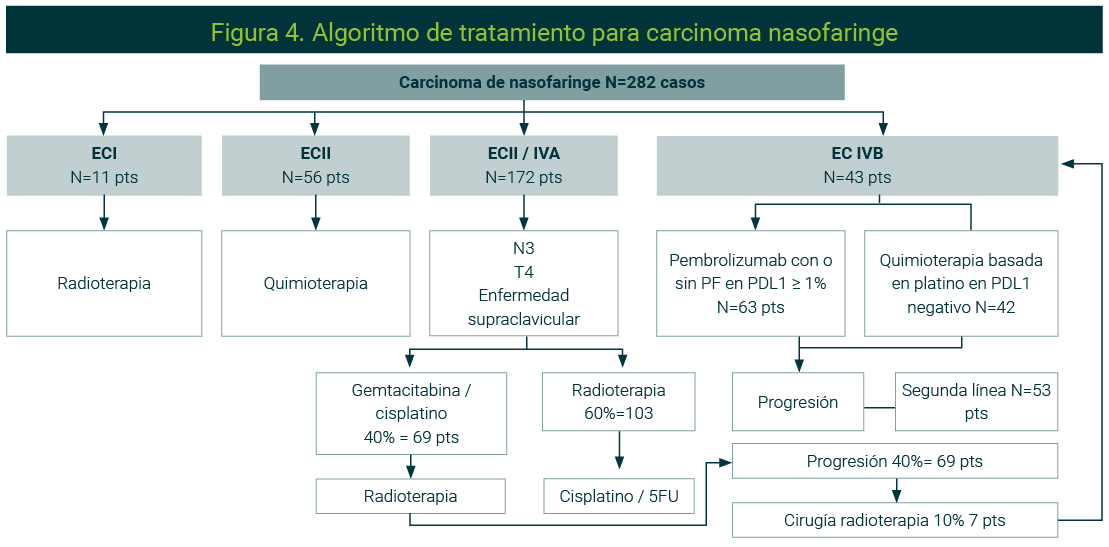
Algoritmo realizado por los autores.
Los carcinomas de las VAD son relativamente frecuentes y afectan catastróficamente la vida de los pacientes. El abordaje multidisciplinario de estas neoplasias es fundamental para el éxito del tratamiento. El pronóstico se basa en el estadio al diagnóstico y la posibilidad de ofrecer un tratamiento radical.
En la mayoría de los casos se requiere de un manejo combinado con cirugía, radioterapia y tratamiento sistémico, además de los cuidados de soporte. La decisión de la secuencia de tratamiento por el equipo multidisciplinario se basará en las características clinicopatológicas de cada caso; es decir, deberá ser individualizado. La cirugía y la radioterapia son las únicas opciones con intento curativo. En la enfermedad recurrente y/o metastásica, la inmunoterapia ha mostrado incrementar la supervivencia global y brindar una opción de tratamiento a estos pacientes, aunque la quimioterapia sigue siendo fundamental en muchos casos.
Los autores declaran que no tienen conflicto de interés.
| 1. | Argiris A, Karamouzis MV, Raben D, Ferris RL. Head and neck cancer. Lancet. 2008;371(9625):1695-709. |
| 2. | Ferlay J, Colombet M, Soerjomataram I, Parkin DM, Piñeros M, Znaor A, et al. Cancer statistics for the year 2020: An overview. Int J Cancer. 2021; 149(4):778-89. |
| 3. | Sierra MS, Soerjomatarama I, Antoni S, Laversanne M, Piñeros M, de Vries E, et al. Cancer patterns and trends in Central and South America. Cancer Epidemiol. 2016;(44 Suppl 1):S23-S42. |
| 4. | Hashibe M, Brennan P, Benhamou S, Castellsague X, Chen C, Curado MP, et al. Alcohol drinking in never users of tobacco, cigarette smoking in never drinkers, and the risk of head and neck cancer: Pooled analysis in the International Head and Neck Cancer Epidemiology Consortium. J Natl Cancer Inst. 2007;99(10):777-89. |
| 5. | National Cancer Institute. Surveillance, Epidemiology, and End Results Program. Cancer stat facts: Oral cavity and pharynx cancer. Available from URL: https://seer.cancer.gov/statfacts/html/oralcav.html |
| 6. | National Cancer Institute. Surveillance, Epidemiology, and End Results Program. Cancer stat facts: Larynx cancer. Available from URL: http://seer.cancer.gov/statfacts/html/laryn.html |
| 7. | Ho AS, Kraus DH, Ganly I, Lee NY, Shah JP, Morris LGT. Decision making in the management of recurrent head and neck cancer. Head Neck. 2014;36(1):144-51. |
| 8. | Pignon JP, le Maître A, Maillard E, Bourhis J, MACH-NC- Collaborative Group. Meta-analysis of chemotherapy in head and neck cancer (MACH-NC): An update on 93 randomised trials and 17,346 patients. Radiother Oncol. 2009;92(1):4-14. |
| 9. | Bonner JA, Harari PM, Giralt J, Azarnia N, Shin DM, Cohen RB, et al. Radiotherapy plus cetuximab for squamous-cell carcinoma of the head and neck. N Engl J Med 2006;354(6):567-78. |
| 10. | Vermorken JB, Mesia R, Rivera F, Remenar E, Kawecki A, Rottey S, et al. Platinum-based chemotherapy plus cetuximab in head and neck cancer. N Engl J Med. 2008;359:(11):1116-27. |
| 11. | Ferris RL, Blumenschein, Jr G, Fayette J, Guigay J, Colevas AD, Licitra L, et al. Nivolumab for recurrent squamous-cell carcinoma of the head and neck. N Eng J Med. 2016;375(19):1856-67. |
| 12. | Burtness B, Harrington KJ, Greil R, Soulieres D, Tahara M, de Castro G Jr, et al. Pembrolizumab alone or with chemotherapy versus cetuximab with chemotherapy for recurrent or metastatic squamous cell carcinoma of the head and neck (KEYNOTE-048): A randomised, open-label, phase 3 study. Lancet. 2019;394(10212):1915-28. |
| 13. | Dayyani F, Etzel CJ, Liu M, Ho CH, Lippman SM, Tsao AS. Meta-analysis of the impact of human papillomavirus (HPV) on cancer risk and overall survival in head and neck squamous cell carcinomas (HNSCC). Head Neck Oncol. 2010; 2:15. |
| 14. | Ang KK, Harris J, Wheeler R, Weber R, Rosenthal DI, Nguyen-Tan PF, et al. Human papillomavirus and survival of patients with oropharyngeal cancer. N Engl J Med. 2010; 363(1):24-35. |
| 15. | Harrington KJ, Ferris RL, Blumenschein G Jr, Colevas AD, Fayette J, Licitra L, et al. Nivolumab versus standard, single-agent therapy of investigator’s choice in recurrent or metastatic squamous cell carcinoma of the head and neck (CheckMate 141): Health-related quality-of-life results from a randomised, phase 3 trial. Lancet Oncol. 2017;18(8):1104-15. |
| 16. | Chhabra N, Chhabra S, Sapra N. Diagnostic modalities for squamous cell carcinoma: An extensive review of literature-considering toluidine blue as a useful adjunct. J Maxillofac Oral Surg. 2015;14(2):188-200. |
| 17. | Harrison LB, Sessions RB, Hong WK (eds.). Head and neck cancer: a multidisciplinary approach. Lippincott Williams & Wilkins; 2009. |
| 18. | Abraham J. Imaging for head and neck cancer. Surg Oncol Clin N Am. 2015;24(3): 455-71. |
| 19. | van Schaik JE, Halmos GB, Witjes MJH, Plaat BEC. An overview of the current clinical status of optical imaging in head and neck cancer with a focus on narrow band imaging and fluorescence optical imaging. Oral Oncol. 2021;121:105504. |
| 20. | Shellenberger TD, Weber RS. Multidisciplinary team planning for patients with head and neck cancer. Oral Maxillofac Surg Clin North Am. 2018;30(4):435-44. |
| 21. | Mäkitie AA, Alabi RO, Orell H, Youssef O, Almangush A, Homma A, et al. Managing cachexia in head and neck cancer: A systematic scoping review. Adv Ther. 2022;39(4):1502-1523. |
| 22. | Megwalu UC, Sikora AG. Survival outcomes in advanced laryngeal cancer. JAMA Otolaryngol Head Neck Surg. 2014;140(9):855-60. |
| 23. | Winquist E, Oliver T, Gilbert R. Postoperative chemoradiotherapy for advanced squamous cell carcinoma of the head and neck: A systematic review with meta‐analysis. Head Neck. 2007;29(1):38-46. |
| 24. | Vokes EE, Kies MS, Haraf DJ, Stenson K, List M, Humerickhouse R, et al. Concomitant chemoradiotherapy as primary therapy for locoregionally advanced head and neck cancer. J Clin Oncol. 2000;18(8):1652-61. |
| 25. | Lacas B, Carmel A, Landais C, Wong SJ, Licitra L, Tobias JS, et al. Meta-analysis of chemotherapy in head and neck cancer (MACH-NC): An update on 107 randomized trials and 19,805 patients, on behalf of MACH-NC Group. Radiother Oncol. 2021; 156:281-293. |
| 26. | Greven KM, Williams 3rd DW, McGuirt Sr WF, Harkness BA, D’Agostino Jr RB, Keyes Jr JW, et al. Serial positron emission tomography scans following radiation therapy of patients with head and neck cancer. Head Neck. 2001;23(11): 942-46. |
| 27. | va Weert S, Leemans CR. Salvage surgery in head and neck cancer. Oral Dis. 2021;27(1):117-24. |
| 28. | Szturz P, Vermorken JB. Translating KEYNOTE-048 into practice recommendations for head and neck cancer. Ann Transl Med. 2020;8(15):975. |
| 29. | Rivera F, García-Castaño A, Vega N, Vega-Villegas ME, Gutiérrez-Sanz L. Cetuximab in metastatic or recurrent head and neck cancer: The EXTREME trial. Expert Rev Anticancer Ther. 2009;9(10):1421-28. |
| 30. | Guigay J, Aupérin A, Fayette J, Saada-Bouzid E, Lafond C, Taberna M, et al. Cetuximab, docetaxel, and cisplatin versus platinum, fluorouracil, and cetuximab as first-line treatment in patients with recurrent or metastatic head and neck squamous-cell carcinoma (GORTEC 2014-01 TPExtreme): A multicentre, open-label, randomised, phase 2 trial. Lancet Oncol. 2021;22(4): 463-75. |
| 31. | Hitt R, Irigoyen A, Cortes-Funes H, Grau JJ, García-Sáenz JA, Cruz-Hernandez JJ, et al. Phase II study of the combination of cetuximab and weekly paclitaxel in the first-line treatment of patients with recurrent and/or metastatic squamous cell carcinoma of head and neck. Ann Oncol. 2012;23(4):1016-22. |
| 32. | Chang ET, Ye W, Zeng YX, Adami HO. The evolving epidemiology of nasopharyngeal carcinoma. Cancer Epidemiol Biomarkers Prev. 2021;30(6):1035-47. |
| 33. | Chen YP, Chan AT, Le QT, Blanchard P, Sun Y, Ma J. Nasopharyngeal carcinoma. Lancet. 2019;394(10192):64-80. |
| 34. | Blanchard P, Lee A, Marguet S, Leclercq J, Ng WT, Ma J, et al. Chemotherapy and radiotherapy in nasopharyngeal carcinoma: An update of the MAC-NPC meta-analysis. Lancet Oncol. 2015;16(6):645-55. |
| 35. | Zhang Y, Chen L, Hu GQ, Zhang N, Zhu XD, Yang KY, et al. Gemcitabine and cisplatin induction chemotherapy in nasopharyngeal carcinoma. N Engl J Med. 2019;381(12):1124-35. |
| 36. | Tian K, Han J, Wang Z, Chen J. Immune checkpoint inhibition in first-line treatment for recurrent or metastatic nasopharyngeal carcinoma: A CAPTAIN-1st and JUPITER-02 trial-based cost-effectiveness analysis. Oral Oncol. 2022;128:105842. |
| 37. | Dietz A, Welslau M, Hahn D, Langer C, Bockmühl U, Müller-Huesmann H, et al. HANNA: Real-world outcomes from an observational study with nivolumab in patients with recurrent or metastatic squamous cell carcinoma of the head and neck in Germany. Abstract 6532, 2020. Available from URL: https://ascopubs.org/doi/10.1200/JCO.2020.38.15_suppl.6532 |
All Rights Reserved® 2019
Latin American Journal of Clinical Sciences and Medical Technology,Publicación contínua • Editor responsable: Gilberto Castañeda Hernández. • Reserva de Derechos al Uso Exclusivo: 04-2019-062013242000-203; ISSN: 2683-2291; ambos otorgados por el Instituto Nacional del Derecho de Autor. • Responsable de la última actualización de este número, Web Master Hunahpú Velázquez Martínez,
Calle Profesor Miguel Serrano #8, Col. Del Valle, Alcaldía Benito Juárez, CP 03100, Ciudad de México, México. Número telefónico: 55 5405 1396 • Fecha de última modificación, 28 de agosto de 2024.
All Rights Reserved® 2019
Publicación contínua • Editor responsable: Gilberto Castañeda Hernández. • Reserva de Derechos al Uso Exclusivo: 04-2019-062013242000-203; ISSN: 2683-2291; ambos otorgados por el Instituto Nacional del Derecho de Autor. • Responsable de la última actualización de este número, Web Master Hunahpú Velázquez Martínez,
Calle Profesor Miguel Serrano #8, Col. Del Valle, Alcaldía Benito Juárez, CP 03100, Ciudad de México, México. Número telefónico: 55 5405 1396 • Fecha de última modificación, 28 de agosto de 2024.