| ** | Latin American Journal of Clinical Sciences and Medical Technology is an open access magazine. To read all published articles and materials you just need to register Registration is free of charge. Register now If you already have registered please Log In | ** |
aInstituto Nacional de Cancerología, Ciudad de México, México; bHospital Regional de Alta Especialidad Bajío, Guanajuato, México; cHospital de Especialidades "Siglo XXI", Instituto Mexicano del Seguro Social, Ciudad de México, México; dInstituto Nacional de Ciencias Médicas y Nutrición “Salvador Zubirán”, Ciudad de México, México; eDirección General de Coordinación de los Hospitales Regionales de Alta Especialidad, Ciudad de México, México; fUniversidad Autónoma de Nuevo León, Facultad de Medicina y Hospital Universitario Dr. José Eleuterio González, Monterrey, Nuevo León, México; gCentro Médico ABC, Ciudad de México. México; hHospital Juárez de México, Ciudad de México, México; iHospital General de México, Ciudad de México, México; jCentro de Hematología y Medicina Interna, Clínica Ruiz, Puebla. México.
Autor para correspondencia: , . Números telefónicos: ; e-mail: victorurbalejo07@gmail.com
Lat Am J Clin Sci Med Technol. 2023 Mar;5:96-106.
Recibido: 12 de enero, 2023
Aceptado: 15 de febrero, 2023
Publicado: 08 de marzo, 2023
Vistas: 11992
Descargas: 33
La leucemia linfoblástica aguda (LLA) es una proliferación maligna de células linfoides (linfoblastos) que pueden ser precursoras de células B o T. La edad de inicio más frecuente es de 1-4 años de edad, y en los adolescentes y adultos jóvenes de los 15-39 años. La respuesta de la enfermedad se encuentra regulada por la heterogeneidad, biología de la enfermedad, factores de riesgo, reordenamientos cromosómicos, variaciones estructurales y en las secuencias de mutaciones que logran alterar la maduración de la línea linfoide; ello causa proliferación celular y alteraciones en su regulación. La introducción de esquemas basados en L-asparaginasa, el uso de inhibidores de tirosin cinasa, así como la inmunoterapia con blinatumomab han mejorado de forma notable la respuesta y supervivencia de los pacientes entre el 60% y el 70%. La oncoguía de leucemia linfoblástica aguda tiene como finalidad mostrar el panorama actual de esta patología, guiar en la utilización de las herramientas para el diagnóstico, la estadificación del riesgo y, finalmente, ofrecer las mejores opciones de tratamiento disponibles.
Acute lymphoblastic leukemia (ALL) is a malignant proliferation of lymphoid cells (lymphoblasts) that can be precursors of B or T cells. The most frequent age of onset is 1-4 years and in adolescents and young adults of 15-39 years old. The disease response is regulated by heterogeneity, disease biology, risk factors, chromosomal rearrangements, structural variations, and contact sequences that alter the lymphoid lineage's maturation; that causes cell activation and alterations in its regulation. The introduction of schemes based on L-asparaginase, the use of tyrosine kinase inhibitors, as well as immunotherapy with blinatumomab have significantly improved the response and survival of patients between 60% and 70%. The objective of these guidelines of acute lymphoblastic leukemia is to show the current panorama of this pathology, guide the use of diagnostic tools, risk staging and, finally, offer the best available treatment options.
Esta guía incluye sugerencias y recomendaciones elaboradas por un grupo de expertos para el manejo de pacientes con leucemia linfoblástica aguda (LLA) en condiciones ideales; no incluye razonamientos costo-eficientes, ni determinantes para la compra de medicamentos. Su objetivo es proporcionar una pauta terapéutica basada tanto en la experiencia de diversas instituciones como en la evidencia de mayor peso publicada recientemente para que los profesionales de la salud dispongan de tal información en beneficio de los pacientes con LLA, la cual representa el 20% de las leucemias en los adultos.
Epidemiología
La LLA es una proliferación maligna de células linfoides en estadios tempranos de diferenciación (linfoblastos) que invaden la médula ósea, sangre y sitios extramedulares. Puede ser de precursores de células B (80%) o T (20%).1
Tiene una incidencia estimada de 1.57 casos por 100,000 habitantes por año.1 Representa el 4% (35,470) de los casos de cáncer estimados en 2020 en hombres y el 3% (25,060) de los casos de cáncer en la mujer en Estados Unidos. Es ligeramente más común en hombres que en mujeres 1.2:1.
La edad de presentación más frecuente es de 1-4 años y en los adolescentes y adultos jóvenes (AYA, adolescent and young adult) de los 15 a los 39 años. Representa el 20% de las leucemias en los adultos. La leucemia linfoblástica se diagnostica antes de los 20 años de edad (alrededor del 60 %). Aunque existen pocos estudios en población mexicana, se reportan prevalencias similares en hombres y mujeres, y edad de presentación del 60% en menores de 30 años.2,3
Factores predisponentes
La mayoría de los pacientes con leucemia está sana, pero existen factores predisponentes como la susceptibilidad genética (síndrome de Down, anemia de Fanconi, ataxia telangiectasia, síndrome de Bloom, variaciones genéticas inherentes [ARID5B, IKZF1, CEBPE], polimorfismos de nucleótidos sencillos [rs12402181 en miR-3117)] y factores de riesgo ambientales (infecciones en la infancia, pesticidas y radiación ionizante).1
El diagnóstico de la LLA requiere de la identificación de 20% o más de blastos leucémicos de origen linfoide (linfoblastos) en la médula ósea o sangre periférica. Si los linfoblastos se limitan a una masa en un ganglio linfático u otro tejido linfático y menos del 20% de las células de la médula ósea son linfoblastos, se denomina linfoma linfoblástico, aunque muchas veces la denominación leucemia/linfoma linfoblástico es correcta.4
La presentación clínica es de inicio agudo, caracterizado por síndromes anémico, hemorragíparo y febril. La hepato-esplenomegalia y el dolor óseo pueden estar presentes. La biometría hemática reporta generalmente leucocitosis con blastos, anemia y trombocitopenia.4
Para completar el diagnóstico se requiere de un panel completo de laboratorio, inmunofenotipo en sangre o médula ósea, además de cariotipo, reacción en cadena de polimerasa (RT PCR) para cromosoma Philadelphia (BCR-ABL) y punción lumbar si se sospecha de enfermedad en sistema nervioso central (SNC).5
Clasificación por inmunofenotipo6,7
La clasificación inmunológica de las leucemias agudas debe hacerse idealmente por citometría de flujo multiparamétrica con diez colores, idealmente. Se emplean diversas clasificaciones inmunológicas mediante los siguientes marcadores:
- Marcadores de células B: Tdt, CD10, CD19, CD20, CD22, CD79a
- Marcadores de células T: CD1a, CD2, CD3, CD4 +/- CD8, CD5, CD7
Los subtipos de LLA, así como las clasificaciones por citogenética y por riesgo se muestran en las tablas 1 a 3.
| Tabla 1. Subtipos de LLA8 | |||
|---|---|---|---|
| B |
| T |
|
| La tabla es propiedad de los autores. | |||
| Tabla 2. Clasificación por citogenética |
|---|
Favorable |
|
Desfavorable5 |
|
| La tabla es propiedad de los autores. |
| Tabla 3. Clasificación de riesgo |
|---|
Favorable o riesgo estándar |
|
Desfavorable o riesgo alto |
|
| La tabla es propiedad de los autores. |
Enfermedad mínima (medible) residual
La persistencia de enfermedad mínima (medible) residual, posterior al tratamiento de inducción de la LLA, se asocia con altas tasas de recaídas y disminución de la supervivencia global (SG), de acuerdo con múltiples estudios.
En México, la forma más común de medirla es mediante la citometría de flujo (CF), con capacidad de detectar células leucémicas residuales en 1 de cada 10,000 células (1x10-4 ó 0.01%); sin embargo, con muestras con adecuada celularidad, la CF de ocho colores puede alcanzar una sensibilidad de 1x10-5.
Los estudios cuantitativos de reacción en cadena de la polimerasa (PCR), para identificar reordenamientos clonales de la cadena pesada de la inmunoglobulina (IGH) o del receptor de células T (TCR), tienen su mayor uso en países europeos. La PCR puede alcanzar niveles más altos de sensibilidad que la CF convencional, lo cual se traduce en mejor predicción del pronóstico.9
El desarrollo de la secuenciación de nueva generación (NGS, new-generation sequencing) es altamente sensible y es capaz de detectar niveles de 1x10-6, lo que favorece la toma de decisiones terapéuticas de forma más precisa.10
Independientemente de la técnica que se tenga disponible, la evaluación de la EMR es imprescindible para una adecuada estratificación del riesgo en la LLA. De acuerdo con múltiples estudios prospectivos realizados en niños y adultos, los pacientes con respuesta completa (RC) molecular tras la consolidación tienen una probabilidad significativamente mayor de remisión completa continua (RCC; 74% frente a 35%; P <0.0001) y de SG (80% vs. 42%; P 0.0001), en comparación con los pacientes con falla molecular. Éste es el factor pronóstico aislado más importante y debe utilizarse para tomar decisiones terapéuticas, incluida la elección de realizar trasplante de médula ósea en pacientes con EMR positiva (riesgo alto) o identificar pacientes de riesgo bajo en los que se puede disminuir la intensidad del tratamiento.9
En la última década, los desenlaces en adultos han mejorado de forma significativa, en parte debido a la utilización de esquemas de inspiración pediátrica al tratamiento de adultos jóvenes, TKI en leucemias Philadelphia+, uso de inmunoterapia y mejor estratificación de riesgo para seleccionar pacientes que se beneficien de trasplante.
A continuación se muestran los esquemas de inspiración pediátrica que más se utilizan en el país.
- Primera línea
- BFM-like. Evaluó a 85 pacientes con LLA Ph- entre 12 y 40 años de 2006 a 2012, tratados con protocolo intensivo. La mediana de seguimiento fue de 40 meses. La tasa de RC fue de 94%. La leucocitosis inicial fue un factor predictivo independiente, relacionado con SG y supervivencia libre de progresión (SLP). El estado de EMR en D29 y D84 fue predictivo de resultados a largo plazo. La SG a 3 años fue de 74%.11
- CALGB 10403 modificado. Está basado en el estudio multicéntrico del grupo colaborativo en EUA, con algunas modificaciones, sobre todo, en disponibilidad local: cambio de pegaspargasa por l'asparaginasa de E. coli, incorporación de rituximab, cambio de tioguanina por 6-mercaptopurina. En el estudio original se incluyeron 318 pacientes y se demostró una SG10 a 3 años de 73%.12
- Los resultados de un estudio local en el que se incluyeron 95 pacientes con LLA B y T entre 14-49 años. La mediana de edad fue de 23 años, la tasa de RC fue del 87.8%, con EMR <0.01% en 39.1%, la SG a 2 años fue del 72.1%. La EMR <0.1% post-inducción se asoció con SG más prolongada; la hiperleucocitosis y el sobrepeso con SG y SLP fueron más cortas.13
- Primera línea
- Hyper-CVAD. Se incluyeron 288 pacientes con LLA, entre 1994 y 2000. La mediana de edad fue de 40 años. La tasa de RC fue de 92%; y la tasa de mortalidad fue del 5% en la inducción. La SG a 5 años fue de 38%. En el análisis multivariado, la hiperleucocitosis, edad >45 años y ECOG bajo fueron de mal pronóstico.14
- Hyper-CVAD + blinatumomab. En un estudio fase II de 2016 al 2020 se evaluaron pacientes mayores de 14 años, con LLA B Ph-. Recibieron 4 ciclos de Hyper-CVAD, seguidos de 4 ciclos de blinatumomab como consolidación. Se incluyeron 38 pacientes, con una media de edad de 37 años, supervivencia libre de enfermedad (SLE) de 73%, y sin recaídas a 2 años.15
- Estudio ECOG-ACRIN E1910. Evaluó el esquema de quimioterapia BFM (Berlin-Frankfurt-Munich), asociada con blinatumomab como consolidación en pacientes con EMR negativa (<0.01%). Se incluyeron pacientes de 30-70 años, tasa de RC post inducción del 81%, EMR post intensificación 78%, la SG del Blina+QT del 83% y de QT 65%.16
- Blinatumomab. En 2018, la Food and Drug Administration (FDA) aprobó el uso de blinatumomab para pacientes en CR1 o CR2 con EMR+, según los resultados del ensayo BLAST. Éste incluyó a 116 pacientes con LLA con EMR ≥0.01%. La tasa de EMR- fue de 85.2% y de 72% para los pacientes en CR1 y CR2, respectivamente. La mediana de SG a 5 años no se alcanzó para los pacientes en CR1 con EMR- y fue de 38.8 meses para los tratados en CR2.17
- Esquemas de moderada intensidad
- PETHEMA. La media de edad fue de 66 años, la RC fue de 74% con SG de 30% a 2 años. Se observaron infecciones grado 3-4 en el 62% de los pacientes en la inducción; mientras que las consolidaciones fueron mejor toleradas, incluido el uso de asparaginasa.18
- GMALL. Dosis reducidas de esquema basado en pediatría (BFM). Tasa de muerte temprana 14%, mortalidad en remisión 6%. Tasa de RC global 76% y por grupo de edad: RC en pacientes entre 55-65 años (84%), 66-75 años (74%), 75-85 años (52%). Tasa de SG a los 5 años de 23%. Es importante señalar que la tasa de RC incrementó a 86% y mortalidad temprana disminuyó a 0% con el uso de citarabina liposomal como profilaxis a SNC.19
- Esquemas de baja intensidad
- POMP/blinatumomab. En el estudio SWOG 1318 se incluyeron pacientes de >65 años con LLA. Mediana de edad 75 años. Los pacientes recibieron dos ciclos de inducción de blinatumomab, posteriormente tres ciclos de consolidación y mantenimiento con POMP por 18 meses. El 66% de los pacientes obtuvo RC, la SLE estimada a los 3 años fue de 37% y la SG estimada a 3 años 37%.20
- PETHEMA. Pacientes adultos mayores y frágiles (ALL-07FRAIL). Pacientes con índice de comorbilidad de Charlson (ICC) ≥4. Inducción basada en vincristina y dexametasona + mantenimiento por 2 años con mercaptopurina y metotrexato (MTX). Se incluyeron 72 pacientes, con una mediana de edad de 67 años (57-89) y mediana de ICC 5 (4-12). Tasa RC 54%, muerte temprana 10%, resistencia 31%. Mediana de SLE fue de 6.9 meses (95% [IC], 0.3-13.5 meses), mediana de SG 7.6 meses (95% [IC], 6.3-8.9 meses). Los eventos adversos más frecuentes fueron hematológicos, grado 3-4 (neutropenia 77% y trombocitopenia 54%). La mitad de pacientes obtuvo RC, éstos podrían beneficiarse de inmunoterapia concomitante o subsecuente.21
- Mini-HyperCVAD + inotuzumab ozogamicin. Realizado en el MD Anderson Cancer Center, en un estudio fase II. Se incluyeron 46 pacientes, mediana de edad de 68 años. Tasa de RC global 95% y 71% de estos pacientes obtuvieron EMR negativa. A los 3 años, la SLP fue de 76% y la SG de 52%. Nueve por ciento de los pacientes desarrolló enfermedad veno-oclusiva (EVO) y dos pacientes fallecieron por esta causa. Otras toxicidades grado 3-4 fueron trombocitopenia (74%), hemorragia (13%), infección durante la inducción (54%), infección durante consolidación (74%), hiperbilirrubinemia (17%), incremento ALT/AST (20%), hiperglucemia (52%) e hipocalcemia (35%). No está disponible en México.22
- Inotuzumab ozogamicin + mini-hyper-CVD + blinatumomab. Es un estudio realizado en MD Anderson Cancer Center. Se incluyeron 135 pacientes (>60 años), de los cuales 77 fueron tratados con HyperCVD estándar y 58 con inotuzumab ozogamicin + mini-hyperCVD con o sin blinatumomab. Recibieron 8 ciclos de mini-hyper-CVD y mantenimiento con POMP durante 3 años. Inotuzumab fue administrado a 1.8 mg/m2 durante inducción y 1.3 mg/m2 durante consolidación, pero debido a EVO, la dosis se redujo a 1.3 mg/m2 y 1.0 mg/m2, respectivamente. Después de 4 ciclos de mini-hyperCVAD, a los pacientes se les administraron 4 ciclos de blinatumomab de consolidación a dosis estándar. El mantenimiento fue alternando bloques de 3 meses con POMP y un ciclo de blinatumomab hasta un total de 16 ciclos. El tratamiento combinado logró una tasa de respuesta de 98% vs. 88% con hyperCVD estándar y baja tasa de mortalidad en RC (5% vs. 17%). La tasa de SLE a los 3 años con la combinación fue de 64% (mediana no alcanzada) vs. 34% (mediana 15 meses) con hyperCVD (p=0.003). La SG a los 3 años 63% (mediana no alcanzada) vs. 34% (mediana 17 meses), respectivamente (p=0.004). No está disponible en México.23
- IDAFLAG. En un estudio en 2005 se incluyeron 23 pacientes con LLA en recaída/refractarios. Las RC fueron de 39.1%; 56.5% fue refractario; la mortalidad en la reinducción fue de <5%. La media de SG fue de 4.5 meses, para los respondedores las SLE y SG fueron de 6 y 9 meses, respectivamente.24
- Hyper-CVAD aumentado se basa en adicionar a la estructura del esquema, una dosis intensificada de vincristina, dexametasona y asparaginasa (L-asparaginasa o pegasparaginasa). En el MD Anderson CC, Faderl y colaboradores estudiaron a 90 pacientes que recibieron el esquema HyperCVAD aumentado en su mayoría LLA-B. De los 88 pacientes evaluables, el 47% integró RC con una media de duración de 5 meses, lo cual permitió que 32% pudiera acceder a un trasplante de progenitores hematopoyéticos.25
- Blinatumomab es un anticuerpo biespecífico CD3/CD19 con una alta eficacia en contra de las células leucémicas B, en especial con una enfermedad limitada. El estudio multicéntrico TOWER demostró la superioridad sobre la quimioterapia estándar en pacientes que ya contaban con múltiples esquemas previos (RC 34% versus 16%, P<0.001), así como aumento en la supervivencia (7.7 meses versus 4 meses, P=0.001), en especial en los casos en primera recaída.26,27 En un análisis de seguimiento a largo plazo de los estudios fase II que incluyeron el uso de blinatumomab, la media de SLE en los pacientes que integraron remisión en los primeros 2 ciclos fue de 7.7 meses (6.2-10 meses, 95% IC), con una SG a 3 años de 17.7%, pero en los que alcanzaron a ser trasplantados la supervivencia fue mayor (37.2% a 3 años).28
- El inotuzumab ozogamicin (IO) es un anticuerpo monoclonal anti-CD22 unido a calicheamicina (un agente alquilante de ADN). En el estudio INNOVATE fase III, el tratamiento con IO logró una tasa de RC significativamente mayor (80.7% vs. 29.4%, p<0.001) que la quimioterapia intensiva estándar en adultos con LLA-B R/R y fue aprobada por la FDA para pacientes R/R.29 No está disponible en México.
- La terapia con células CAR-T (chimeric antigen receptor) es una opción que ha mostrado respuestas en poblaciones refractarias. Las células CAR-T son células T del paciente, modificadas genéticamente para identificar y eliminar las células malignas mediante el reconocimiento de antígenos específicos del tumor. En LLA-B, las células CAR se dirigen contra CD19 y también se desarrollaron CAR-T contra CD22. Los reportes iniciales en pacientes refractarios muestran tasas de RC de 70-90%, tanto en niños como adultos, aunque con toxicidades significativas como el síndrome de liberación de citocinas (SLC). El tisagenlecleusel (CAR-T contra el antígeno CD19) fue aprobado recientemente por FDA para los pacientes R/R a varias líneas de tratamiento en pacientes de 1 a 25 años de edad.30 No está disponible en México.
La introducción de los inhibidores de tirosina ha derivado en una mejora notable en el resultado del tratamiento de esta leucemia; la supervivencia ahora oscila entre 40% y el 50% con imatinib + quimioterapia (QT) combinada.31
El enfoque estándar actual es la combinación de un protocolo de QT que emplea de cuatro a cinco agentes citotóxicos que se usan típicamente para la LLA y se combinan con imatinib en una dosis diaria simultánea de 400 mg a 800 mg.32
Las tasas de remisión completa en estos estudios superaron sistemáticamente el 90%. El perfil y la incidencia de toxicidad grave no fueron diferentes a los asociados con los regímenes históricos de quimioterapia sola. La SG estimada en los diferentes estudios osciló entre el 36% y el 76% a 1-3 años de seguimiento.33 El estudio francés GRAAPH-2003 tuvo SG de 52% a 4 años versus 20% en la era pre imatinib.34
Esquemas no intensivos
Evitar la toxicidad de la QT intensiva es muy importante en México debido al alto porcentaje de mortalidad asociado con dicho tratamiento. En otro estudio del grupo francés realizado por Rea et al., el uso inicial de QT no intensiva (vincristina + esteroide + imatinib a dosis de 800 mg al día) obtuvo tasas de RC de 90%, y la mortalidad se redujo durante la inducción. Once pacientes murieron; la media de SG fue de 404 días.35
En pacientes ancianos con LLA Ph +, el GIMEMA realizó un estudio en el que los pacientes mayores de 60 años recibieron un tratamiento de inducción de 45 días con imatinib (800 mg/día) en combinación con prednisona, seguido de mantenimiento con imatinib hasta recidiva de la enfermedad o toxicidad excesiva. Todos los pacientes alcanzaron la remisión completa y no hubo muertes en RC. Sin embargo, la mediana de duración de la remisión fue de sólo ocho meses y la mediana de supervivencia desde el diagnóstico fue de 20 meses.36
Otros TKI
Los inhibidores de tirosina cinasa (TKI, tyrosine kinase inhibitors) de segunda generación combinados con QT intensiva o de baja intensidad dieron como resultado tasas de RC más altas que con los regímenes basados en imatinib.36
La combinación de dasatinib con una variedad de regímenes de quimioterapia citotóxica tanto en pacientes jóvenes como de edad avanzada con LLA Ph+de novo (o mínimamente pretratada) se exploró en ensayos recientes de fase II.37
Las tasas de RC superaron el 90%, independientemente del régimen utilizado; las tasas de remisión molecular oscilaron entre el 28% y el 72%.32
Ponatinib es un TKI de tercera generación con amplio espectro de inhibición de cinasas. Es activo frente a la mayoría de las mutaciones BCR-ABL1 conocidas y es el único TKI con actividad frente a los subclones Ph+ LLA con la mutación T315I. Ha mostrado actividad clínica en la LLA Ph+ en recaída o refractaria y en el entorno de primera línea, en combinación con quimioterapia.38
La combinación de Hyper-CVAD y ponatinib dio como resultado una tasa de RC general de 84%, una tasa de supervivencia a 5 años de 73% y 86% entre los pacientes que se sometieron y no se sometieron a SCT alogénico, respectivamente. Ello sugiere que es posible que el trasplante alogénico de células madre (SCT, stem-cell transplant) no sea necesario con este régimen. Sin embargo, la posibilidad de que exista un rearreglo tipo Ph-like con positividad para IKZF1, CDKN2A/B u otra mutación de mal pronóstico, además de la posible necesidad de usar TKI de forma indefinida, hacen que el trasplante siga siendo (hasta ahora) una opción útil y menos costosa en este contexto.39
Esquemas sin QT
La reciente combinación sin QT de dasatinib y blinatumomab fue segura y eficaz en pacientes con LLA Ph+, recién diagnosticada y dio como resultado una tasa de SG estimada a 3 años del 80%; el 50% de los pacientes se sometió a SCT alogénico.
El régimen sin QT de ponatinib y blinatumomab resultó en una tasa de RC de 86% y una tasa de SG a los 2 años de 93%, sin recaídas ni muertes relacionadas con la leucemia, excepto un paciente que se sometió a SCT alogénico. Ello sugiere que el SCT alogénico pudiera no ser necesario con este régimen, particularmente cuando la ERM es negativa.40 En todos los tratamientos anteriores debe incluirse la quimioterapia intratecal (QIT) para prevenir la recaída al SNC.
El sitio más común de infiltración es el SNC, lo cual se define como evidencia morfológica inequívoca de linfoblastos en el líquido cefalorraquídeo (LCR), detectada por cytospin, CF, o parálisis de pares craneales, o falla neurológica.41 Tiene una prevalencia del 5-10% al momento del diagnóstico e incrementa hasta 40% en la recaída. Las recaídas aisladas oscilan entre 0% y 11%; mientras que asociado a compromiso sistémico se encuentra entre 1 y 4%.42
Factores de riesgo
- Recuento elevado de leucocitos
- Inmunofenotipo de células T
- Translocaciones t (1;19) y t (9;22)
- Leucemia de linaje mixto
- Reordenamientos citogenéticos en MLL/KMT2A
- Hipodiploidías
- Fusión de TCF3-PBX143
La citomorfología por cytospin es el estándar de oro; sin embargo, tiene especificidad del 95% para el diagnóstico de infiltración a SNC y sensibilidad baja (50%).44
La sensibilidad de los métodos de diagnóstico actuales se considera inadecuada para determinar el tratamiento dirigido al SNC estratificado por riesgo, por lo que se utiliza la clasificación de infiltración a SNC (Tabla 4, guía argentina hematología 2019). Ello hace necesaria la búsqueda de nuevos biomarcadores que nos permitan predecir infiltración a SNC y en un futuro modificar el tratamiento con terapias blanco.45,46
| Tabla 4. Clasificación de infiltración a SNC | ||
|---|---|---|
| Estatus 1 (negativo) | Estatus 2 | Estatus 3 (positivo) |
| Sin evidencia clínica de enfermedad | Presencia de blastos y relación GR / GB ≤ 100: 1 analizados con el citocentrifugado con un recuento celular < o = 5/ mm3 Con esta relación GR / GB, la punción lumbar se considera no traumática y el LCR no contaminado con sangre | Presencia de lesión tumoral en cerebro o meninges evidenciada en TAC o RMN |
| Sin evidencia de imágenes patológicas en TAC y / o RMN atribuibles a LLA | Linfoblastos identificados y GR / GB > 100: 1 analizados con cytospin Con esta relación GR / GB, la punción lumbar se considera traumática y el LCR contaminado de sangre | Parálisis de par craneal, aunque no se detecten blastos en el LCR ni lesiones ocupantes demostrables por TAC y / o RMN |
| Fondo de ojo normal | Punción lumbar traumática (LCR contaminado de sangre): se combina con un recuento de GB inicial > 50.000/ mm3 | Punción lumbar no traumática donde se evidencia la presencia de >5 / mm3 células que, analizadas en el cytospin, corresponden mayoritariamente a blastos |
| Ausencia de blastos en LCR | ||
| SNC: sistema nervioso central; GR: glóbulo rojo; GB: glóbulo blanco; TAC: tomografía axial computarizada RMN: resonancia magnética nuclear; LLA: leucemia linfoblástica aguda; LCR: líquido cefalorraquídeo. La tabla es propiedad de los autores. | ||
El tratamiento actual dirigido al SNC comprende la terapia sistémica con buena penetración en el SNC, acompañada de QIT repetida que varía en número, según el esquema de 19 a 26 veces durante 2 a 3 años.47
La recaída en el SNC es una de las principales causas de fracaso del tratamiento entre los pacientes con LLA; por lo que las terapias actuales dirigidas al SNC también están asociadas con morbilidades significativas que incluyen deficiencias neurocognitivas, endocrinopatías y neoplasias malignas secundarias.
En consecuencia, se necesitan nuevas terapias contra la leucemia dirigidas al SNC para mejorar los resultados a largo plazo en la LLA y, al mismo tiempo, disminuir la morbilidad relacionada con el tratamiento.48
Profilaxis
Los pacientes de riesgo alto tienen mayor probabilidad de desarrollar una recaída extramedular; por tanto, la profilaxis adecuada para reducir este riesgo es crucial. En ausencia de ésta, se observa recurrencia en SNC en aproximadamente 30%.49
La profilaxis estándar consiste en QT sistémica e IT con o sin radioterapia (RT). La triple terapia IT es la más utilizada y se basa en MTX, citarabina y corticosteroides.50 Sin embargo, no mostró superioridad sobre la terapia de MTX como monoterapia.51 Se deben evitar las PL traumáticas, sobre todo en la inducción para evitar siembras directas.52
A pesar de profilaxis adecuada, alrededor del 10% desarrollará compromiso del SNC. Evaluar la mejor estrategia de tratamiento para la recaída en el SNC es incluso más desafiante por la falta de nuevos medicamentos y secuelas de neurotoxicidad. La terapia sistémica, como la dirigida al SNC, es esencial para la curación, independientemente del sitio de recaída.45
Si bien las opciones terapéuticas disponibles son las mismas que las utilizadas para la profilaxis, se adoptan estrategias como QIT más frecuentes (dos a tres veces por semana hasta su negativización o de acuerdo con el protocolo), así como la intensificación de la QT sistémica.50
Algunos protocolos contemplan la RT como parte del tratamiento. El SCT favoreció la SG 56% sobre la quimio/Rt 20-30%.52
- Pacientes con CD20+ >20%
- Adición de rituximab/ofatumumab5,8
- Trasplante de médula ósea
El SCT es una alternativa terapéutica eficaz para las personas con LLA. Las indicaciones se mencionan en la Tabla 5.
| Tabla 5. Indicaciones de trasplante alogénico en LLA (adaptado de Stelljes 2019)53 | |
|---|---|
| Edad | ≥40 años |
| Leucocitos al diagnóstico | >30x109 / L en LLA-B |
| ≥100x109 / L en LLA-T | |
| Citogenética de alto riesgo | t(9; 22) |
| t(4; 11)(q24.1;q32) | |
| Citogenética de alto riesgo | Cariotipo complejo |
| Hipodiploidía baja o triploidía | |
| LLA de precursores T-tempranos | |
| LLA similar al cromosoma Filadelfia | |
| Deleción IKZF1 en LLA-B | |
| NOTCH1 / FBXW7, NK-RAS, PTEN en LLA-T | |
| Respuesta al tratamiento | Enfermedad refractaria a cuatro semanas |
| EMR | ≥1x10-4 después de dos ciclos de tratamiento |
| La tabla es propiedad de los autores. | |
Los pacientes en recaída también deben recibir terapia celular, incluidos trasplante alogénico y terapia con células con receptores antigénicos quiméricos (CAR-T), ya que son las terapias que proporcionan las mayores probabilidades de curación y supervivencia a largo plazo.53-56
El SCT autólogo no es una terapia estándar en LLA, se considera opcional para pacientes con LLA de riesgo alto que no son elegibles para alo-trasplante, particularmente los que tienen EMR negativa. El beneficio de rescate con células hematopoyéticas autólogas (posterior a QT intensiva), en comparación con la quimioterapia convencional carece de evidencia en estudios prospectivos.57
El acondicionamiento en SCT alogénico puede incluir un esquema mieloablativo con irradiación corporal total (12-13 Gy) en combinación con ciclofosfamida o etopósido, o alternativamente busulfán y ciclofosfamida; se prefiere la administración intravenosa y con monitoreo de niveles de busulfán en plasma.55,58
Existe un ensayo aleatorizado en pacientes pediátricos que ha demostrado mejores desenlaces con el uso de irradiación corporal total.52 Para personas mayores de 50 años o para quienes tienen comorbilidades o deterioro en su clase funcional, el uso de acondicionamientos de intensidad reducida debe ser considerado, con varias opciones disponibles para el acondicionamiento, incluidos irradiación corporal total (≤8 Gy) o un alquilante (melfalán, busulfán, treosulfán) con fludarabina y/o ciclofosfamida.
El donante de elección es un donante HLA-idéntico relacionado. Cuando no existe un donante HLA-idéntico en la familia, se puede considerar la posibilidad de un SCT no relacionado HLA-idéntico. Si esto no es factible por premura, acceso o dificultades regulatorias, el uso de un donante haploidéntico es aceptable. Por último, el uso de unidades de cordón umbilical y de trasplantes no relacionados no idénticos son la tercera opción.53,59
La fuente celular, ya sea sangre periférica o médula ósea, no ha demostrado diferencias en SG. La sangre periférica se asocia con mayores tasas de enfermedad de injerto contra hospedero (EICH), recuperación temprana y menor tasa de falla primaria. Por otro lado, la médula ósea se asocia con menos tasa de EICH y recuperación más tardía.
La profilaxis para EICH estándar incluye inhibidores de calcineurina + metotrexato para receptores de un trasplante de donante idéntico, con globulina anti-timocito para los receptores de un trasplante no relacionado.53,55
Para receptores de trasplante haploidéntico, la ciclofosfamida postrasplante (50 mg/kg día +3 y +4) en combinación con micofenolato ha logrado reducir las tasas de EICH agudo y crónico grave. Su uso en trasplantes de donantes idénticos ha demostrado superioridad en SLE de injerto contra hospedero y recaída en un estudio aleatorizado reciente, por lo que se considera una alternativa aceptable.60
Para los pacientes con LLA Ph+, el mantenimiento postrasplante con inhibidores de tirosincinasa se considera el estándar.61 Para pacientes con LLA y EMR positiva postrasplante, el uso de terapias anticipadas con QT, infusión de linfocitos del donante han mostrado resultados prometedores. Para los pacientes en recaída postrasplante, una segunda terapia celular es el tratamiento que ofrece mayores probabilidades de supervivencia a largo plazo.
La terapia con CAR-T anti-CD19 es una alternativa para personas con LLA en recaída a dos o más líneas de tratamiento, incluido un SCT previo, basado en ensayos clínicos internacionales de fase II que han demostrado su eficacia y seguridad, inicialmente en pacientes pediátricos y posteriormente en adultos.30,62 Esta herramienta logra obtener altas tasas de remisión completa con EMR negativa y está relacionada con SLC, neurotoxicidad a corto plazo, aplasia de células B y citopenias a largo plazo.63
La secuenciación óptima de las terapias celulares aún es desconocida y todavía se debate la necesidad de un SCT alogénico posterior a la terapia con CAR-T.
Resumen y avances en el tratamiento
Los principales avances en la terapia para LLA son:
- Utilización de esquemas basados en Pediatría en pacientes AYA
- Combinación de quimio/inmunoterapia en primera línea
- Utilización de TKI de tercera generación con quimio/inmunoterapia en pacientes Ph+
- Uso de métodos más efectivos para medir EMR (como NGS
- CAR-T como consolidación
Sirva la Figura 1 como un resumen de tratamiento.
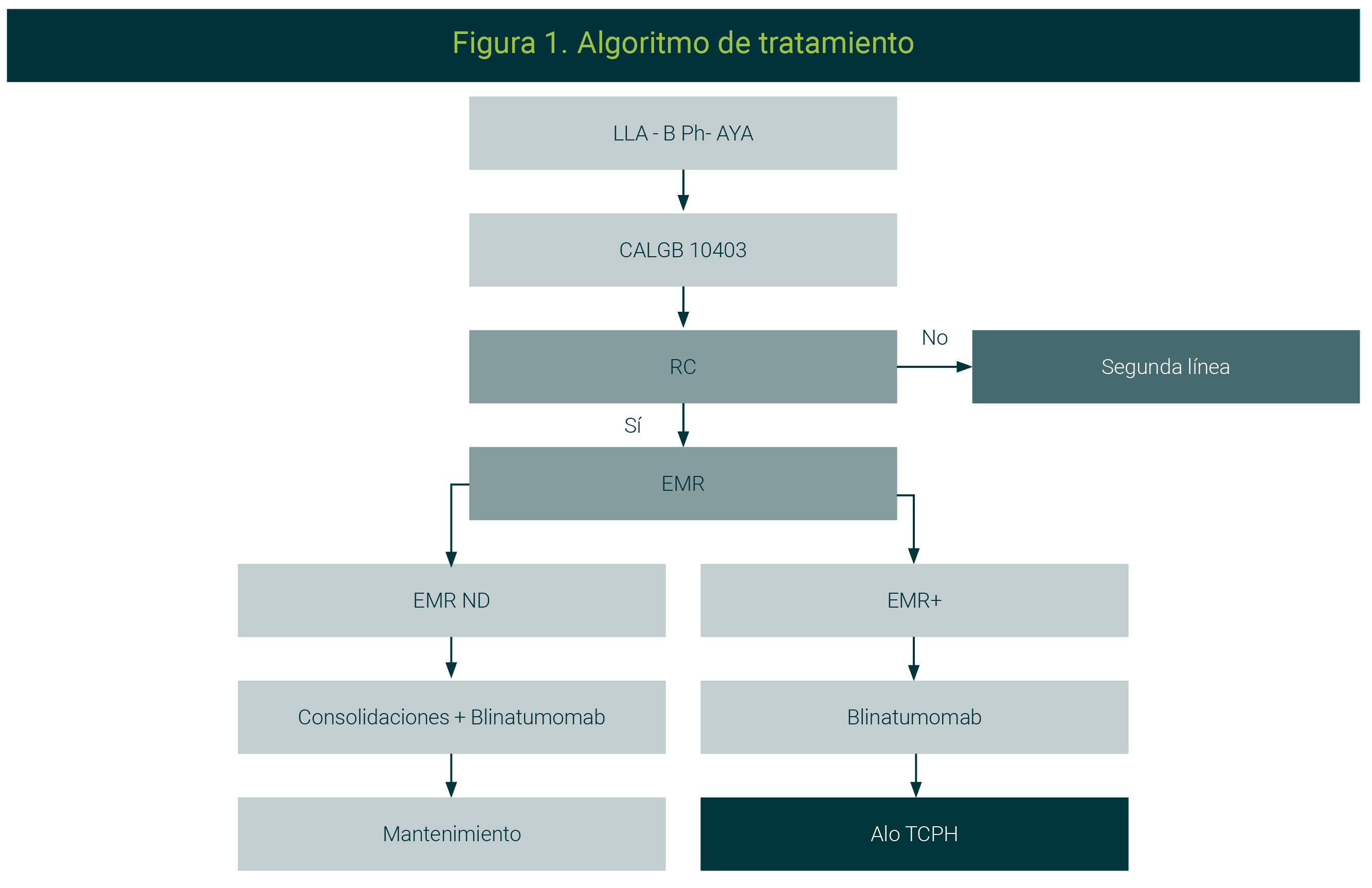
La leucemia linfoblástica aguda representa un reto en el tratamiento debido a la falta de acceso de medicamentos nuevos como inotuzumab ozogamicin, CAR-T y a la limitación en el acceso al SCT.
Se han realizado importantes avances en el tratamiento combinado de quimioterapia con inmunoterapia como primera línea en pacientes con EMR- y EMR + con LLA Ph- y se han obtenido buenos resultados.
La utilización de blinatumomab en combinación con ponatinib en primera línea para pacientes con LLA Ph+ representa una modalidad novedosa y prometedora sin quimioterapia; se contempla incluso no llevar a estos pacientes a SCT por los buenos resultados obtenidos con este esquema.
Para algunos subtipos de LLA que tienen mal pronóstico como KMT2A, hipodiploidía con mutación de TP53, Ph-like, se recomienda el SCT como consolidación del tratamiento.
Se requieren más ensayos clínicos para identificar las mejores combinaciones de quimioterapia, anticuerpos monoclonales, CAR-T y TKI con la finalidad de alcanzar la cura en estos pacientes.
Los autores declaran no tener ningún conflicto de interés.
| 1. | Malard F, Mohty M. Acute lymphoblastic leukaemia. Lancet. 2020;395(10230):1146-62. |
| 2. | Ramos Peñafiel C, Olarte Carrillo I, Ceron Maldonado R, Miranda Peralta E, Rozen Fuller E, Kassack Ipiña JJ, et al. Efecto de la metformina en la etapa de inducción en pacientes con leucemia aguda linfoblástica y su impacto clínico en la supervivencia. Rev Med Chil. 2018;146(7):846-53. |
| 3. | Siegel RL, Miller KD, Jemal A. Cancer statistics, 2020. CA Cancer J Clin. 2020;70(1):7-30. |
| 4. | Arber DA, Orazi A, Hasserjian R, Thiele J, Borowitz MJ, Le Beau MM, et al. The 2016 revision to the World Health Organization classification of myeloid neoplasms and acute leukemia. Blood. 2016;127(20):2391-2405. Blood. 2016;128(3):462-463. |
| 5. | Brown PA, Shah B, Advani A, Aoun P, Boyer MW, Burke PW, et al. Acute lymphoblastic leukemia, version 2.2021, NCCN Clinical Practice Guidelines in Oncology. J Natl Compr Canc Netw. 2021;19(9):1079-1109. |
| 6. | Peters JM, Ansari MQ. Multiparameter flow cytometry in the diagnosis and management of acute leukemia. Arch Pathol Lab Med. 2011;135(1):44-54. |
| 7. | Ruiz-Argüelles GJ, Ruiz-Delgado GJ (editores). Fundamentos de Hematología. Sexta edición. Ciudad de México: Editorial Médica Panamericana; 2021. 138 p. |
| 8. | Hoelzer D, Bassan R, Dombret H, Fielding A, Ribera JM, Buske C, et al. Acute lymphoblastic leukaemia in adult patients: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2016;27(suppl 5):v69-v82. |
| 9. | Abou Dalle I, Jabbour E, Short NJ. Evaluation and management of measurable residual disease in acute lymphoblastic leukemia. Ther Adv Hematol. 2020;11:2040620720910023. |
| 10. | Ladetto M, Brüggemann M, Monitillo L, Ferrero S, Pepin F, Drandi D, et al. Next-generation sequencing and real-time quantitative PCR for minimal residual disease detection in B-cell disorders. Leukemia. 2014;28(6):1299-307. |
| 11. | Rytting ME, Thomas DA, O'Brien SM, Ravandi-Kashani F, Jabbour EJ, Franklin AR, et al. Augmented Berlin-Frankfurt-Münster therapy in adolescents and young adults (AYAs) with acute lymphoblastic leukemia (ALL). Cancer. 2014;120(23):3660-8. |
| 12. | Stock W, Luger SM, Advani AS, Yin J, Harvey RC, Mullighan CG, et al. A pediatric regimen for older adolescents and young adults with acute lymphoblastic leukemia: Results of CALGB 10403. Blood. 2019;133(14):1548-59. Erratum in: Blood. 2019 Sep 26;134(13):1111. |
| 13. | Rangel-Patiño J, Yu Ling LT, Urbalejo-Ceniceros VI, Luna-Pérez MEM, Espinosa-Bautista KA, Amador LF, et al. Effectiveness and security of a modified CALGB 10403 in adolescents and young adults with acute lymphoblastic leukemia in low-and-middleincome countries: A multicentric experience in Central America. Blood. 2021; 138(Suppl 1):2284-86. |
| 14. | Kantarjian H, Thomas D, O'Brien S, Cortes J, Giles F, Jeha S, et al. Long-term follow-up results of hyperfractionated cyclophosphamide, vincristine, doxorubicin, and dexamethasone (Hyper-CVAD), a dose-intensive regimen, in adult acute lymphocytic leukemia. Cancer. 2004;101(12):2788-801. |
| 15. | Jabbour E, Short NJ, Jain N, Thompson PA, Kadia TM, Ferrajoli A, et al. Hyper-CVAD and sequential blinatumomab for newly diagnosed Philadelphia chromosome-negative B-cell acute lymphocytic leukaemia: A single-arm, single-centre, phase 2 trial. Lancet Haematol. 2022;9(12):e878-e885. |
| 16. | Litzow MR, Sun Z, Paietta E, Mattison RJ, Lazarus HM, Rowe JM, et al. ASH 2022. Abstr LBA-1 Consolidation therapy with blinatumomab improves overall survival in newly diagnosed adult patients with B-lineage acute lymphoblastic leukemia in measurable residual disease negative remission: Results from the ECOG-ACRIN E1910 randomized phase III National Cooperative Clinical Trials Network Trial. Available from URL: https://ashpublications.org/blood/article/140/Supplement%202/LBA-1/493429/Consolidation-Therapy-with-Blinatumomab-Improves |
| 17. | Gökbuget N, Dombret H, Bonifacio M, Reichle A, Graux C, Faul C, et al. Blinatumomab for minimal residual disease in adults with B-cell precursor acute lymphoblastic leukemia. Blood. 2018;131(14):1522-1531. Erratum in: Blood. 2019;133(24):2625. |
| 18. | Ribera JM, García O, Oriol A, Gil C, Montesinos P, Bernal T, et al. Feasibility and results of subtype-oriented protocols in older adults and fit elderly patients with acute lymphoblastic leukemia: Results of three prospective parallel trials from the PETHEMA group. Leuk Res. 2016;41:12-20. |
| 19. | O'Dwyer KM, Liesveld JL. Philadelphia chromosome negative B-cell acute lymphoblastic leukemia in older adults: Current treatment and novel therapies. Best Pract Res Clin Haematol. 2017;30(3):184-192. |
| 20. | Advani AS, Moseley A, O'Dwyer KM, Wood BL, Fang M, Wieduwilt MJ, et al. SWOG 1318: A Phase II trial of blinatumomab followed by POMP maintenance in older patients with newly diagnosed Philadelphia chromosome-negative B-cell acute lymphoblastic leukemia. J Clin Oncol. 2022;40(14):1574-82. |
| 21. | Ribera JM, García O, Chapchap EC, Gil C, González-Campos J, Barba P, et al. Treatment of frail older adults and elderly patients with Philadelphia chromosome-negative acute lymphoblastic leukemia: Results of a prospective trial with minimal chemotherapy. Clin Lymphoma Myeloma Leuk. 2020;20(8):e513-e522. |
| 22. | Sasaki K, Jabbour EJ, O'Brien SM, Ravandi F, Thomas DA, Garcia-Manero G, et al. Inotuzumab ozogamicin in combination with low-intensity chemotherapy (mini-hyperCVD) as frontline therapy for older patients with acute lymphoblastic leukemia (ALL): Interim result of a phase II clinical trial. Blood. 2016;128(22):588. |
| 23. | Jabbour EJ, Sasaki K, Ravandi F, Short NJ, Garcia-Manero G, Daver N, et al. Inotuzumab ozogamicin in combination with low-intensity chemotherapy (mini-HCVD) with or without blinatumomab versus standard intensive chemotherapy (HCVAD) as frontline therapy for older patients with Philadelphia chromosome-negative acute lymphoblastic leukemia: A propensity score analysis. Cancer. 2019;125(15):2579-86. |
| 24. | Specchia G, Pastore D, Carluccio P, Liso A, Mestice A, Rizzi R, et al. FLAG-IDA in the treatment of refractory/relapsed adult acute lymphoblastic leukemia. Ann Hematol. 2005;84(12):792-5. |
| 25. | Faderl S, Thomas DA, O'Brien S, Ravandi F, Garcia-Manero G, Borthakur G, et al. Augmented hyper-CVAD based on dose-intensified vincristine, dexamethasone, and asparaginase in adult acute lymphoblastic leukemia salvage therapy. Clin Lymphoma Myeloma Leuk. 2011;11(1):54-9. |
| 26. | Samra B, Jabbour E, Ravandi F, Kantarjian H, Short NJ. Evolving therapy of adult acute lymphoblastic leukemia: State-of-the-art treatment and future directions. J Hematol Oncol. 2020;13(1):70. |
| 27. | Kantarjian H, Stein A, Gökbuget N, Fielding AK, Schuh AC, Ribera JM, et al. Blinatumomab versus chemotherapy for advanced acute lymphoblastic leukemia. N Engl J Med. 2017;376(9):836-47. |
| 28. | Topp MS, Gökbuget N, Zugmaier G, Stein AS, Dombret H, Chen Y, et al. Long-term survival of patients with relapsed/refractory acute lymphoblastic leukemia treated with blinatumomab. Cancer. 2021;127(4):554-59. |
| 29. | Kantarjian HM, DeAngelo DJ, Stelljes M, Liedtke M, Stock W, Gökbuget N, et al. Inotuzumab ozogamicin versus standard of care in relapsed or refractory acute lymphoblastic leukemia: Final report and long-term survival follow-up from the randomized, phase 3 INO-VATE study. Cancer. 2019;125(14):2474-87. |
| 30. | Maude SL, Laetsch TW, Buechner J, Rives S, Boyer M, Bittencourt H, et al. Tisagenlecleucel in children and young adults with B-cell lymphoblastic leukemia. N Engl J Med. 2018;378(5):439-48. |
| 31. | Abou Dalle I, Jabbour E, Short NJ, Ravandi F. Treatment of Philadelphia chromosome-positive acute lymphoblastic leukemia. Curr Treat Options Oncol. 2019;20(1):4. |
| 32. | Gökbuget N, Hoelzer D. Treatment of adult acute lymphoblastic leukemia. Semin Hematol. 2009;46(1):64-75. |
| 33. | Thomas DA, Faderl S, Cortes J, O'Brien S, Giles FJ, Kornblau SM, et al. Treatment of Philadelphia chromosome-positive acute lymphocytic leukemia with hyper-CVAD and imatinib mesylate. Blood. 2004;103(12):4396-4407. |
| 34. | Tanguy-Schmidt A, Rousselot P, Chalandon Y, Cayuela JM, Hayette S, Vekemans MC, et al. Long-term follow-up of the imatinib GRAAPH-2003 study in newly diagnosed patients with de novo Philadelphia chromosome-positive acute lymphoblastic leukemia: A GRAALL study. Biol Blood Marrow Transplant. 2013;19(1):150-5. |
| 35. | Rea D, Legros L, Raffoux E, Thomas X, Turlure P, Maury S, et al. High-dose imatinib mesylate combined with vincristine and dexamethasone (DIV regimen) as induction therapy in patients with resistant Philadelphia-positive acute lymphoblastic leukemia and lymphoid blast crisis of chronic myeloid leukemia. Leukemia. 2006;20(3):400-3. |
| 36. | Vignetti M, Fazi P, Cimino G, Martinelli G, Di Raimondo F, Ferrara F, et al. Imatinib plus steroids induces complete remissions and prolonged survival in elderly Philadelphia chromosome-positive patients with acute lymphoblastic leukemia without additional chemotherapy: Results of the Gruppo Italiano Malattie Ematologiche dell'Adulto (GIMEMA) LAL0201-B protocol. Blood. 2007;109(9):3676-8. |
| 37. | Ottmann O, Dombret H, Martinelli G, Simonsson B, Guilhot F, Larson RA, et al. Dasatinib induces rapid hematologic and cytogenetic responses in adult patients with Philadelphia chromosome positive acute lymphoblastic leukemia with resistance or intolerance to imatinib: Interim results of a phase 2 study. Blood. 2007;110(7):2309-15. |
| 38. | Martinelli G, Papayannidis C, Piciocchi A, Robustelli V, Soverini S, Terragna C, et al. INCB84344-201: Ponatinib and steroids in frontline therapy for unfit patients with Ph+ acute lymphoblastic leukemia. Blood Adv. 2022;6(6):1742-53. |
| 39. | Jabbour E, Short NJ, Ravandi F, Huang X, Daver N, DiNardo CD, et al. Combination of hyper-CVAD with ponatinib as first-line therapy for patients with Philadelphia chromosome-positive acute lymphoblastic leukaemia: Long-term follow-up of a single-centre, phase 2 study. Lancet Haematol. 2018;5(12):e618-e627. |
| 40. | Short NJ, Kantarjian HM, Konopleva M, Jain N, Huang X, Ravandi F, et al. Combination of ponatinib and blinatumomab in Philadelphia chromosome-positive acute lymphoblastic leukemia: Early results from phase II study. J Clin Oncol. 2021;39(15):7001. |
| 41. | Mikhael NL, Seif H Gendi MA, Hassab H, Megahed EA. Evaluation of multiplexed biomarkers in assessment of CSF infiltration in pediatric acute lymphoblastic leukemia. Int J Hematol Oncol. 2019;8(3):IJH22. |
| 42. | van der Velden VH, de Launaij D, de Vries JF, de Haas V, Sonneveld E, Voerman JSA, et al. New cellular markers at diagnosis are associated with isolated central nervous system relapse in paediatric B-cell precursor acute lymphoblastic leukaemia. Br J Haematol. 2016;172(5):769-81. |
| 43. | Jeha S, Pei D, Raimondi SC, Onciu M, Campana D, Cheng C, et al. Increased risk for CNS relapse in pre-B cell leukemia with the t(1;19)/TCF3-PBX1. Leukemia. 2009;23(8):1406-9. |
| 44. | de Graaf MT, de Jongste AHC, Kraan J, Boonstra JG, Sillevis Smitt PA, Gratama JW. Flow cytometric characterization of cerebrospinal fluid cells. Cytometry B Clin Cytom. 2011;80(5):271-81. |
| 45. | Thastrup M, Duguid A, Mirian C, Schmiegelow K, Halsey C. Central nervous system involvement in childhood acute lymphoblastic leukemia: Challenges and solutions. Leukemia. 2022;36(12):2751-2768. |
| 46. | Sociedad Argentina de Hematología Guías de Diagnóstico y Tratamiento 2019. Disponible en URL: http://www.sah.org.ar/docs/2019/Guia_2019-completa.pdf |
| 47. | Basile P, Gordon PM, Jonart LM, Ebadi M, Johnson K, Makori J. Influence of the CNS niche on acute lymphoblastic leukemia biology. Blood. 2018;132(Suppl 1):4084. |
| 48. | Yeh TC, Liang DC, Hou JY, Jaing TH, Lin DT, Yang CP, et al. Treatment of childhood acute lymphoblastic leukemia with delayed first intrathecal therapy and omission of prophylactic cranial irradiation: Results of the TPOG-ALL-2002 study. Cancer. 2018;124(23):4538-47. |
| 49. | Matloub Y, Lindemulder S, Gaynon PS, Sather H, La M, Broxson E, et al. Intrathecal triple therapy decreases central nervous system relapse but fails to improve event-free survival when compared with intrathecal methotrexate: Results of the Children's Cancer Group (CCG) 1952 study for standard-risk acute lymphoblastic leukemia, reported by the Children's Oncology Group. Blood. 2006;108(4):1165-73. |
| 50. | Salzer WL, Burke MJ, Devidas M, Dai Y, Hardy KK, Kairalla JA, et al. Impact of intrathecal triple therapy versus intrathecal methotrexate on disease-free survival for high-risk B-lymphoblastic leukemia: Children's Oncology Group Study AALL1131. J Clin Oncol. 2020;38(23):2628-38. |
| 51. | Dutch Childhood Oncology Group, te Loo DMWM, Kamps WA, van der Does-van den Berg A, van Wering ER, de Graaf SSN. Prognostic significance of blasts in the cerebrospinal fluid without pleiocytosis or a traumatic lumbar puncture in children with acute lymphoblastic leukemia: Experience of the Dutch Childhood Oncology Group. J Clin Oncol. 2006;24(15):2332-6. |
| 52. | Peters C, Dalle JH, Locatelli F, Poetschger U, Sedlacek P, Buechner J, et al. Total body irradiation or chemotherapy conditioning in childhood ALL: A multinational, randomized, noninferiority phase III study. J Clin Oncol. 2021;39(4):295-307. |
| 53. | Stelljes M, Marks DI. Acute lymphoblastic leukemia in adults. In: Carreras E, Dufour C, Mohty M, Kröger N, editors. The EBMT Handbook: Hematopoietic Stem Cell Transplantation and Cellular Therapies [Internet]. 7th ed. Cham (CH): Springer; 2019. Chapter 71. PMID: 32091765. |
| 54. | Gabelli M, Zecca M, Messina C, Carraro E, Buldini B, Rovelli AM, et al. Hematopoietic stem cell transplantation for isolated extramedullary relapse of acute lymphoblastic leukemia in children. Bone Marrow Transplant. 2019;54(2):275-283. |
| 55. | DeFilipp Z, Advani AS, Bachanova V, Cassaday RD, Deangelo DJ, Kebriaei P, et al. Hematopoietic cell transplantation in the treatment of adult acute lymphoblastic leukemia: Updated 2019 evidence-based review from the American Society for Transplantation and Cellular Therapy. Biol Blood Marrow Transplant. 2019;25(11):2113-23. |
| 56. | Kanate AS, Majhail NS, Savani BN, Bredeson C, Champlin RE, Crawford S, et al. ndications for hematopoietic cell transplantation and immune effector cell therapy: Guidelines from the American Society for Transplantation and Cellular Therapy. Biol Blood Marrow Transplant. 2020;26(7):1247-56. |
| 57. | Goldstone AH, Richards SM, Lazarus HM, Tallman MS, Buck G, Fielding AK, et al. In adults with standard-risk acute lymphoblastic leukemia, the greatest benefit is achieved from a matched sibling allogeneic transplantation in first complete remission, and an autologous transplantation is less effective than conventional consolidation/maintenance chemotherapy in all patients: Final results of the International ALL Trial (MRC UKALL XII/ECOG E2993). Blood. 2008;111(4):1827-33. |
| 58. | Marks DI, Forman SJ, Blume KG, Pérez WS, Weisdorf DJ, Keating A, et al. A comparison of cyclophosphamide and total body irradiation with etoposide and total body irradiation as conditioning regimens for patients undergoing sibling allografting for acute lymphoblastic leukemia in first or second complete remission. Biol Blood Marrow Transplant. 2006;12(4):438-53. |
| 59. | Marks DI, Woo KA, Zhong X, Appelbaum FR, Bachanova V, Barker JN, et al. Unrelated umbilical cord blood transplant for adult acute lymphoblastic leukemia in first and second complete remission: A comparison with allografts from adult unrelated donors. Haematologica. 2014;99(2):322-8. |
| 60. | Holtan SG, Hamadani M, Wu J, AL Malki MM, Runaas L, Elmariah H, et al. Post-transplant cyclophosphamide, tacrolimus and mycophenolate mophetil as the new standard for graft-versus-host disease (GVHD) prophylaxis in reduced intensity conditioning: Results from phase III BMT CTN 1703. Blood. 2022;140(Suppl 2):LBA-4. |
| 61. | Warraich Z, Tenneti P, Thai T, Hubben A, Amin H, McBride A, et al. Relapse prevention with tyrosine kinase inhibitors after allogeneic transplantation for Philadelphia chromosome-positive acute lymphoblast leukemia: A systematic review. Biol Blood Marrow Transplant. 2020;26(3):e55-e64. |
| 62. | Shah BD, Ghobadi A, Oluwole O, Logan AC, Boissel N, Cassaday RD, et al. KTE-X19 for relapsed or refractory adult B-cell acute lymphoblastic leukemia: Phase 2 results of the single-arm, open-label, multicentre ZUMA-3 study. Lancet 2021;398(10299):491-502. |
| 63. | Jacoby E, Gökbuget N, Nagler A. Adult acute lymphoblastic leukemia. 2022 Feb 7. In: Kröger N, Gribben J, Chabannon C, et al., editors. The EBMT/EHA CAR-T Cell Handbook [Internet]. Cham (CH): Springer; 2022. Chapter 11. Available from URL: https://www.ncbi.nlm.nih.gov/books/NBK584135. |
All Rights Reserved® 2019
Latin American Journal of Clinical Sciences and Medical Technology,Publicación contínua • Editor responsable: Gilberto Castañeda Hernández. • Reserva de Derechos al Uso Exclusivo: 04-2019-062013242000-203; ISSN: 2683-2291; ambos otorgados por el Instituto Nacional del Derecho de Autor. • Responsable de la última actualización de este número, Web Master Hunahpú Velázquez Martínez,
Calle Profesor Miguel Serrano #8, Col. Del Valle, Alcaldía Benito Juárez, CP 03100, Ciudad de México, México. Número telefónico: 55 5405 1396 • Fecha de última modificación, 28 de agosto de 2024.
All Rights Reserved® 2019
Publicación contínua • Editor responsable: Gilberto Castañeda Hernández. • Reserva de Derechos al Uso Exclusivo: 04-2019-062013242000-203; ISSN: 2683-2291; ambos otorgados por el Instituto Nacional del Derecho de Autor. • Responsable de la última actualización de este número, Web Master Hunahpú Velázquez Martínez,
Calle Profesor Miguel Serrano #8, Col. Del Valle, Alcaldía Benito Juárez, CP 03100, Ciudad de México, México. Número telefónico: 55 5405 1396 • Fecha de última modificación, 28 de agosto de 2024.