| ** | Latin American Journal of Clinical Sciences and Medical Technology is an open access magazine. To read all published articles and materials you just need to register Registration is free of charge. Register now If you already have registered please Log In | ** |
aUnidad Funcional de Tumores Digestivos, Instituto Nacional de Cancerología México, Ciudad de México, México.
Autor para correspondencia: , . Números telefónicos: ; e-mail: draonco.diaz@gmail.com
Lat Am J Clin Sci Med Technol. 2023 Apr;5:115-124.
Recibido: 23 de febrero, 2023
Aceptado: 11 de marzo, 2023
Publicado: 03 de abril, 2023
Vistas: 23065
Descargas: 173
El cáncer gástrico ocupa el quinto lugar en incidencia en el mundo, y en México es la sexta neoplasia maligna más frecuente. Los factores de riesgo asociados con cáncer gástrico son edad (> 65 años), sexo masculino, dieta alta en sal y nitratos, carnes ahumadas y procesadas, deficiencia de vitamina C, tabaquismo, consumo intenso de alcohol, infección por H. pylori y virus de Epstein-Barr. En países occidentales, el cáncer gástrico se asocia con obesidad y enfermedad por reflujo gastroesofágico, predominantemente proximal o en cardias. El cuadro clínico es inespecífico en etapas tempranas. La endoscopia permite la toma de biopsia para confirmación histopatológica. En los tumores confinados a la mucosa, el tratamiento vía endoscópica es la mejor opción por la alta tasa de resecabilidad, preservación del órgano y baja recurrencia. En la etapa localmente avanzada, el tratamiento quirúrgico es la mejor alternativa para el control oncológico locorregional. Asimismo, se ha demostrado el beneficio de la quimioterapia perioperatoria. Se recomienda el uso de quimioterapia adyuvante para los pacientes sin tratamiento previo, que fueron llevados de forma inicial a gastrectomía total. El cáncer gástrico avanzado irresecable o metastásico tiene mal pronóstico, aunque éste ha mejorado recientemente. La presente oncoguía incluye recomendaciones para el diagnóstico, etapificación y tratamiento, basadas en la experiencia del Instituto Nacional de Cancerología y en la evidencia publicada recientemente.
Gastric cancer ranks fifth in incidence worldwide, and Mexico is the sixth most frequent malignant neoplasm. Risk factors associated with gastric cancer are age (> 65 years), being male, a diet high in salt and nitrates, smoked and processed meats, vitamin C deficiency, smoking, heavy alcohol consumption, and infection by H. pylori and Bar Epstein virus. In Western countries, gastric cancer is associated with obesity and gastroesophageal reflux disease, predominantly proximal or in the cardia. The clinical picture is nonspecific in the early stages. Endoscopy allows biopsy for histopathological confirmation. Endoscopic treatment is the best option in tumors confined to the mucosa due to the high resectability rate, the organ´s appearance, and low recurrence. Surgical treatment is the best alternative for locoregional oncological control in the locally advanced stage. Likewise, the benefit of perioperative chemotherapy has been demonstrated. Adjuvant chemotherapy is recommended for patients without previous treatment and who initially underwent a total gastrectomy. Unresectable or metastatic advanced gastric cancer has a poor prognosis, although it has recently improved. This oncoguía included recommendations for diagnosis, staging, and treatment based on our Instituto Nacional de Cancerología´s experience and the most recently published evidence.
Estas guías son sugerencias y recomendaciones para el manejo de pacientes en condiciones ideales; no constituyen razonamientos costo-eficientes, ni determinantes para compra de medicamentos. Su objetivo es proporcionar una guía básica, basada tanto en la experiencia del Instituto Nacional de Cancerología (INCan), como en la evidencia de mayor peso publicada recientemente, para que los médicos tratantes dispongan de tal información en la toma de decisiones y beneficio de los pacientes con cáncer gástrico.
Epidemiología
El cáncer gástrico ocupa el quinto lugar en incidencia en el mundo, con casi un millón de casos nuevos; es también el cuarto lugar en mortalidad (alrededor de 769,000 muertes por año).1 En México, es la sexta neoplasia maligna más frecuente y ocupa el quinto lugar en mortalidad, con 8,804 casos nuevos y 6,735 muertes por año.2
Se han identificado distintos factores de riesgo asociados con cáncer gástrico3-10:
- Edad > 65 años y sexo masculino (con una relación 1:2)
- Dieta alta en sal y nitratos, carnes ahumadas y procesadas
- Deficiencia de vitamina C
- Tabaquismo y consumo intenso de alcohol (≥ 4 tragos día o ≥ 30g/d)
- Infección por H. pylori y virus de Epstein-Barr
- Obesidad, enfermedad por reflujo gastroesofágico (ERGE), anemia perniciosa, gastrectomía parcial, enfermedad de Ménétrier y antecedentes de linfoma MALT (mucosa-associated lymphoid tissue)
- Historia familiar de cáncer gástrico (10%) y síndromes hereditarios (2-5%) (Tabla 1)
| Tabla 1. Síndromes hereditarios asociados con cáncer gástricoSíndrome | |||
|---|---|---|---|
| Síndrome | Características | Riesgo | Recomendación de seguimiento |
| Síndrome de CGDH | AD Mutación de CDH1 (35 - 50%) o PALB2 | 56-80% | Panendoscopia previa a la gastrectomía; en pacientes que no deseen gastrectomía profiláctica, cada 6-12 meses |
| Síndrome de Lynch | AD Mutación en genes de reparación de ADN (MLH1, MSH2, MSH6 y PMS2) | 11-30% | La panendoscopia de tamizaje debe ser considerada en los pacientes con ascendencia asiática |
| Síndrome poliposo juvenil | AD Mutaciones en genes SMAD4 o BMPR1A | 9-50% | Panendoscopia a partir de la adolescencia y con repetición anual en presencia de pólipos o cada 2-3 años en caso de estudio normal |
| Síndrome de Peutz Jeghers | AD Mutaciones en gen STK11 | 29% | Panendoscopia en la adolescencia cada 2 a 3 años, dependiendo del número de pólipos |
| CGDH: cáncer gástrico difuso hereditario; AD: autosómico dominante.Tabla original de los autores | |||
Los factores de riesgo varían de acuerdo con el área demográfica. En Asia Oriental se relaciona con infección por H. pylori y factores dietéticos-ambientales, cuya localización es distal o en antro. En países occidentales, el cáncer gástrico se asocia con obesidad y ERGE, predominantemente proximal o en cardias.
Clasificación
- Histológica (clasificación de la Organización Mundial de la Salud [OMS]):
- Tubular
- Papilar
- Mucinoso
- Poco cohesivo (incluidas las células en anillo de sello)11
- Clínicopatológica de Luaren (para adenocarcinoma gástrico)12,13:
- Difuso. Indiferenciado y con discohesión celular. Asociado con síndromes hereditarios, jóvenes y mujeres; peor pronóstico
- Intestinal. Bien diferenciado, células organizadas de forma tubular o glandular. Más frecuente en áreas de riesgo alto. Relacionado con factores ambientales (H. pylori, tabaquismo, factores dietéticos y lesiones precursoras); mejor supervivencia
- Mixto o indeterminado
- Molecular (The Cancer Genome Atlas):14
- EBV (9%). Mutación PIK3CA, sobrexpresión de PD-L1/2 y JAK2, silenciación de CDKN2A
- MSI (22%). Silenciación de MLH1. Hipermutación de oncoproteína diana
- Estabilidad genómica (20%). Histología difusa, mutación en CDH1 y RHOA
- Inestabilidad cromosómica (50%). Sobrexpresión y amplificación de RTK
- Mutación TP53; aneuploidía; activación RTK-RAS
- Macroscópica de Borrman en cáncer gástrico avanzado:15
- Tipo I. Polipoide
- Tipo II. Ulcerado con bordes elevados
- Tipo III. Ulcerado infiltrante
- Tipo IV. Infiltración difusa
Tamizaje
En los países de baja prevalencia, la vigilancia se enfoca en la población de riesgo alto.9,10,16-19:
- Lesiones precursoras. En casos de metaplasia intestinal con factores de riesgo, gastritis atrófica avanzada y displasia gástrica, se recomienda vigilancia con rangos de seis meses a tres años
- Dar seguimiento más específico en pacientes con síndromes hereditarios
Cuadro clínico
- Inespecífico en etapas tempranas
- Pérdida de peso
- Dolor abdominal
- Dispepsia y/o plenitud postprandial
- Disfagia (tumores proximales)
- Vómito
- Sagrado de tracto digestivo (hematemesis y/o melena)
- Síndrome anémico
Pueden aparecer adenopatías palpables periumbilicales (ganglio de la hermana María José) y supraclavicular izquierdo (ganglio de Virchow). En etapas más avanzas, ascitis, ictericia y tumor abdominal palpable.20
Estudios de extensión5,9,21-23
Endoscopia
Es el estándar de oro porque permite la toma de biopsia para confirmación histopatológica, define la localización y extensión intragástrica, así como el grado de obstrucción.
Ultrasonido endoscópico
Estatificación de profundidad (T) y del estado ganglionar (N) con una exactitud diagnóstica de 54 a 86% y de 50 a 71.2%, respectivamente. Su principal indicación es para tumores tempranos (T1) que permitan decidir un tratamiento endoscópico (T1a) vs. quirúrgico (T1b-2).
Tomografía computarizada (TC)
La TC contrastada tiene una exactitud diagnóstica de 71-88% para evaluar T y 61-78% para N. Es un estudio que permitirá completar la estadificación y evaluar la extensión locorregional y a distancia. Se debe indicar la TC de tórax y abdomen completo a doble contraste (intravenoso y oral).
Tomografía por emisión de positrones (PET-CT)
Puede mejorar la detección ganglionar (sensibilidad de 49% y especificidad de 92%) y de enfermedad metastásica (sensibilidad de 56% y especificidad de 97%). Tiene baja sensibilidad para la histología difusa y la carcinomatosis peritoneal.
Laparoscopia diagnóstica con lavado peritoneal
Incremento entre 20 y 31% en diagnóstico de carcinomatosis que no es medible por TC; modifica el abordaje terapéutico hasta en 60%. Se recomienda realizar en tumores de histología difusa, T3-4 y con afección ganglionar que son los que tienen mayor riesgo de afectar el peritoneo.
Estatificación
La clasificación que más se usa en el INCan es la del TNM de la American Joint Committee on Cancer (AJCC, octava edición) que en su última edición ha mostrado cambios en la estadificación clínica (Tabla 2).24
| Tabla 2. Sistema de clasificación TNM clínico | |
|---|---|
T: tumor primario | |
| Tx | Tumor primario no puede ser evaluado |
| T0 | No hay evidencia de tumor primario |
| Tis | Carcinoma in situ: tumor intraepitelial sin invasión de la lámina propia, displasia de alto grado |
| T1 | Tumor invade la lámina propia, la muscular de la mucosa o la submucosa |
| T1a | Tumor invade la lámina propia o la muscular de la mucosa |
| T1b | Tumor invade la submucosa |
| T2 | Tumor invade la muscular propia |
| T3 | Tumor penetra el tejido conectivo subseroso, sin invasión del peritoneo visceral o estructuras adyacentes |
| T4 | Tumor invade la serosa (peritoneo visceral) o estructuras adyacentes |
| T4a | Tumor invade la serosa (peritoneo visceral) |
| T4b | Tumor invade estructuras/órganos adyacentes |
N: ganglios linfáticos regionales | |
| Nx | Ganglios linfáticos regionales no valorables |
| N (-) | Sin ganglios linfáticos regionales con metástasis |
| N (+) | Ganglios linfáticos regionales con metástasis |
M: metástasis a distancia | |
| M0 | No metástasis a distancia |
| M1 | Metástasis a distancia |
| Tomado de Amin MB, 2017.24 La tabla es de uso libre | |
Las estrategias de tratamiento dependen de la etapa clínica de la enfermedad (Figura 1).
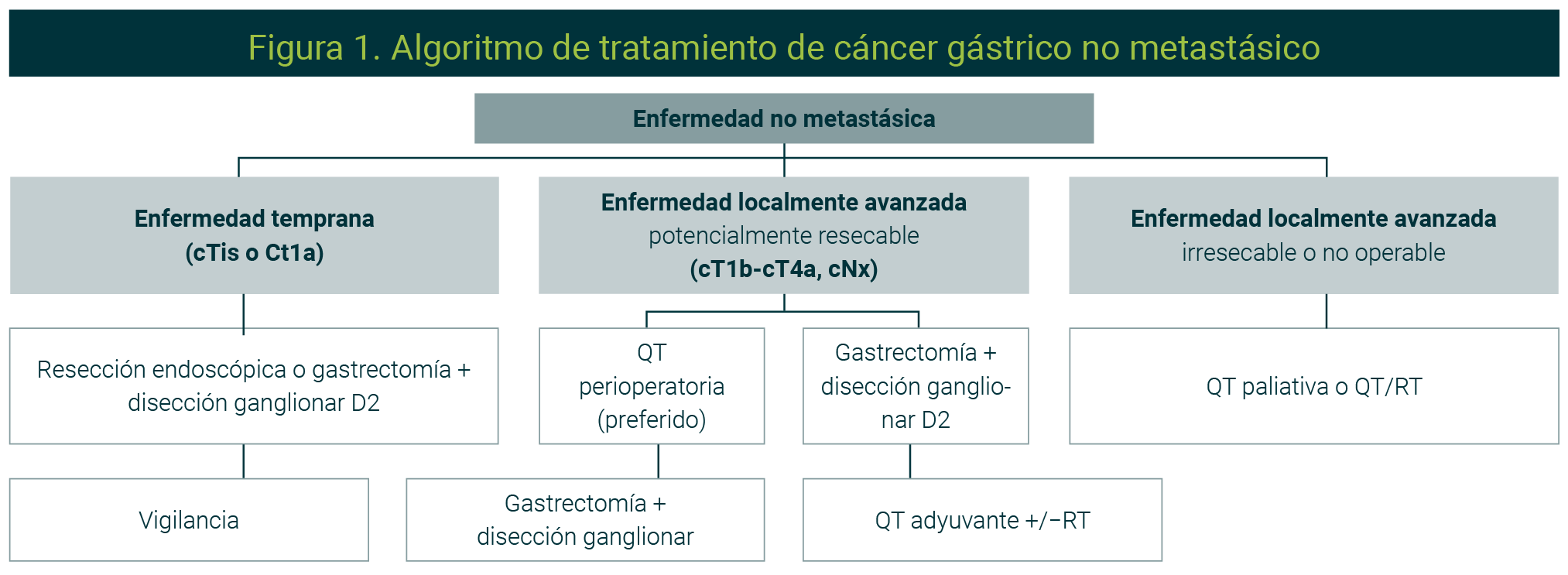
Tomado de Lordick F, 2022.5 La figura es de uso libre
Etapa temprana (T1-2, N0, M0)
Los tumores confinados a la mucosa (T1a) no tienen afección ganglionar y el tratamiento vía endoscópica es la mejor opción por la alta tasa de resecabilidad, preservación del órgano y baja recurrencia. Los pacientes candidatos son los que tienen tumores menores de 2 cm, bien diferenciados y no ulcerados, a los que se puede realizar resección de la mucosa o disección de la submucosa.
Los tumores con afección de la submucosa y muscular propia (T1b-2), sin afección ganglionar clínica, deberán recibir tratamiento quirúrgico para lograr mejor control oncológico y descartar la afección ganglionar, que puede estar presente hasta en un 15%. Según la localización del tumor, se pueden ofrecer resecciones preservadoras (gastrectomía proximal, gastrectomía preservadora de píloro) y la disección ganglionar puede limitarse a realizar una D1+ (niveles ganglionares 1 al 7 más 8, 9 y 11).
En esta etapa se recomienda el abordaje por mínima invasión. Hay varios estudios asiáticos, prospectivos, aleatorizados y multicéntricos que han demostrado que realizar una gastrectomía subtotal para tumores distales no es inferior (para resultados oncológicos a largo plazo) a la cirugía abierta porque mantiene los beneficios de este abordaje: menos sangrado, recuperación temprana, peristalsis y menor estancia hospitalaria. Ello será así siempre que se realice en centros de alto volumen y por cirujanos expertos. No obstante, realizar una gastrectomía total aún es debatible por el incremento en la morbilidad, secundaria a la reconstrucción que es más compleja.
Etapa localmente avanzada (T1b a 4, N+, M0)
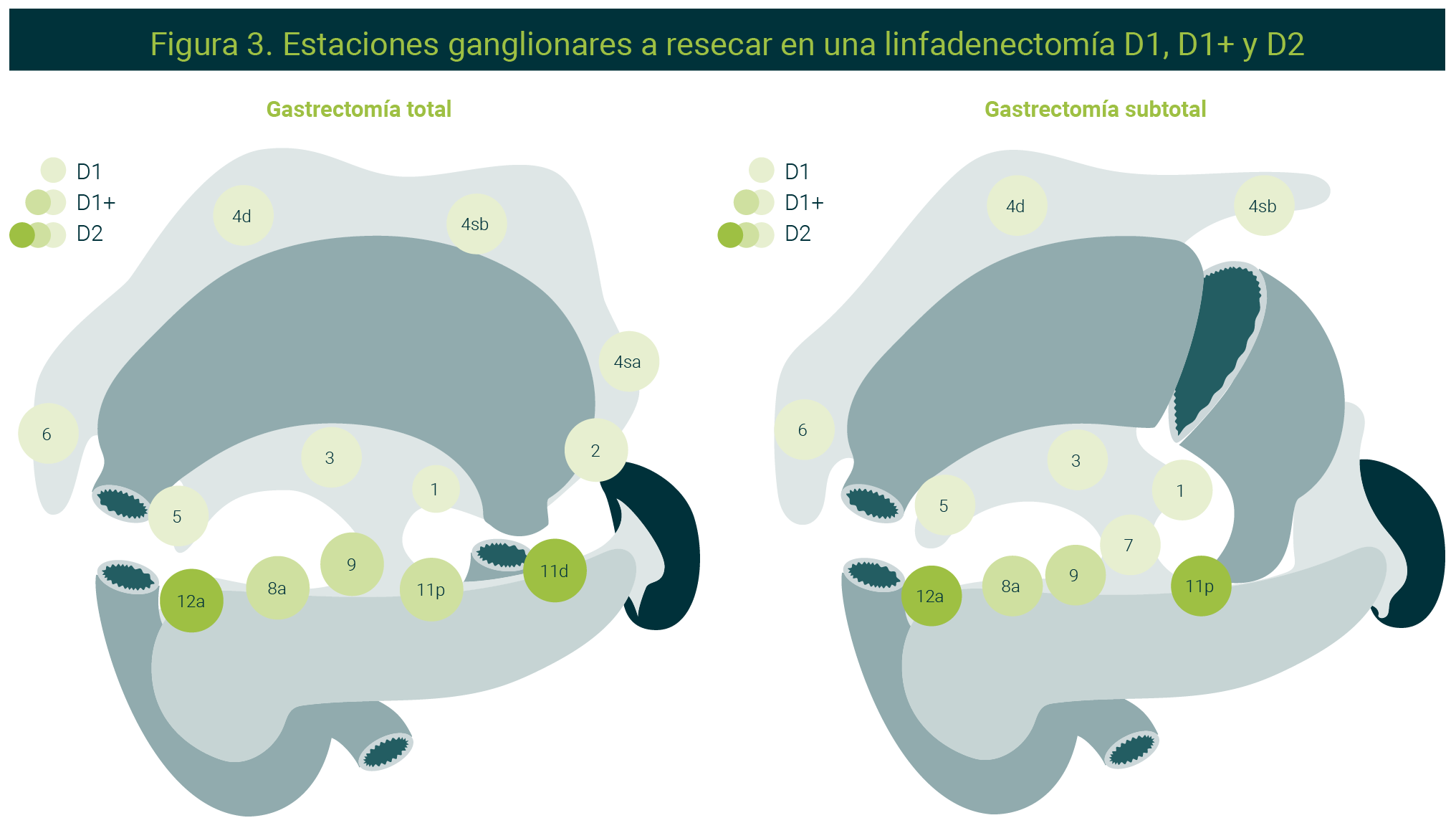
El tratamiento quirúrgico es la mejor opción para el control oncológico locorregional. La disección ganglionar D2 por estaciones ganglionares descrita desde 1961 por la escuela japonesa se considera piedra angular del tratamiento quirúrgico en Asia. En la Tabla 3 se muestran las estaciones ganglionares que ha descrito la escuela japonesa para el cáncer gástrico y en la Figura 2 se muestran las estaciones ganglionares que se deben disecar en una linfadenectomía D1, D1+ y D2, cuando realizamos una gastrectomía total y subtotal.17
| Tabla 3. Estaciones ganglionares en cáncer gástrico | |
|---|---|
| 1 | Ganglios paracardiales derechos |
| 2 | Ganglios paracardiales izquierdos |
| 3 | Ganglios de la curvatura menor |
| 4SA | Ganglios gástricos cortos |
| 4SB | Ganglios de vasos gastroepiploicos izquierdos |
| 4D | Ganglios de vasos gastroepiploicos derechos |
| 5 | Ganglios suprapilóricos |
| 6 | Ganglios infrapilóricos |
| 7 | Ganglios de arteria gástrica izquierda |
| 8ª | Ganglios de arteria hepática común antero - superior |
| 9 | Ganglios del tronco celíaco |
| 10 | Ganglios del hilio esplénico |
| 11 | Ganglios de arteria esplénica |
| 12 | Ganglios del ligamento hepatoduodenal |
| 13 | Ganglios cara posterior cabeza de páncreas |
| 14 | Ganglios de vasos mesentéricos superiores |
| 15 | Ganglios de arteria cólica media |
| 16 | Ganglios para - aórticos |
| Tomado de Japanese Gastric Cancer Association, 2021.17 La tabla es de uso libre | |
Sin embargo, en Europa el tema de la disección ganglionar generó controversia en los estudios prospectivos realizados en el decenio de los noventa, donde se mostraba una alta morbimortalidad sin beneficio oncológico en los pacientes llevados a la linfadenectomía D2. Sin embargo, después de revisar y eliminar las limitaciones de los estudios (muchos centros de bajo volumen y pancreatectomía distal con esplenectomía de rutina), en el estudio holandés con un seguimiento a 15 años, se reportó que la disección D2 disminuye la recurrencia locorregional y mortalidad específica contra la D1, siempre que se realice en centros con experiencia.25
En 2010, se realizó un estudio europeo prospectivo que comparó la disección D2 vs. D1, de acuerdo con los lineamientos japoneses y se observó que la morbilidad disminuyó a 17.9%, al igual que la mortalidad en 2.2%; también incrementó la cosecha ganglionar para D2 (D1 28.2 vs. 37.3 D2). Con un seguimiento a 8.8 años, la disección D2 prolongó la supervivencia y el período libre de enfermedad a 5 años.26 Con estos resultados, las guías europeas han adoptado la disección D2 como parte del tratamiento quirúrgico, pero se debe realizar en centros con experiencia.
La guía NCCN (National Comprehensive Cancer Network) menciona que la disección D2 se debe realizar en tumores localmente avanzados por cirujanos con experiencia y que se requiere mínimo 16 ganglios para estadificar.9 No obstante, el estudio de Woo et al. con 25,000 pacientes encontró que una cosecha ganglionar mínima de 29 ganglios, sí incrementa la supervivencia etapa por etapa.27
El estudio holandés CRITICS cuidó a detalle los principios quirúrgicos y en él se definieron dos términos nuevos para valorar la calidad de la disección ganglionar:
- Cumplimiento quirúrgico-patológico, que se refiere a disecar al menos 16 ganglios
- Cumplimiento quirúrgico, que es disecar ganglios por estaciones que incluya los niveles del 1 al 9 y 11 donde el concepto «no cumplimiento» se define como la ausencia de ganglios en las estaciones; y «contaminación» cuando se agregan ganglios de una o más estaciones a la estación disecada28
Desde 2017, en el INCan se realiza la disección D2 por estaciones ganglionares en tumores localmente avanzados. Para junio de 2020 ya se había operado a 71 pacientes con una morbilidad mayor (Clavien 3-4) de 11.2% y mortalidad a 30 días del 1.4%. La cosecha ganglionar media es de 60.9 (31-130) con un cumplimiento quirúrgico-patológico del 100% y cumplimiento quirúrgico del 50.7%, lo cual es similar a lo reportado por en el estudio CRITICS.
En cuanto a los márgenes quirúrgicos, se han adoptado las recomendaciones de la escuela japonesa, donde el margen proximal mínimo es de 3 cm para tumores con crecimiento expansivo (intestinal) y de 5 cm con crecimiento infiltrativo (difuso). Sin embargo, para tumores en fondo gástrico cercanos a la unión esofagogástrica, se recomienda un margen entre 2-3 cm esofágico y enviar a transoperatorio para corte congelado.
Respecto al margen distal, se recomienda entre 1-2 cm sobre el duodeno, tomando como límite máximo la arteria gastroduodenal. La gastrectomía subtotal se indicará cuando el tumor se localice en el tercio distal gástrico y se mantendrá un margen proximal entre 3 a 5 cm sobre la curvatura menor, sin que quede comprometida la unión esofagogástrica. La reconstrucción de elección será la «Y de Roux» porque es la que reporta el menor porcentaje de reflujo biliar.
Finalmente, el abordaje por mínima invasión aún genera controversia, por lo que se encuentran en desarrollo los estudios prospectivos. El estudio CLASS-01 para tumores distales, en centros de alto volumen, no fue inferior para morbimortalidad, y el seguimiento a 5 años reportó resultados oncológicos similares entre ambos grupos. No obstante, las limitaciones fueron que 30% tuvo etapa patológica temprana y en los que se encontraban en etapa III se observó tendencia no significativa a incrementar la recurrencia peritoneal en el grupo laparoscópico.29
El estudio coreano KLASS-02 —que fue muy riguroso para la inclusión de pacientes con tumores gástricos distales en centros de alto volumen (80 gastrectomías anuales) operados por cirujanos con experiencia (50 gastrectomías laparoscópicas)— reportó significancia estadística para disminuir la morbilidad en el grupo laparoscópico (16.6% vs. 24.1%, p=0.003), sin diferencias para mortalidad a 90 días. En el seguimiento a tres años no se reportó inferioridad en el grupo laparoscópico para supervivencia y período libre de enfermedad.30
En Occidente, el estudio LOGICA (realizado en Holanda) concluyó que la gastrectomía total y subtotal en etapa localmente avanzada es posible por mínima invasión, tiene resultados similares para morbimortalidad y oncológicos a corto plazo vs. cirugía abierta en centros de alto volumen con cirujanos experimentados y con tratamiento sistémico neoadyuvante.31
Enfermedad locorregional
Quimioterapia perioperatoria
Distintos estudios han mostrado el beneficio de la quimioterapia perioperatoria. Por ejemplo, el estudio fase III MAGIC comparó el tratamiento con quimioterapia perioperatoria con epirrubicina/5FU/cisplatino (ECF) contra únicamente cirugía. Los resultados mostraron una supervivencia a 5 años de 36 vs. 23%, a favor del grupo de quimioterapia perioperatoria.32 El estudio fase III FNCLCC mostró resultados similares con el esquema cisplatino/5FU (PF) perioperatorio vs. solo cirugía, con una supervivencia a 5 años de 38 vs. 24%.33
En 2018 se compraron dos distintos esquemas de quimioterapia perioperatoria con 5FU/ácido folínico/oxaliplatino/docetaxel (FLOT) vs. ECF. Se encontró que la supervivencia global (SG) había aumentado con el esquema FLOT, y que hubo mejores respuestas patológicas. Pese a ello, el triplete representa un aumento en la toxicidad, por lo que la selección de pacientes debe realizarse de acuerdo con el estado funcional y comorbilidades.34
Actualmente, la quimioterapia preoperatoria es el tratamiento de elección para pacientes ≥ T1bN0M0, donde previamente se sugiere realizar una laparoscopia diagnóstica +/- lavado peritoneal. Los esquemas de quimioterapia perioperatoria de elección incluyen triplete con FLOT (8 ciclos) en pacientes con buen estado funcional o duplete con fluoropirimidinas + platinos (PF 6 ciclos o 5FU/AF/oxaliplatino, 8 ciclos).
Quimioterapia adyuvante
De acuerdo con los estudios fase III ACTS y CLASSIC, la quimioterapia adyuvante presenta una SG a 3 años de 80% vs. 70% y una supervivencia libre de enfermedad a 3 años de 72 vs. 59%, al compararse con cirugía sola.35,36 Por lo tanto, se recomienda el uso de quimioterapia adyuvante para los pacientes sin tratamiento previo (quimioterapia y/o radioterapia), que fueron llevados de forma inicial a gastrectomía total con disección ganglionar D2, con reporte histopatológico ≥ pT2N0M0.
Quimiorradioterpia
El uso de la quimiorradioterpia (QT/RT) en el contexto de adyuvancia es cuestionable. De forma inicial, el estudio de McDonalds mostró beneficio al agregar la QT/RT postoperatoria, pero en este estudio únicamente el 10% de los pacientes fue llevado a disección ganglionar D2.37 Posteriormente, los estudios CRITICS, ARTIST y ARTIST II compararon el uso de QT/RT vs. solo QT en el contexto adyuvante, pero no encontraron beneficio adicional con QT/RT en los pacientes con pT3-T4N0 o N+ llevados a disección ganglionar D2.38-40
La QT/RT debe considerarse para los pacientes llevados a cirugía con disección ganglionar inferior a una D2 y en caso de márgenes positivos. QT/RT también es una opción en pacientes con enfermedad irresecable.
Enfermedad avanzada
El cáncer gástrico avanzado irresecable o metastásico tiene mal pronóstico, mismo que históricamente ha mejorado y mostrado medianas de supervivencia de 11 meses, en comparación con los mejores cuidados de soporte. Los tratamientos sistémicos tienen el objetivo de controlar y paliar los síntomas, aumentar la supervivencia y mejorar la calidad de vida.
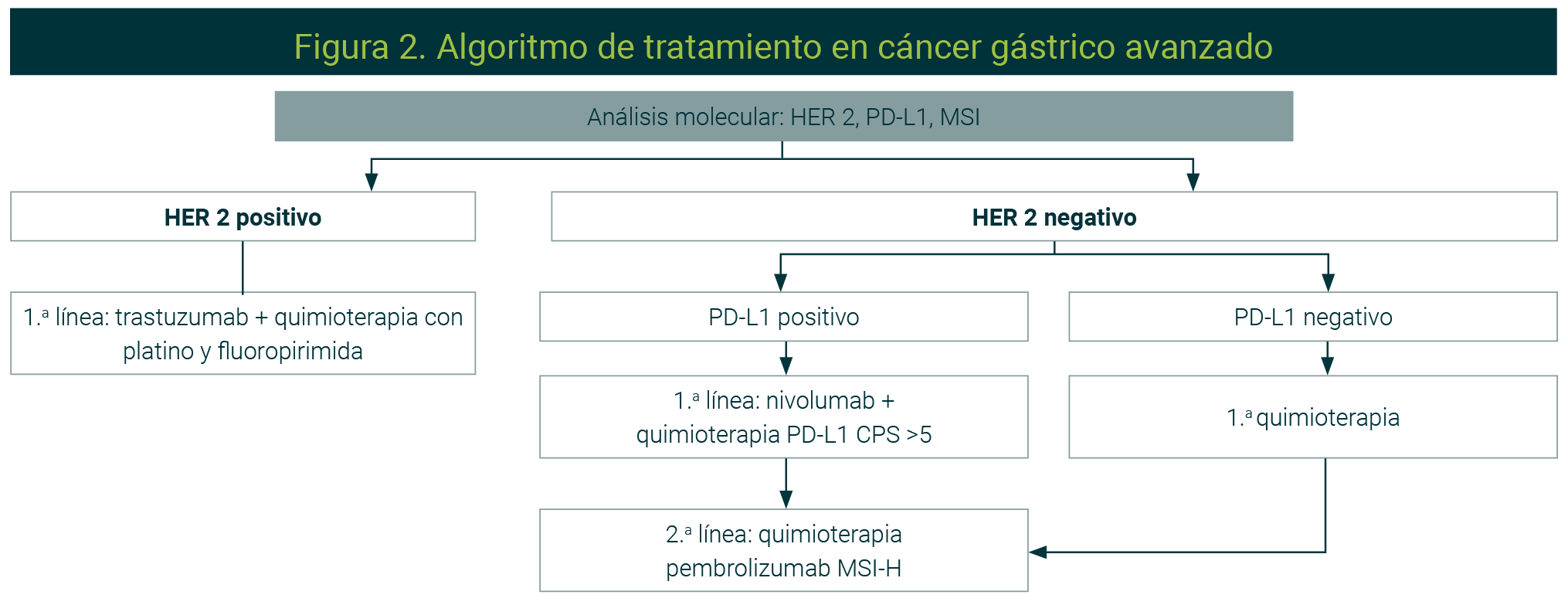
En los enfermos con cáncer gástrico avanzado (Figura 3) se requiere valorar el nivel de actividad funcional determinado por el ECOG; así como las comorbilidades de los pacientes con la finalidad de considerar si son candidatos a un tratamiento sistémico. Igualmente, se debe determinar la sobrexpresión del receptor HER2, la expresión de PDL1 (ligandos L1 de muerte celular programada) y las enzimas reparadoras de bases de ADN (inestabilidad microsatelital), ya que las terapias dirigidas a estos biomarcadores han mejorado la tasa de respuesta y prolongado la supervivencia.4,5
La figura es de uso libre
La quimioterapia estándar de primera línea se basa en dobletes de sales de platino y fluoropirimidinas. El oxaliplatino y el cisplatino son los fármacos más utilizados; mientras que las fluoropirimidinas pueden administrarse como infusión (5-FU) o como tratamiento oral (capecitabina).
Se demostró que el cisplatino y el oxaliplatino tienen efectividad similar. En ensayos aleatorizados, los pacientes mayores de 65 años con oxaliplatino obtuvieron un perfil de seguridad superior, lo cual puede estar asociado con una supervivencia más prolongada.41
La capecitabina oral es al menos tan efectiva como la infusión de 5FU. Se puede preferir el 5-FU en infusión cuando la disfagia es un problema.
Aunque el uso de tripletes ha proporcionado tasas de respuesta objetiva mayor, se recomienda menos debido a la toxicidad secundaria y porque los desenlaces en supervivencia han sido limítrofes; en pacientes con enfermedad oligometastásica (probables candidatos a control local posterior) pueden ser una opción.42
La combinación de irinotecán y fluoropirimidina intravenosa ha sido evaluada en comparación con el cisplatino/5FU o esquemas de epirrubicina/cisplatino/capecitabina, y ha demostrado mejoría en el tiempo de falla a tratamiento (HR 0.77, IC 95% 0.63-0.93, p=0.008). Esta combinación puede ser considerada una alternativa en pacientes que no son candidatos a oxaliplatino.43
Segunda línea de tratamiento
Algunos tratamientos son paclitaxel semanal (80 mg/SC D1, D8, D15 cada 28 días), docetaxel o irinotecán porque resultan en una supervivencia libre de progresión (SLP) de 2 meses.44 La combinación paclitaxel con ramucirumab presentó una SLP de 4.4 frente a 2.9 meses y una SG de 9.6 meses frente a 7.4 meses (p = 0.017).45 Así, si el paciente puede tolerar quimioterapia se prefiere ramucirumab con quimioterapia en segunda línea.
Terapia anti-HER2
La amplificación del oncogén HER2, que conlleva la sobrexpresión del receptor HER2 (ERBB2), está asociada con proliferación de células tumorales, apoptosis, migración, adhesión y diferenciación. La sobrexpresión de HER2 en el cáncer gástrico o de la unión gastroesofágica varía dependiendo de los diferentes estudios, su frecuencia oscila entre 4.4% y 25.4% (media de 17.9%).
Trastuzumab es un anticuerpo monoclonal contra el receptor HER2. El estudio ToGA comparó quimioterapia y trastuzumab con quimioterapia sola en pacientes con cáncer gástrico o de la unión gastroesofágica avanzado HER2 positivo. La supervivencia media fue de 16 meses con trastuzumab y quimioterapia, comparada con 11.1 meses en pacientes con quimioterapia sola (HR 0.74, 95% CI 0.60-0.91, p=0.0046).46
Inmunoterapia: inhibidores de puntos de control inmunitarios
La aprobación de pembrolizumab para tumores sólidos metastásicos, con deficiencia del sistema de reparación de bases de ADN (dMMR, deficient mismatch repair enzymes) o inestabilidad alta de microsatélites se basa en la aprobación agnóstica con indicación en pacientes que han progresado a una primera línea de tratamiento y que presenten inestabilidad de microsatélites.8,9
Pembrolizumab fue aprobado por la Food and Drug Administration (FDA) como monoterapia para el tratamiento del cáncer gástrico metastásico o de la unión gastroesofágica, tratados previamente, de acuerdo con el estudio KEYNOTE-059.47
La tasa de respuesta a pembrolizumab fue de 11.6%, con respuesta completa en 2.3%. En los pacientes con PD-L1 CPS ≥1, la tasa de respuesta fue de 22.7%; mientras que en los pacientes con PD-L1 negativo, la tasa de respuesta fue de sólo 8.6%. En los pacientes con MSI-H, la tasa de respuesta fue de 57%.47
El estudio CheckMate-649 compara nivolumab + ipilimumab vs. nivolumab + quimioterapia vs. quimioterapia sola, en primera línea.48
Los resultados positivos en el grupo de tratamiento con nivolumab + quimioterapia en primera línea indicaron que la supervivencia general y SLP fueron más largas que con quimioterapia sola, en pacientes con CPS>5. La supervivencia media con nivolumab y quimioterapia fue 14.4 vs. 11.1 meses con quimioterapia sola. La SLP fue de 7.7 meses con nivolumab + quimioterapia vs. 6.1 meses con quimioterapia sola.48
Apoyo nutricional
La atención y cuidados nutricionales son fundamentales para el bienestar de los pacientes con cáncer gástrico. Un ensayo aleatorizado fase III, reciente, demostró aumento en la supervivencia de tres meses para los pacientes que recibieron atención de apoyo multidisciplinario, en comparación con los que recibieron quimioterapia estándar.49
La atención de apoyo incluye tanto la paliación de los síntomas como el apoyo nutricional. La pérdida de peso es multifactorial y puede deberse a obstrucción del tracto gastrointestinal, anorexia, malabsorción o hipermetabolismo. En los estudios clínicos, la pérdida de peso mayor a 10% antes del tratamiento y 3-5% durante el primer ciclo de tratamiento, se asocia con una SG reducida.50
El cáncer gástrico es el quinto cáncer más común y la tercera causa más frecuente de muerte por cáncer a nivel mundial. Los factores de riesgo para la afección incluyen la infección por Helicobacter pylori, edad, alto consumo de sal y las dietas bajas en vegetales.
El cáncer gástrico se diagnostica histológicamente después de una biopsia endoscópica y se estadifica mediante TC, ecografía endoscópica, PET y laparoscopia. Es una enfermedad molecular y fenotípicamente muy heterogénea.
El tratamiento principal para el cáncer gástrico temprano es la resección endoscópica. El cáncer gástrico que no se puede operar tempranamente se trata con cirugía, que debe incluir linfadenectomía D2 (incluidas las estaciones de ganglios linfáticos en el mesenterio perigástrico y a lo largo de las ramas arteriales celíacas).
La quimioterapia perioperatoria o adyuvante prolonga la supervivencia en pacientes con cánceres en estadio 1B o superior. El cáncer gástrico avanzado se trata con líneas secuenciales de quimioterapia; en primera línea con un doblete de platino y fluoropirimidina (la supervivencia media es inferior a 1 año).
Las terapias dirigidas autorizadas para tratar el cáncer gástrico incluyen trastuzumab (primera línea para pacientes con HER2 positivo), taxanos con antiangiogénico de segunda línea y nivolumab recientemente autorizados en tumores con CPS > 5 o pembrolizumab (anti-PD-1 de tercera línea con MSI-H).
Los autores declaran no tener conflicto de interés.
| 1. | Sung H, Ferlay J, Siegel RL, Laversanne M, Soerjomataram I, Jemal A, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2021;71(3):209-49. |
| 2. | World Health Organization. International Agency for Research on Cancer. Global Cancer Observatory: Cancer Today. Available from URL: https://gco.iarc.fr/today/home |
| 3. | Lott PC, Carvajal-Carmona LG. Resolving gastric cancer aetiology: An update in genetic predisposition. Lancet Gastroenterol Hepatol. 2018;3(12):874-83. |
| 4. | Smyth EC, Nilsson M, Grabsch HI, van Grieken NC, Lordick F. Gastric cancer. Lancet. 2020;396(10251):635-48. |
| 5. | Lordick F, Carneiro F, Cascinu S, Fleitas T, Haustermans K, Piessen G, et al. Gastric cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol. 2022;33(10):1005-20. |
| 6. | Kim J, Cho YA, Choi WJ, Jeong SH. Gene-diet interactions in gastric cancer risk: A systematic review. World J Gastroenterol. 2014;20(28):9600-10. |
| 7. | Machlowska J, Baj J, Sitarz M, Maciejewski R, Sitarz R. Gastric cancer: Epidemiology, risk factors, classification, genomic characteristics and treatment strategies. Int J Mol Sci. 2020;21(11):4012. |
| 8. | Ajani JA, Lee J, Sano T, Janjigian YY, Fan D, Song S. Gastric adenocarcinoma. Nat Rev Dis Primers. 2017;3:17036. |
| 9. | National Comprehensive Cancer Network. Gastric Cancer (version 2.2022). Available from URL: https://jnccn.org/view/journals/jnccn/20/2/article-p167.xml |
| 10. | Kim W, Kidambi T, Lin J, Idos G. Genetic syndromes associated with gastric cancer. Gastrointest Endosc Clin N Am. 2022;32(1):147-162. |
| 11. | Kushima R. The updated WHO classification of digestive system tumours-gastric adenocarcinoma and dysplasia. Pathologe. 2022;43(1):8-15. |
| 12. | Chen YC, Fang WL, Wang RF, Liu CA, Yang MH, Lo SS, et al. Clinicopathological variation of Lauren Classification in gastric cancer. Pathol Oncol Res. 2016;22(1):197-202. |
| 13. | Lauren P. The two histological main types of gastric carcinoma: Diffuse and so-called intestinal-type carcinoma. An attempt at a histo-clinical classification. Acta Pathol Microbiol Scand. 1965;64:31-49. |
| 14. | Cancer Genome Atlas Research Network. Comprehensive molecular characterization of gastric adenocarcinoma. Nature. 2014;513(7517):202-9. |
| 15. | Li C, Oh SJ, Kim S, Hyung WJ, Yan M, Zhu ZG, et al. Macroscopic Borrmann type as a simple prognostic indicator in patients with advanced gastric cancer. Oncology. 2009;77(3-4):197-204. |
| 16. | Kim B, Cho SJ. Endoscopic screening and surveillance for gastric cancer. Gastrointest Endosc Clin N Am. 2021 Jul;31(3):489-501. |
| 17. | Japanese Gastric Cancer Association. Japanese gastric cancer treatment guidelines 2018 (5th edition). Gastric Cancer. 2021;24(1):1-21. |
| 18. | Gupta S, Li D, El Serag HB, Davitkov P, Altayar O, Sultan S, et al. AGA Clinical Practice Guidelines on management of gastric intestinal metaplasia. Gastroenterology. 2020;158(3):693-702. |
| 19. | Pimentel-Nunes P, Libânio D, Marcos-Pinto R, Areia M, Leja M, Esposito G, et al. Management of epithelial precancerous conditions and lesions in the stomach (MAPS II): European Society of Gastrointestinal Endoscopy (ESGE), European Helicobacter and Microbiota Study Group (EHMSG), European Society of Pathology (ESP), and Sociedade Portuguesa de Endoscopia Digestiva (SPED) guideline update 2019. Endoscopy. 2019;51(4):365-88. |
| 20. | Vitiello GA, Hani L, Wang A, Porembka MR, Alterio R, Ju M, et al. Clinical presentation patterns and survival outcomes of Hispanic patients with gastric cancer. J Surg Res. 2021;268:606-15. |
| 21. | Fairweather M, Jajoo K, Sainani N, Bertagnolli MM, Wang J. Accuracy of EUS and CT imaging in preoperative gastric cancer staging. J Surg Oncol. 2015;111(8):1016-20. |
| 22. | Yoon H, Lee DH. New approaches to gastric cancer staging: Beyond endoscopic ultrasound, computed tomography and positron emission tomography. World J Gastroenterol. 2014;20(38):13783-90. |
| 23. | Sarela AI, Lefkowitz R, Brennan MF, Karpeh MS. Selection of patients with gastric adenocarcinoma for laparoscopic staging. Am J Surg. 2006;191(1):134-8. |
| 24. | Amin MB, Edge SB, Greene FL, Byrd DR, Brookland RK, Washington MK, et al (editors). AJCC Cancer Staging Manual. 8th edition. American College of Surgeons, Springer Cham; 2017. |
| 25. | Songun I, Putter H, Kranenbarg EMK, Sasako M, van de Velde CJH. Surgical treatment of gastric cancer: 15-year follow-up results of the randomised nationwide Dutch D1D2 trial. Lancet Oncol. 2010;11(5):439-49. |
| 26. | Degiuli M, Sasako M, Ponti A, Vendrame A, Tomatis M, Mazza C, et al. Randomized clinical trial comparing survival after D1 or D2 gastrectomy for gastric cancer. Br J Surg. 2014;101(2):23-31. |
| 27. | Woo Y, Goldner B, Ituarte P, Lee B, Melstrom L, Son T, et al. Lymphadenectomy with optimum of 29 lymph nodes retrieved associated with improved survival in advanced gastric cancer: A 25,000-patient international database study. J Am Coll Surg. 2017;224(4):546-555. |
| 28. | Claassen YHM, de Steur WO, Hartgrink HH, Dikken JL, van Sandick JW, van Grieken NCT, et al. Surgicopathological quality control and protocol adherence to lymphadenectomy in the CRITICS gastric cancer trial. Ann Surg. 2018;268(6):1008-13. |
| 29. | Huang C, Liu H, Hu Y, Sun Y, Su X, Cao H, et al. Laparoscopic vs open distal gastrectomy for locally advanced gastric cancer: Five-year outcomes from the CLASS-01 randomized clinical trial. JAMA Surg. 2022;157(1):9-17. |
| 30. | Hyung WJ, Yang HK, Park YK, Lee HJ, An JY, Kim W, et al. Long-term outcomes of laparoscopic distal gastrectomy for locally advanced gastric cancer: The KLASS-02-RCT randomized clinical trial. J Clin Oncol. 2020;38(28):3304-3313. |
| 31. | van der Veen A, Brenkman HJF, Seesing MFJ, Haverkamp L, Luyer MDP, Nieuwenhuijzen GAP, et al. Laparoscopic versus open gastrectomy for gastric cancer (LOGICA): A multicenter randomized clinical trial. J Clin Oncol. 2021;39(9):978-89. |
| 32. | Cunningham D, Allum WH, Stenning SP, Thompson JN, Van de Velde CJH, Nicolson M, et al. Perioperative chemotherapy versus surgery alone for resectable gastroesophageal cancer. N Engl J Med. 2006;355(1):11-20. |
| 33. | Ychou M, Boige V, Pignon JP, Conroy T, Bouché O, Lebreton G, et al. Perioperative chemotherapy compared with surgery alone for resectable gastroesophageal adenocarcinoma: An FNCLCC and FFCD multicenter phase III trial. J Clin Oncol. 2011;29(13):1715-21. |
| 34. | Al-Batran SE, Homann N, Pauligk C, Goetze TO, Meiler J, Kasper S, et al. Perioperative chemotherapy with fluorouracil plus leucovorin, oxaliplatin, and docetaxel versus fluorouracil or capecitabine plus cisplatin and epirubicin for locally advanced, resectable gastric or gastro-oesophageal junction adenocarcinoma (FLOT4): A randomised, phase 2/3 trial. Lancet. 2019;393(10184):1948-57. |
| 35. | Bang YJ, Kim YW, Yang HK, Chung HC, Park YK, Lee KH, et al. Adjuvant capecitabine and oxaliplatin for gastric cancer after D2 gastrectomy (CLASSIC): A phase 3 open-label, randomised controlled trial. Lancet. 2012;379(9813):315-21. |
| 36. | Sakuramoto S, Sasako M, Yamaguchi T, Kinoshita T, Fujii M, Nashimoto A, et al. Adjuvant chemotherapy for gastric cancer with S-1, an oral fluoropyrimidine. N Engl J Med. 2007;357(18):1810-20. |
| 37. | Macdonald JS, Smalley SR, Benedetti J, Hundahl SA, Estes NC, Stemmermann GN, et al. Chemoradiotherapy after surgery compared with surgery alone for adenocarcinoma of the stomach or gastroesophageal junction. N Engl J Med. 2001;345(10):725-30. |
| 38. | Cats A, Jansen EPM, van Grieken NCT, Sikorska K, Lind P, Nordsmark M, et al. Chemotherapy versus chemoradiotherapy after surgery and preoperative chemotherapy for resectable gastric cancer (CRITICS): An international, open-label, randomised phase 3 trial. Lancet Oncol. 2018;19(5):616-28. |
| 39. | Lee J, Lim DH, Kim S, Park SH, Park JO, Park YS, et al. Phase III trial comparing capecitabine plus cisplatin versus capecitabine plus cisplatin with concurrent capecitabine radiotherapy in completely resected gastric cancer with D2 lymph node dissection: The ARTIST trial. J Clin Oncol. 2012 ;30(3):268-73. |
| 40. | Park SH, Lim DH, Sohn TS, Lee J, Zang DY, Kim ST, et al. A randomized phase III trial comparing adjuvant single-agent S1, S-1 with oxaliplatin, and postoperative chemoradiation with S-1 and oxaliplatin in patients with node-positive gastric cancer after D2 resection: The ARTIST 2 trial☆. Ann Oncol. 2021;32(3):368-74. |
| 41. | Al-Batran SE, Hartmann JT, Probst S, Schmalenberg H, Hollerbach S, Hofheinz R, et al. Phase III trial in metastatic gastroesophageal adenocarcinoma with fluorouracil, leucovorin plus either oxaliplatin or cisplatin: A study of the Arbeitsgemeinschaft Internistische Onkologie. J Clin Oncol. 2008;26(9):1435-42. |
| 42. | Al-Batran SE, Homann N, Pauligk C, Illerhaus G, Martens UM, Stoehlmacher J, et al. Effect of neoadjuvant chemotherapy followed by surgical resection on survival in patients with limited metastatic gastric or gastroesophageal junction cancer: The AIO-FLOT3 trial. JAMA Oncol. 2017;3(9):1237-44. |
| 43. | Wagner AD, Syn NL, Moehler M, Grothe W, Yong WP, Tai BC, et al. Chemotherapy for advanced gastric cancer. Cochrane Database Syst Rev. 2017;8(8):CD004064. |
| 44. | Fuchs CS, Tomasek J, Yong CJ, Dumitru F, Passalacqua R, Goswami C, et al. Ramucirumab monotherapy for previously treated advanced gastric or gastro-oesophageal junction adenocarcinoma (REGARD): An international, randomised, multicentre, placebo-controlled, phase 3 trial. Lancet. 2014;383(9911):31-39. |
| 45. | Wilke H, Muro K, Van Cutsem E, Oh SC, Bodoky G, Shimada Y, et al. Ramucirumab plus paclitaxel versus placebo plus paclitaxel in patients with previously treated advanced gastric or gastro-oesophageal junction adenocarcinoma (RAINBOW): A double-blind, randomised phase 3 trial. Lancet Oncol. 2014;15(11):1224-35. |
| 46. | Bang YJ, Van Cutsem E, Feyereislova A, Chung HC, Shen L, Sawaki A, et al. Trastuzumab in combination with chemotherapy versus chemotherapy alone for treatment of HER2-positive advanced gastric or gastro-oesophageal junction cancer (ToGA): A phase 3, open-label, randomised controlled trial. Lancet. 2010;376(9742):687-97. |
| 47. | Fuchs CS, Doi T, Jang RW, Muro K, Satoh T, Machado M, et al. Safety and efficacy of pembrolizumab monotherapy in patients with previously treated advanced gastric and gastroesophageal junction cancer: Phase 2 clinical KEYNOTE-059 trial. JAMA Oncol. 2018;4(5):e180013. |
| 48. | Janjigian YY, Shitara K, Moehler M, Garrido M, Salman P, Shen L, et al. First-line nivolumab plus chemotherapy versus chemotherapy alone for advanced gastric, gastro-oesophageal junction, and oesophageal adenocarcinoma (CheckMate 649): A randomised, open-label, phase 3 trial. Lancet. 2021;398(10294):27-40. |
| 49. | Lu Z, Fang Y, Liu C, Zhang X, Xin X, He Y, et al. Early interdisciplinary supportive care in patients with previously untreated metastatic esophagogastric cancer: A phase III randomized controlled trial. J Clin Oncol. 2021;39(7):748-56. |
| 50. | Mansoor W, Roeland EJ, Chaudhry A, Liepa AM, Wei R, Knoderer H, et al. Early weight loss as a prognostic factor in patients with advanced gastric cancer: Analyses from REGARD, RAINBOW, and RAINFALL phase III studies. Oncologist. 2021;26(9):e1538-e1547. |
All Rights Reserved® 2019
Latin American Journal of Clinical Sciences and Medical Technology,Publicación contínua • Editor responsable: Gilberto Castañeda Hernández. • Reserva de Derechos al Uso Exclusivo: 04-2019-062013242000-203; ISSN: 2683-2291; ambos otorgados por el Instituto Nacional del Derecho de Autor. • Responsable de la última actualización de este número, Web Master Hunahpú Velázquez Martínez,
Calle Profesor Miguel Serrano #8, Col. Del Valle, Alcaldía Benito Juárez, CP 03100, Ciudad de México, México. Número telefónico: 55 5405 1396 • Fecha de última modificación, 28 de agosto de 2024.
All Rights Reserved® 2019
Publicación contínua • Editor responsable: Gilberto Castañeda Hernández. • Reserva de Derechos al Uso Exclusivo: 04-2019-062013242000-203; ISSN: 2683-2291; ambos otorgados por el Instituto Nacional del Derecho de Autor. • Responsable de la última actualización de este número, Web Master Hunahpú Velázquez Martínez,
Calle Profesor Miguel Serrano #8, Col. Del Valle, Alcaldía Benito Juárez, CP 03100, Ciudad de México, México. Número telefónico: 55 5405 1396 • Fecha de última modificación, 28 de agosto de 2024.