| ** | Latin American Journal of Clinical Sciences and Medical Technology is an open access magazine. To read all published articles and materials you just need to register Registration is free of charge. Register now If you already have registered please Log In | ** |
aUnidad Funcional de Oncología Torácica, Departamento de Oncología Médica, Instituto Nacional de Cancerología, Ciudad de México, México; bServicio de Radio-oncología, Médica Sur, Ciudad de México, México; cUnidad Funcional de Oncología Torácica, Departamento de Radio-oncología, Instituto Nacional de Cancerología, Ciudad de México, México; dUnidad Funcional de Oncología Torácica, Servicio de Cirugía de Tórax y Neumología, Instituto Nacional de Cancerología, Ciudad de México, México.
Autor para correspondencia: , . Números telefónicos: ; e-mail: drcoronacruz@gmail.com
Lat Am J Clin Sci Med Technol. 2023 May;5:125-130.
Recibido: 07 de marzo, 2023
Aceptado: 06 de abril, 2023
Publicado: 02 de mayo, 2023
Vistas: 4346
Descargas: 46
El cáncer de pulmón (CP) ocupó el segundo lugar en incidencia y el primero en mortalidad en 2020 en el mundo. En México es la quinta neoplasia más frecuente. El cáncer de pulmón de células pequeñas (CPCP) se presenta en el 60% de los casos como enfermedad extensa y el 40% restante como enfermedad limitada. El CPCP es una neoplasia con un comportamiento biológico agresivo, lo que le confiere un peor pronóstico cuando se compara con el cáncer de pulmón de células no pequeñas (CPCNP). El tabaquismo es el factor de riesgo más importante para desarrollar esta neoplasia. El tratamiento de los pacientes con CPCP debe ser multidisciplinario e incluir principalmente cirugía, quimioterapia, radioterapia y terapia dirigida, así como inhibidores de puntos de control inmunológico. En esta oncoguía se presentan los criterios de diagnóstico, estadificación y tratamiento del Instituto Nacional de Cancerología (INCan) con el objetivo de orientar al lector y homogeneizar los criterios de abordaje.
Lung cancer (LC) ranked second in incidence and first in mortality in 2020 worldwide. In Mexico, it is the fifth most frequent neoplasia. Small cell lung cancer (SCLC) presents in 60% of cases as an extensive disease and the remaining 40% as a limited disease. SCLC is a neoplasm with aggressive biological behavior, which gives it a worse prognosis when compared to non-small cell lung cancer (NSCLC). Smoking is the most important risk factor for developing this neoplasm. The treatment of patients with SCLC must be multidisciplinary and include mainly surgery, chemotherapy, radiotherapy, and targeted therapy, as well as immune checkpoint inhibitors. This oncoguía presents the diagnostic, staging, and treatment criteria followed at Instituto Nacional de Cancerología (INCan) in order to guide the reader and standardize the approach criteria.
Estas guías son sugerencias y recomendaciones para el manejo de pacientes en condiciones ideales. No constituyen razonamientos costo-eficientes, ni determinantes para la compra de medicamentos. El objetivo principal de este documento es contribuir a la homogeneidad de criterios en el manejo del cáncer de pulmón de células pequeñas (CPCP) en la práctica habitual de las instituciones de Salud en México.
El cáncer de pulmón (CP) ocupó el segundo lugar en incidencia con 2 206 771 casos en el mundo y el primero en mortalidad con 1 796 144 fallecimientos reportados en 2020. En México es la quinta neoplasia más frecuente con 7 588 casos y la quinta causa en mortalidad con 7100 fallecimientos.1
Para facilitar su estudio, esta neoplasia se divide en dos grandes grupos: cáncer de pulmón de células no pequeñas (CPCNP), que constituye del 80 a 85% de los casos, y el CPCP que se presenta entre el 15 y 20% de los pacientes.2
El CPCP se presenta en el 60% de los casos como enfermedad extensa (etapas IV de la AJCC,American Joint Committe on Cancer ) y el 40% restante como enfermedad limitada (etapas I-III de la AJCC).1,2
El CPCP es una neoplasia con un comportamiento biológico agresivo, lo que le confiere un peor pronóstico cuando se compara con el CPCNP. La mediana de supervivencia (SV) oscila entre 15 a 20 meses para la enfermedad localizada (EL) y de 8 a 13 meses para la enfermedad extensa (EE). A dos años, sólo el 13% de los pacientes con EL y el 3% de los pacientes con EE estarán vivos.3,4
El tabaquismo es el factor de riesgo más importante para desarrollar esta neoplasia porque se asocia con más del 90% de los casos.3
Si bien la mayoría de los pacientes con CP se presenta con dos o más síntomas respiratorios, es importante señalar que éstos por lo general indican una enfermedad avanzada. Por tanto, es fundamental que los médicos de primer contacto tengan conocimiento de los factores de riesgo para esta neoplasia y un alto índice de sospecha.5
Generalmente la radiografía de tórax es el estudio inicial en la mayoría de los pacientes; sin embargo, es crucial saber que la tomografía computarizada (TAC) de tórax es el estudio recomendable cuando se sospecha de CP. La tomografía por emisión de positrones (PET CT) es el mejor estudio para la evaluación de lesiones sospechosas de CP pues además permite establecer la etapa clínica (EC).6
Para la confirmación histológica se cuenta con métodos endoscópicos, percutáneos guiados por imagen y quirúrgicos; la elección de la técnica dependerá del tamaño y localización de la lesión de interés, así como del estado de salud y preferencias del paciente. Siempre se buscará el método que proporcione la mayor cantidad de tejido y que sea la menos mórbida, lo cual dependerá también de la disponibilidad del recurso humano y material de cada centro.5,6
Para el diagnóstico patológico se recomienda seguir la clasificación de tumores pulmonares de la Organización Mundial de la Salud (OMS) 2015.7 Se sugiere obtener suficiente tejido para realizar el perfil básico de inmunohistoquímica y perfil de biomarcadores.
El CPCP es un tumor de origen neuroendocrino, por lo que se recomienda realizar estudios de inmunohistoquímica (IHQ) para el diagnóstico diferencial. La mayoría de los casos será positivo para queratina, antígeno de membrana epitelial y factor de transcripción tiroides 1 (TTF1); este último marcador es útil para confirmar el origen pulmonar de la neoplasia. Los marcadores neuroendocrinos como sinaptofisina, cromogranina y CD56 se pueden expresar hasta en 75% de los casos.8
Los sistemas de estadificación de mayor utilidad —tanto pronóstica como para la selección del tratamiento— son el del Veterans Administration Lung Cancer Chemotherapy Study Group (VALG) y el de la AJCC-TNM9:
- Enfermedad limitada (EL). Tumor confinado a un hemitórax y ganglios regionales que pueden ser incluidos en un campo de radioterapia (correspondiente a los estadios I a IIIB del TNM).
- Enfermedad extensa (EE). Tumor que no puede ser incluido en un campo de radioterapia, entre los que se encuentra la enfermedad metastásica a distancia, la presencia de derrame pericárdico o pleural, ganglios supraclaviculares contralaterales o afección ganglionar contralateral.
Un resumen con los estudios mínimos para el abordaje inicial se presenta en la Figura 1.6-9
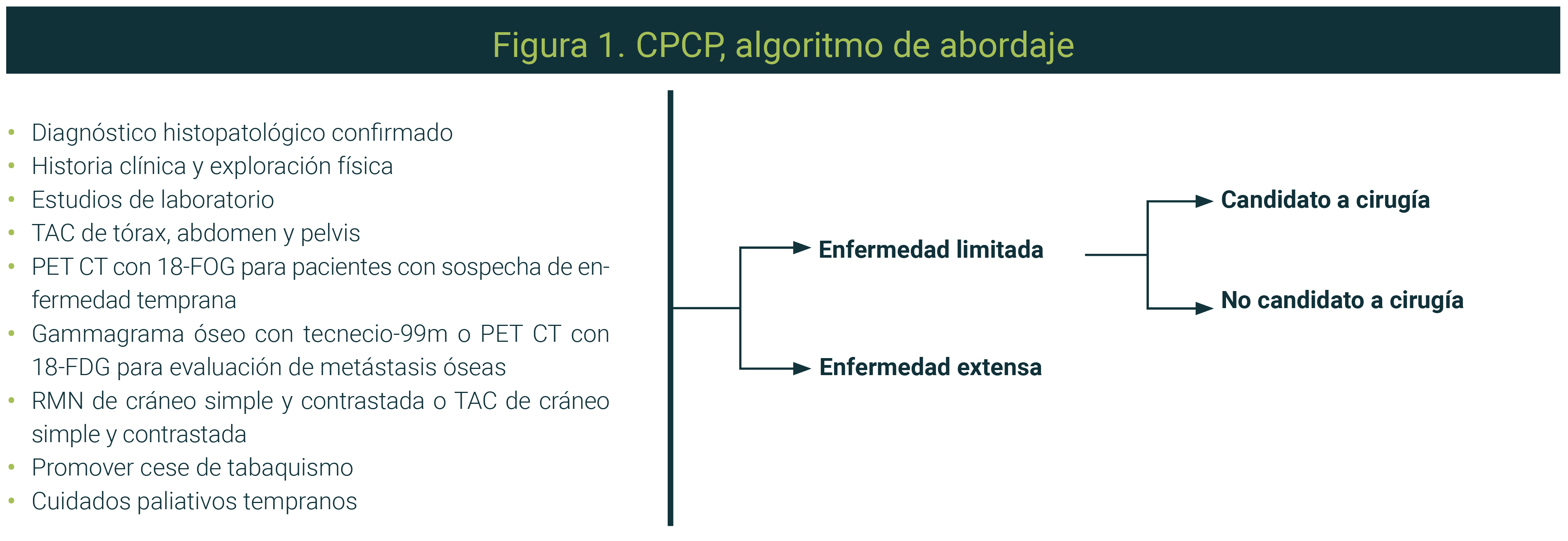
El tratamiento de los pacientes con CPCP debe ser multidisciplinario e incluir principalmente cirugía, quimioterapia, radioterapia y terapia dirigida, así como inhibidores de puntos de control inmunológico.
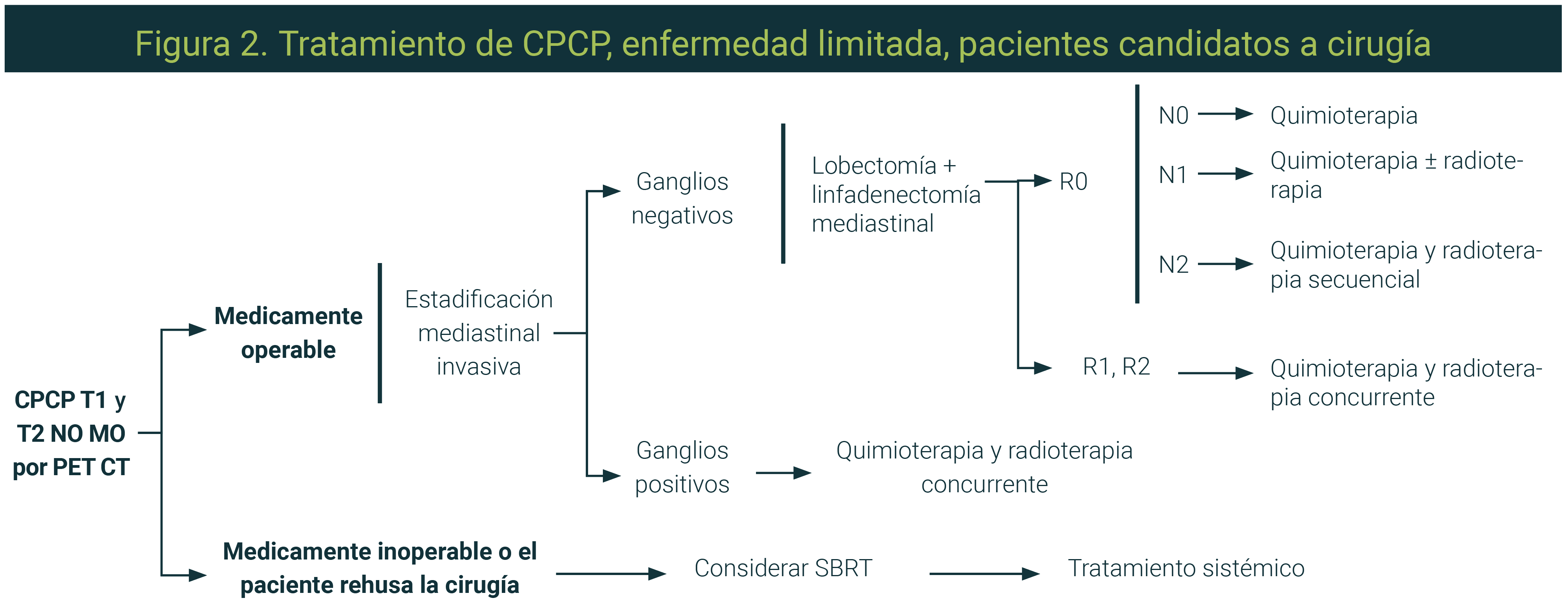
Enfermedad limitada en pacientes candidatos a cirugía10,11
- Los pacientes con enfermedad limitada, que son candidatos a cirugía (Figura 2), tienen intención curativa y tumores T1 y T2 sin evidencia de afección ganglionar mediastinal después de una evaluación no invasiva con PET/CT y también con métodos invasivos como mediastinoscopia, ultrasonido endobronquial (EBUS) y/o ultrasonido esofágico (EUS) o cirugía video-asistida (VATS).
- En pacientes no candidatos a cirugía no se requiere evaluación mediastinal pues no modificará el tratamiento.
- La resección quirúrgica preferida es la lobectomía pulmonar.
- Los métodos aceptados para la evaluación ganglionar del mediastino durante la cirugía para CPCNP son el muestreo mediastinal (MM) y la disección mediastinal sistemática (DMS). Para el caso del CPCP, el consenso de expertos ha optado por realizar siempre una linfadenectomía mediastinal.
- No se debe ofrecer cirugía a pacientes con tumores de mayor tamaño y/o cualquier evidencia de afección ganglionar mediastinal (N1, N2 o N3).
- Se recomienda el tratamiento con radioterapia estereotáxica (SBRT) en pacientes definidos como médicamente inoperables con tumores T1 y T2 N0.
- Se recomienda quimioterapia adyuvante por cuatro ciclos con esquema de platino (carboplatino o cisplatino) + etopósido para los pacientes sometidos a cirugía con márgenes negativos.
- La recomendación de radioterapia postquirúrgica depende de la presencia de ganglios mediastinales en reporte de Patología y se puede ofrecer de manera concurrente o secuencial.
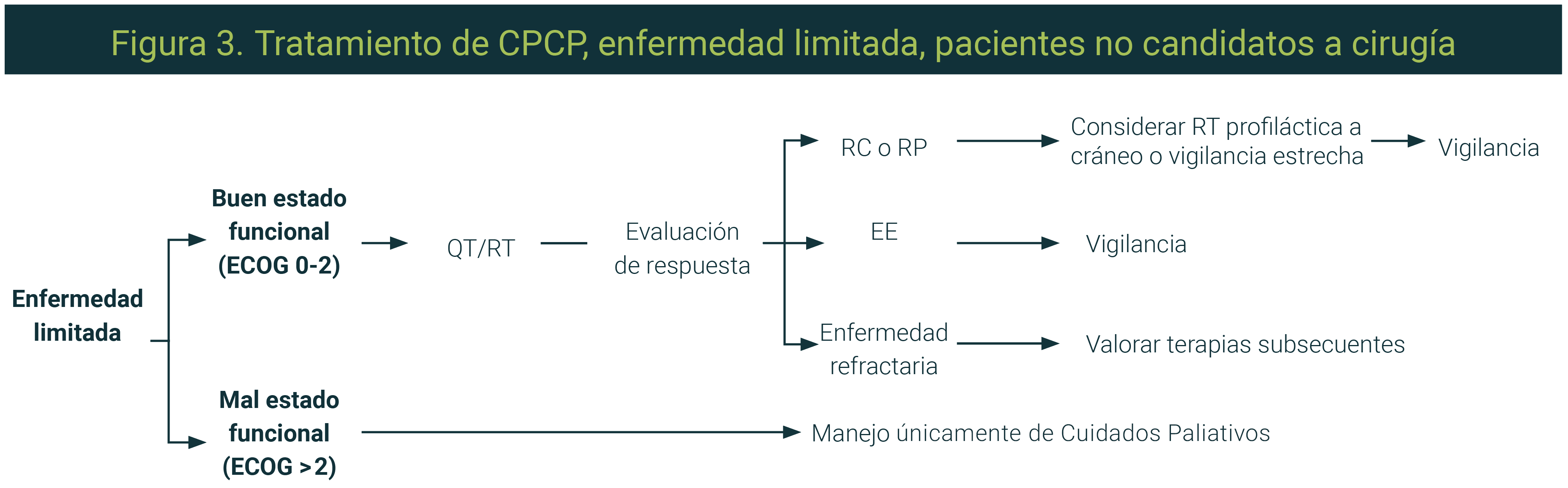
Enfermedad limitada en pacientes no candidatos a cirugía12,13
- El manejo del paciente con enfermedad limitada (Figura 3) consiste en quimio-radioterapia concomitante. Se sugiere el inicio de la radioterapia de manera temprana, no más allá del segundo ciclo de tratamiento con quimioterapia.
- El estándar de tratamiento de quimioterapia utilizado en la concomitancia con radioterapia se basa en platino + etopósido, por 4-6 ciclos, cada 21-28 días.
- Durante la quimio-radioterapia concomitante en la enfermedad limitada no se recomienda el uso profiláctico de factores estimulantes de colonias de granulocitos.
- Para el tratamiento con radioterapia, el esquema recomendado es el bifraccionado (45 Gy en 30 fracciones, 150 cGy por fracción, dos veces al día); sin embargo, el esquema convencional (60-70Gy en 30-35 fracciones) es una alternativa aceptable como esquema de tratamiento.
- En los pacientes con respuesta al tratamiento inicial con quimio-radioterapia se recomienda valorar la radioterapia profiláctica a cráneo a una dosis estándar de 25Gy en 10 fracciones.
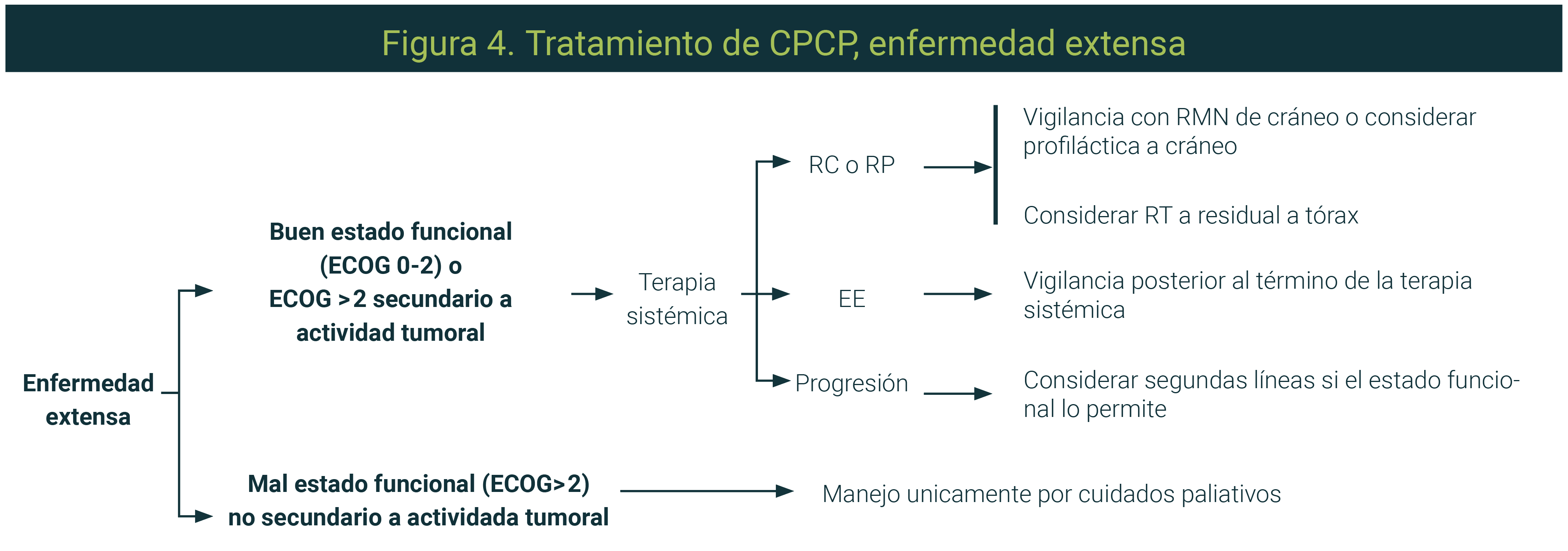
- El tratamiento de primera línea en enfermedad extensa (Figura 4) consiste en quimioterapia paliativa a base de platinos (carboplatino o cisplatino) + etopósido en combinación con inmunoterapia (durvalumab o atezolizumab, este último sólo en combinación de carboplatino) por cuatro ciclos, seguidos de mantenimiento con inmunoterapia.
- Se recomiendan de 4 a 6 ciclos de tratamiento de quimioterapia, aunque con el uso de inmunoterapia lo más indicado son únicamente cuatro ciclos de quimioterapia basada en platinos.
- Se recomienda considerar el tratamiento de consolidación local a tumor residual en tórax, en pacientes con buena respuesta al tratamiento de primera línea.
- El uso de radioterapia profiláctica a cráneo en enfermedad extensa se puede omitir en los pacientes que responden al tratamiento y tienen la posibilidad de seguimiento con vigilancia estrecha. En quienes no se pueda realizar una resonancia magnética nuclear (RMN) de cráneo o puedan llevar seguimiento se recomienda la radioterapia profiláctica a cráneo.
- En pacientes con progresión posterior a seis meses de finalizada la quimioterapia con platinos se recomienda reintroducir esquema basado en platinos.
- En pacientes con progresión a una primera línea con inmunoterapia y que se planea la reintroducción de esquema basado en platinos no se recomienda continuar el tratamiento con inmunoterapia.
- En caso de buen estado funcional, se recomienda ofrecer tratamiento con camptotecinas (topotecán e irinotecán), taxanos (paclitaxel o docetaxel), gemcitabina o lurbinectidina a pacientes con progresión de la enfermedad en menos de seis meses de finalizado el tratamiento de primera línea con platinos (platino resistente o refractario).
- No se recomienda el uso de inmunoterapia en pacientes refractarios a platino por su efectividad limitada.
- La recomendación para terceras líneas de tratamiento o más se basa en el estado funcional del paciente. En caso de ECOG 0-2, se puede recomendar tratamiento con quimioterapia monodroga o inmunoterapia si no se ha recibido previamente.
- El tratamiento estándar de paciente con metástasis cerebrales en CPCP es la radioterapia a cráneo total dosis de 30Gy en 10 fracciones o 20Gy en 5 fracciones. Se puede considerar tratamiento con SBRT en pacientes principalmente con oligometástasis.
Esquema de tratamiento enfermedad temprana candidatos a cirugía, quimioterapia adyuvante
- Cisplatino: 75 mg/m2 SC, día 1 c/21 días (4 ciclos) o carboplatino: AUC5 c/21 días (4 ciclos)
- Etopósido: 120 mg/m2 SC, días 1, 2, 3 cada 21 días (4 ciclos)
- Fosaprepitant: 150 mg, día 1 c/21 días (4 ciclos)
- Ondansetrón: 16 mg, días 1,2,3 c/21 días (4 ciclos)
- Dexametasona: 16 mg, días 1,2,3 c/21 días (4 ciclos)
- Filgrastim: 300 mcg por 5 días, c/21 días (4 ciclos)
Esquema de tratamiento enfermedad temprana, quimioradioterapia
- Cisplatino: 75 mg/m2 SC, día 1 c/21 días (4 ciclos) o carboplatino: AUC5 c/21 días (4 ciclos)
- Etopósido: 120 mg/m2 SC, días 1, 2, 3 cada 21 días (4 ciclos)
- Fosaprepitant: 150 mg, día 1 c/21 días (4 ciclos)
- Ondansetrón: 16 mg, días 1,2,3 c/21 días (4 ciclos)
- Dexametasona: 16 mg, días 1,2,3 c/21 días (4 ciclos)
Esquema de tratamiento enfermedad extensa primera línea
- Cisplatino: 75mg/m2 SC, día 1 c/21 días (4 ciclos) o carboplatino: AUC5 c/21 días (4 ciclos)
- Etopósido: 120 mg/m2 SC, días 1, 2, 3 cada 21 días (4 ciclos)
- Durvalumab 1500 mg cada 21 días los primeros 4 ciclos, seguidos por 1500 mg cada 28 días hasta progresión
- Fosaprepitant: 150 mg, día 1 c/21 días (4 ciclos)
- Ondansetrón: 16 mg, días 1,2,3 c/21 días (4 ciclos)
- Dexametasona: 8 mg, días 1,2,3 c/21 días (4 ciclos)
- Carboplatino: AUC5 c/21 días (4 ciclos)
- Etopósido: 120 mg/m2 SC, días 1, 2, 3 cada 21 días (4 ciclos)
- Atezolizumab 1200 mg cada 21 días, iniciar con la quimioterapia y continuar hasta progresión
- Fosaprepitant: 150 mg, día 1 c/21 días (4 ciclos)
- Ondansetrón: 16 mg, días 1,2,3 c/21 días (4 ciclos)
- Dexametasona: 16 mg, días 1,2,3 c/21 días (4 ciclos)
Esquema de tratamiento segunda línea
- Irinotecán: 60 mg/m2 SC, días 1, 8 y 15 c/4 semanas hasta progresión
- Ondansetrón: 8 mg, días 1, 8 y 15 c/4 hasta progresión
- Dexametasona: 8 mg, días 1, 8 y 15 c/4 hasta progresión
- Topotecán: 1.7 mg/m2 SC c/3 semanas, días 1 a 5 hasta progresión
- Ondansetrón: 8 mg c/3 semanas, días 1 a 5 hasta progresión
- Dexametasona: 16 mg c/3 semanas, días 1 a 5 hasta progresión
- Gemcitabina: 1000 mg/mg2, días 1,8,15 cada 28 días hasta progresión
- Ondasetrón: 8 mg días 1, 8, 15 cada 28 días hasta progresión
- Dexametasona: 8 mg días 1, 8, 15 cada 28 días hasta progresión
- Paclitaxel: 175 mg/m2 día 1 cada 21 días hasta progresión
- Ondansetrón: 8 mg cada 21 días hasta progresión
- Dexametasona: 8 mg cada 21 días hasta progresión
- Clorfenamina: 10 mg cada 21 días hasta progresión
El CPCP constituye una neoplasia biológicamente agresiva y de alta letalidad. La estandarización de los procedimientos presentados en esta oncoguía busca ofrecer al clínico un resumen de las recomendaciones para el abordaje y tratamiento de estos pacientes, según la mejor evidencia disponible a la fecha y con la finalidad de optimizar el tratamiento y mejorar el pronóstico de los pacientes. Se debe promover tanto el diagnóstico oportuno como el incremento en los programas de prevención del tabaquismo, su principal factor de riesgo, dado que se le considera una neoplasia prevenible.
Agradecemos a la Dirección de Docencia del INCan el interés y las facilidades para el desarrollo de esta publicación. De igual forma, un reconocimiento a todo el personal médico y paramédico de la Unidad Funcional de Oncología Torácica del INCan que contribuyen para el desarrollo y actualización de estas guías.
Los autores declaran no tener conflictos de interés
| 1. | Sharma R. Mapping of global, regional and national incidence, mortality and mortality-to-incidence ratio of lung cancer in 2020 and 2050. Int J Clin Oncol. 2022;27(4):665-75. |
| 2. | World Health Organization. International Agency for Research on Cancer. Mexico fact sheets (GLOBOCAN 2020). Available from URL: http://gco.iarc.fr/today/home// |
| 3. | Govindan R, Page N, Morgensztern D, Read W, Tierney R, Vlahiotis A, et al. Changing epidemiology of small-cell lung cancer in the United States over the last 30 years: Analysis of the surveillance, epidemiologic, and end results database. J Clin Oncol. 2006;24(28):4539-44. |
| 4. | Osterlind K, Hansen HH, Hansen M, Dombernowsky P, Andersen PK. Long-term disease-free survival in small-cell carcinoma of the lung: A study of clinical determinants. J Clin Oncol. 1986;4(9):1307-13. |
| 5. | Ettinger DS, Aisner J. Changing face of small-cell lung cancer: Real and artifact. J Clin Oncol. 2006;24(28):4526-7. |
| 6. | Albain KS, Crowley JJ, Livingston RB. Long-term survival and toxicity in small cell lung cancer. Expanded Southwest Oncology Group experience. Chest. 1991;99(6):1425-32. |
| 7. | Travis WD, Brambilla E, Nicholson AG, Yatabe Y, Austin JHM, Beasley MB, et al. The 2015 World Health Organization classification of lung tumors impact of genetic, clinical and radiologic advances since the 2004 classification. J Thorac Oncol.2015;10(9):1243-60. |
| 8. | Guinee DG Jr, Fishback NF, Koss MN, Abbondanzo SL, Travis WD. The spectrum of immunohistochemical staining of small-cell lung carcinoma in specimens from transbronchial and open-lung biopsies. Am J Clin Pathol. 1994;102(4):406-14. |
| 9. | Lababede O, Meziane MA. The eight edition of TNM staging of lung cancer: Reference chart and diagrams. Oncologist. 2018;23(7):844-48. |
| 10. | Takenaka T, Takenoyama M, Inamasu E, Yoshida T, Toyokawa G, Nosali K, et al. Role of surgical resection for patients with limited disease small-cell lung cancer. Lung Cancer. 2015;88(1):52-6. |
| 11. | Wakeam E, Byrne JP, Darling GE, Varghese Jr TK. Surgical treatment for early small cell lung cancer: Variability in practice and impact on survival. Ann Thorac Surg. 2017;104(6):1872-80. |
| 12. | Cabrera-Miranda LA, Lozano-Ruiz FJ, Blake-Cerda M, Corona-Cruz JF, Sánchez-Reyes R, Pérez-Álvarez SI, et al. Guía de práctica clínica para el manejo del cáncer de pulmón de células pequeñas: enfermedad limitada. Gac Mex Oncol. 2023; 22(1):3-23. |
| 13. | Früh M, De Ruysscher D, Popat S, Crinò L, Peters S, Felip E, et al. Small-cell lung cancer (SCLC): ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2013;24(Suppl 6):vi99- vi105. |
All Rights Reserved® 2019
Latin American Journal of Clinical Sciences and Medical Technology,Publicación contínua • Editor responsable: Gilberto Castañeda Hernández. • Reserva de Derechos al Uso Exclusivo: 04-2019-062013242000-203; ISSN: 2683-2291; ambos otorgados por el Instituto Nacional del Derecho de Autor. • Responsable de la última actualización de este número, Web Master Hunahpú Velázquez Martínez,
Calle Profesor Miguel Serrano #8, Col. Del Valle, Alcaldía Benito Juárez, CP 03100, Ciudad de México, México. Número telefónico: 55 5405 1396 • Fecha de última modificación, 28 de agosto de 2024.
All Rights Reserved® 2019
Publicación contínua • Editor responsable: Gilberto Castañeda Hernández. • Reserva de Derechos al Uso Exclusivo: 04-2019-062013242000-203; ISSN: 2683-2291; ambos otorgados por el Instituto Nacional del Derecho de Autor. • Responsable de la última actualización de este número, Web Master Hunahpú Velázquez Martínez,
Calle Profesor Miguel Serrano #8, Col. Del Valle, Alcaldía Benito Juárez, CP 03100, Ciudad de México, México. Número telefónico: 55 5405 1396 • Fecha de última modificación, 28 de agosto de 2024.