| ** | Latin American Journal of Clinical Sciences and Medical Technology is an open access magazine. To read all published articles and materials you just need to register Registration is free of charge. Register now If you already have registered please Log In | ** |
aDepartamento de Anestesia Oncológica, Instituto Nacional de Cancerología, Ciudad de México, México.
Autor para correspondencia: , . Números telefónicos: ; e-mail: cuellarluis@hotmail.com
Lat Am J Clin Sci Med Technol. 2023 Aug;5:206-223.
Recibido: 02 de junio, 2023
Aceptado: 07 de agosto, 2023
Publicado: 29 de agosto, 2023
Vistas: 27575
Descargas: 276
El cáncer es la segunda causa de muerte a nivel mundial. Debido a la mejora en las modalidades de diagnóstico, más pacientes llegan al quirófano para cirugías e intervenciones específicas para el paciente oncológico. La anestesia y los cuidados intensivos específicos de las cirugías oncológicas precisan de numerosos conocimientos especializados para lograr un mejor manejo perioperatorio de estos casos, disminuir las complicaciones postoperatorias y prolongar las supervivencias global y libre de cáncer después de la cirugía. La alta especialidad en oncoanestesia ha permitido ampliar el conocimiento de las necesidades de pacientes con cáncer y lograr un manejo anestésico con claros objetivos oncológicos.
Cancer is the second cause of death worldwide. Due to the improvement in diagnostic modalities, more patients are coming to the operating room for specific surgeries and interventions for the cancer patient. Anesthesia and specific intensive care of oncological surgeries require a lot of specialized knowledge for better perioperative management of these cases, to reduce postoperative complications, and prolong overall and cancer-free survival after surgery. The high specialty in oncoanesthesia has made it possible to broaden the knowledge of the needs of cancer patients and thus achieve anesthetic management with clear oncological objectives.
De acuerdo con las estimaciones de GLOBOCAN 2020, en el mundo se encontraron 19.3 millones de nuevos casos de cáncer y casi 10.0 millones de muertes por esa causa.1
El cáncer de mama femenino superó al cáncer pulmonar como el cáncer diagnosticado con mayor frecuencia, con un estimado de 2.3 millones de casos nuevos (11.7%), seguido de cáncer de pulmón (11.4%), colorrectal (10.0%), próstata (7.3%) y estómago (5.6%).1
En México, de acuerdo con el reporte del INEGI (2022) a propósito del Día Internacional de la Lucha contra el Cáncer de Mama (19 de octubre), 90,525 personas murieron durante 2021 por tumores malignos (8.1% del total de defunciones) y de éstas, 7,973 murieron por cáncer de mama.2
Por tanto, es evidente que la carga global del cáncer va en aumento y muchos más pacientes se presentarán para cirugía u otras intervenciones diagnósticas o terapéuticas oncológicas que requieren anestesia. La terapia oncológica es única porque requiere de un equipo multidisciplinario de oncólogos quirúrgicos, médicos, radiólogos, además de especialistas en Medicina Paliativa y anestesiólogos.3
Actualmente, la resección quirúrgica se considera el método más efectivo para extirpar el tumor primario y para aumentar la supervivencia a largo plazo en la gran mayoría de los tumores sólidos. Aun así, la recurrencia tumoral y el desarrollo de metástasis son muy frecuentes, incluso después del tratamiento quirúrgico, también son responsables de hasta el 90% de la mortalidad relacionada con cáncer.4
No es nuevo el creciente interés en cómo las intervenciones perioperatorias pudieran alterar el resultado oncológico. Los «criterios de referencia» de la oncoanestesia son:
- minimizar la morbilidad perioperatoria y el dolor por cáncer persistente posquirúrgico para que los pacientes puedan comenzar la quimioterapia o radioterapia postoperatoria planificada;
- regresar al tratamiento oncológico previsto (RIOT) a tiempo para reducir la metástasis y la recurrencia.5
Si bien continuamos actualizándonos en la biología perioperatoria en el contexto de la atención del cáncer, nuestros esfuerzos no sólo deben centrarse en optimizar la condición preoperatoria del paciente (prehabilitación y optimización) para garantizar los máximos beneficios de la cirugía, debemos conocer profundamentelos efectos adversos y toxicidades asociados con las terapias contra el cáncer (agentes quimioterapéuticos, inmunoterapia y radioterapia), así como el estado funcional general del paciente y el momento de la intervención quirúrgica.
Es preciso reconocer la importancia de la mejoría nutricional, el acondicionamiento fisiológico (entrenamiento cardiovascular y de fuerza), el control de la anemia y la terapia conductual para reducir la respuesta al estrés.
Asimismo, es crucial comprender los procesos fisiopatológicos (respuesta de estrés neural-inflamatorio-inmunomoduladora) y cómo podemos modularlos con nuestro arsenal actual de técnicas anestésicas, incluidos los agentes anestésicos (p. ej., volátiles, TIVA [total intravenousanesthesia, anestesia total intravenosa], técnicas neuroaxiales) y complementos perioperatorios (p. ej., opioides, AINE). Ello ayudará a minimizar las complicaciones posoperatorias y garantizar que el paciente se mantenga «encaminado» para completar su camino terapéutico bajo la mayor evidencia disponible.
Estas guías son sugerencias y recomendaciones para el manejo anestésico de pacientes oncológicos en condiciones ideales. Sus objetivos son exponer brevemente los tópicos relevantes del quehacer del anestesiólogo oncólogo y mostrar la evidencia más reciente y la experiencia del Departamento de Anestesia Oncológica del Instituto Nacional de Cancerología (INCan) en el manejo anestésico con objetivos oncológicos.
El manejo preoperatorio del paciente oncológico puede ser complejo. Los efectos directos e indirectos del cáncer y los efectos secundarios de la terapia oncológica dirigida pueden influir en la evaluación y el manejo perioperatorio.
Debemos considerar la historia natural del cáncer, el estado nutricional y funcional actual, síntomas y problemas médicos generales agregados, así como los efectos de las terapias recibidas.
La importancia es detectar y conocer condiciones que puedan ser optimizadas o que requieran un manejo específico durante el perioperatorio, sin que esto retrase la oportuna entrega de la terapia definitiva, ya sea cirugía, quimioterapia o radioterapia. La cirugía del cáncer generalmente no es electiva y, por lo tanto, la cantidad de tiempo disponible para optimizar medicamente a un paciente puede ser limitada.6
A continuación, se mencionarán algunos detalles específicos a considerar en la valoración del paciente oncológico previo a su ingreso a cirugía, sin olvidar la aplicación de escalas que deben ser aplicadas de forma individualizada: RCRI, ARISCAT, NSQIP, SORT, P-POSSUM, GUPTA, CAPRINI y GOLDMAN.7
Estado funcional
Existen dos escalas frecuentemente utilizadas en la valoración del estado funcional de pacientes oncológicos: Eastern Cooperative Oncology Group (ECOG) y Karnofsky. Aplicarlas nos permite conocer y evaluar de forma periódica una posible disminución funcional de nuestros pacientes a través del tiempo y de sus tratamientos oncológicos.
Nutrición
Los pacientes con cáncer pueden sufrir de desnutrición por diversos factores. La ingesta de alimentos puede resultar afectada por dolor, náusea, estomatitis o tumores que afectan la orofaringe o el tracto gastrointestinal.
Dolor
Numerosos pacientes recibirán formas de opioides de acción prolongada y pueden requerir la rotación a opioides de acción corta en el período perioperatorio.
Los medicamentos antinflamatorios no esteroideos (AINE) pueden causar sangrado, gastritis y deterioro de la función renal; los opioides pueden causar náusea, estreñimiento, sedación y delirio. En la Oncoguía del manejo de dolor en cáncer 2023 y en Portenoy R (2022) se ofrece mayor información al respecto.8,9
Valoración cardiovascular
Los pacientes con cáncer tienen riesgo de enfermedad pericárdica maligna y no maligna. Las metástasis al pericardio pueden causar derrames, taponamiento y pericarditis constrictiva.
La radioterapia al mediastino puede causar pericarditis constrictiva o derrames con o sin taponamiento, la cual puede presentarse meses o años después del tratamiento con radiación.
En consecuencia, se debe realizar una ecocardiografía si el examen físico revela hallazgos consistentes con taponamiento o constricción, o si la electrocardiografía o las imágenes sugieren un derrame pericárdico significativo.
El taponamiento y la pericarditis constrictiva deben tratarse antes de la cirugía siempre que sea posible. Los pacientes con derrames pericárdicos malignos asintomáticos deben ser monitoreados cuidadosamente en busca de taponamiento perioperatorio.
Ciertos agentes quimioterapéuticos (particularmente trastuzumab y las antraciclinas) causan cardiotoxicidad significativa. La cardiopatía preexistente, la radioterapia y la exposición a otros agentes quimioterapéuticos (taxanos, trastuzumab) pueden reducir el umbral de dosis acumulada de antraciclina en el que se desarrolla la miocardiopatía.10
Efectos de masa cardiopulmonar
Los pacientes con tumores en las vías respiratorias centrales o adyacentes a ellas tienen riesgo de obstrucción en dichas vías. El estridor u otros signos o síntomas de obstrucción de vías respiratorias superiores deben evaluarse antes de la operación mediante laringoscopia y estudios de imagen.
Las masas en el mediastino anterior y medio pueden comprimir las vías respiratorias inferiores, el corazón y los vasos principales. De modo que la evaluación preoperatoria debe incluir una revisión detallada de los síntomas respiratorios, incluidos estridor, disnea, sibilancias y ortopnea, así como un examen para detectar signos de síndrome de vena cava superior.
Los pacientes con cualquier evidencia de compresión de las vías respiratorias centrales, cardiacas o de los vasos principales pueden requerir precauciones y cuidados anestésicos especiales, que incluyen intubación con fibra óptica mientras están despiertos, ventilación espontánea en cirugía, posición de urgencia, broncoscopia rígida o bypass cardiopulmonar (en caso de colapso cardiovascular).
Toxicidad pulmonar
Tanto la quimioterapia como la radioterapia pueden producir toxicidad pulmonar, que puede intensificarse cuando se administran de forma concomitante.
La bleomicina se asocia con toxicidad pulmonar significativa en hasta el 10% de los pacientes, y el tratamiento con oxígeno inhalado suplementario puede inducir toxicidad pulmonar varios años después del tratamiento. Por ende, se debe titular cuidadosamente el oxígeno suplementario durante la cirugía.10,11
Estado endocrino y electrolítico
Numerosos regímenes quimioterapéuticos incluyen glucocorticoides (ya sea como agente terapéutico o como componente de la premedicación) para prevenir las náuseas y los vómitos inducidos por la quimioterapia o una reacción a la infusión. Sin embargo, pueden desenmascarar la diabetes oculta o exacerbar los niveles de glucosa en sangre, previamente controlados.
La hiponatremia ocurre en pacientes con cáncer y puede atribuirse a efectos paraneoplásicos del tumor o ser causada por tratamientos. Por ello, es necesario identificarla, evitar exacerbarla con soluciones intravenosas hipotónicas, monitorear de cerca y manejar cuidadosamente al paciente en el período postoperatorio.
La hipercalcemia es otra complicación común y ocurre en hasta el 15% de los pacientes. Se recomienda no descartar una medición de calcio sérico preoperatorio. Si se identifica hipercalcemia, se debe optimizar la hidratación del paciente y normalizar los niveles de calcio antes de la cirugía.
La insuficiencia suprarrenal puede ocurrir como resultado de la supresión suprarrenal del tratamiento crónico con glucocorticoides o, con menor frecuencia, de la enfermedad metastásica en ambas glándulas suprarrenales.
La radioterapia en el cuello puede causar hipotiroidismo y a su vez complicar el tratamiento a largo plazo con los inhibidores de la tirosina cinasa, sunitinib y sorafenib.
Debido a que el hipotiroidismo se asocia con una cicatrización deficiente del sitio quirúrgico, se deben medir las concentraciones séricas de TSH y T4 libre antes de la cirugía en pacientes que hayan recibido una dosis total de más de 10 Gy en el cuello o que estén recibiendo tratamiento con sunitinib o sorafenib.
Los pacientes que presenten hipotiroidismo deben recibir suplementos de hormona tiroidea antes de la cirugía y evitar complicaciones propias del descontrol hormonal.12,13
Los feocromocitomas son tumores raros, neuroendocrinos, secretores de catecolaminas que surgen de las células cromafines. En esta condición clínica se indica una preparación farmacológica preoperatoria, primero con alfa-adrenérgicos farmacológicos, seguidos de un bloqueo beta-adrenérgico que tiene como objetivo controlar la hipertensión, incluida la prevención de una crisis hipertensiva durante la cirugía.
Estado hematológico
La hipercoagulabilidad es común en pacientes oncológicos, particularmente en aquéllos con enfermedad avanzada y tumores cerebrales. Puede deberse a niveles plasmáticos elevados de factores de coagulación, citocinas o a una mayor liberación del activador tisular del plasminógeno. La hipercoagulabilidad también es un posible efecto secundario del tratamiento del cáncer con ciertos medicamentos (bleomicina, cisplatino).
El tromboembolismo venoso perioperatorio es más frecuente en pacientes con cáncer que en la población general y ocurre hasta en 40% de los pacientes oncológicos. Esta consideración resulta más que evidente en la puntuación de CAPRINI, por lo que es necesario conocer las opciones de profilaxis de acuerdo con el riesgo estadificado.14
La anemia es otra complicación común en pacientes y es un predictor independiente de mal pronóstico; por tanto, los pacientes deben someterse a un hemograma completo con diferencial antes de la cirugía.
Generalmente, la deficiencia de hierro contribuye al desarrollo de la anemia, particularmente en pacientes con tumores de cabeza y cuello y neoplasias malignas gastrointestinales. Idealmente debe tratarse antes de la cirugía para mejorar la fuerza, la resistencia y, posiblemente, la calidad de vida del paciente.
Se deben considerar de forma individual los suplementos de hierro por vía oral o el reemplazo bajo formulaciones intravenosas; en la actualidad, el hierro intravenoso es el más seguro.15
Los pacientes mielosuprimidos, como resultado de la quimioterapia o de una neoplasia hematológica, tienen mayor riesgo de infección. El riesgo aumenta cuando la neutropenia y la linfopenia son más largas. Siempre que sea posible, la cirugía que no sea de emergencia debe posponerse en pacientes neutropénicos.
La fiebre postoperatoria es común y si se desarrolla en el contexto de neutropenia, se necesitan intervenciones diagnósticas y terapéuticas agresivas.
La trombocitopenia ocurre en estos pacientes como resultado de la malignidad o del tratamiento. En general, un recuento de plaquetas de al menos 50,000/microL es adecuado para la mayoría de los procedimientos quirúrgicos, pero también se debe considerar el procedimiento específico y la función plaquetaria.16
Por lo tanto, el conocimiento de la valoración preoperatoria permite brindar al paciente oncológico su optimización antes de la cirugía y una adecuada prehabilitación de la mano de protocolos de recuperación acelerada. Proporcionar un plan anestésico apropiado logra disminuir complicaciones y el oportuno retorno a su terapia oncológica.
La misión de la sociedad ERAS (Enhanced Recovery After Surgery) es desarrollar la atención perioperatoria y mejorar la recuperación mediante la investigación, la educación, la auditoría y la implementación de la práctica basada en la evidencia.
El Dr. Henry Kehlet fue el primero en sugerir el concepto de cirugía fast-track en la década de los noventa. Demostró que, aplicando principios perioperatorios basados en evidencia, la estancia intrahospitalaria podía disminuir entre 2 y 3 días, lo cual repercutiría positivamente en la recuperación del paciente.
El primer protocolo se publicó en 2005 para pacientes sometidos a cirugía de colon y se complementó en 2009 con información para cirugía rectal.
A lo largo de los años se han realizado múltiples publicaciones, actualizaciones y se han implementado varios programas y directrices para adaptarse a los retos que la sociedad ha enfrentado recientemente, incluida la pandemia de COVID 19 (Figura 1).17

Figura elaborada por Diana Laura Palomares-Gómez; Anestesia Oncológica del Instituto Nacional de Cancerología.
Los protocolos enfatizan la necesidad de describir ampliamente al paciente todo el acto perioperatorio con el objetivo de que lo comprenda, participe activamente, se atenúe la ansiedad y se establezcan claramente las expectativas tanto del equipo quirúrgico como del paciente.17,18
Idealmente, se deben cubrir todas las pautas para obtener el mejor resultado, pero se ha observado que cumplir con el 90% de las estrategias se traduce en menos del 20% de complicaciones en el postoperatorio (véase la Tabla 1).17,18
| Tabla 1. Recomendaciones compartidas entre los programas ERAS | |
|---|---|
| Ayuno | Permitir el consumo de líquidos claros hasta 2 h y sólidos hasta 6 h, previo a la inducción anestésica. |
| Carga de carbohidratos | Administrar maltodextrina vía oral al 12.5%, 100 g en la noche, previa a la cirugía y 50 g 2 - 3 h previo a la inducción. |
| Prevención de NVPO | Identificar FR con escala: si presenta 1 - 2 FR, se recomienda el uso de 2 antieméticos, si cuenta con 3-4 FR la combinación de 3-4 medicamentos, así como el uso de TIVA. |
| Tromboprofilaxis | Uso de heparina de bajo peso molecular o no fraccionada 2-12 horas, previo a la cirugía y continuarla hasta el egreso hospitalario. |
| Premedicación | No se recomienda el uso de ansiolíticos u opioides de larga duración. Evitar el uso de benzodiacepinas de corta duración en el paciente geriátrico. |
| Alcohol/tabaco | Se debe suspender el consumo por lo menos cuatro semanas antes del evento quirúrgico. |
| Prevención de anemia | Realizar el tamizaje 3-4 semanas antes de la cirugía con la intención de indicar hierro, ácido fólico, vitamina B12 o eritropoyetina acorde con las necesidades del paciente. |
| Antibioticoterapia | Administrar el fármaco durante los 60 minutos previos a la incisión quirúrgica, ajustar dosis si el IMC>35 kg/m2. Se debe repetir dosis en caso de sangrado >1500 ml y en cirugías prolongadas acorde con la vida media del antibiótico seleccionado. |
| Manejo anestésico | Se recomienda utilizar monitoreo de la profundidad anestésica y del bloqueo neuromuscular. |
| Hipotermia | La temperatura se reduce 0.5-1.5°C durante los primeros 30 minutos de la cirugía, por lo que se recomienda mantener un calentamiento activo. |
| Cirugía | Preferir uso de técnicas mínimamente invasivas. |
| Glicemia | Se recomienda mantener las cifras lo más cercanas a lo normal, sin comprometer la seguridad del paciente. |
| Manejo hídrico | Mantener un balance neutro, evitar la sobrecarga hídrica (ganancia de peso >2.5 kg en el postoperatorio). Promover el uso de soluciones cristaloides balanceadas con una infusión basal de 3 ±2 ml/kg/h más una reanimación guiada por objetivos. |
| Analgesia multimodal | Combinación de técnica neuroaxial, regional e infusiones intravenosas (opioides, paracetamol, anestésicos locales, AINE). |
| Otros | Uso de escalas de valoración preoperatoria (P - POSSUM, índice de LEE, test de caminata, CPET), nutrición preoperatoria, prevención de delirium postoperatorio, atenuación y tratamiento de íleo, movilización temprana, evitar uso de sonda nasogástrica (valorar en casos de cirugía gástrica y esofágica) y de drenajes, así como retirar de manera temprana la sonda urinaria. |
| ERAS: Enhanced Recovery After Surgery; NVPO: áusea y vómito postoperatorio; FR: factor de riesgo; TIVA: (total intravenous anesthesia) anestesia total intravenosa; IMC: índice de masa corporal; AINE: antinflamatorios no esteroideos; CPET: (cardiopulmonary exercise testing) prueba cardiopulmonar de ejercicio. Tabla realizada por Diana Laura Palomares - Gómez; Anestesia Oncológica del Instituto Nacional de Cancerología. | |
Es necesario contar con un equipo profesional, multidisciplinario que priorice el retorno del paciente a la vida cotidiana y, específicamente en el paciente con cáncer, para que continúe con el tratamiento previsto, ya sea quimioterapia (QT), radioterapia (RT) o inmunoterapia.
En 2014, Aloia y colaboradores reportaron que al adoptar las pautas del protocolo ERAS en pacientes llevados a resección hepática se redujo el tiempo de inicio de la terapia adyuvante, el cual es fundamental para el pronóstico y calidad de vida de los pacientes.
Dichos autores describieron el concepto RIOT (Return to Intended Oncologic Therapy), que es uno de nuestros principales objetivos como anestesiólogos, por lo que en esta guía se enfatiza en recomendaciones específicas para la cirugía oncológica con un apartado especial para la citorreducción, con quimioterapia intraperitoneal hipertérmica (Tabla 2).19-24
| Tabla 2. Recomendaciones específicas de ERAS con enfoque oncológico | |
|---|---|
Cirugía de hígado |
|
Cirugía ginecológia |
|
Cirugía de esófago |
|
Cirugía de tórax |
|
| ERAS: Enhanced Recovery After Surgery; PVC: presión venosa central; HIPEC: (hyperthermic intraperitoneal chemotherapy) quimioterapia intraperitoneal hipertérmica; QT: quimioterapia; RT: radioterapia; PEEP: (positive end - expiratory pressure) presión positiva al final de la expiración; CPAP: (continuous positive airway pressure) presión positiva continua de las vías respiratorias; UTI: Unidad de Cuidados Intensivos; FIO2: fracción inspirada de oxígeno; CAM: concentración alveolar mínima. Tabla realizada por Diana Laura Palomares - Gómez; Anestesia Oncológica del Instituto Nacional de Cancerología | |
HIPEC
El uso de quimioterapia intraperitoneal hipertérmica (HIPEC, hyperthermic intraperitoneal chemotherapy) es uno de los procedimientos quirúrgicos más complejos y de alto riesgo, realizados exclusivamente en pacientes oncológicos. Por tanto, es necesario destacar algunas de las recomendaciones de las guías publicadas en 2020.
Si el paciente se encuentra con QT sistémica se debe suspender por lo menos tres semanas antes del evento quirúrgico. En caso de que se administren antiangiogénicos, se deben suspender cinco semanas antes. No se ha demostrado que una técnica anestésica sea superior a otra (halogenado vs. TIVA [total intravenous anesthesia]).25,26
Se recomienda el uso de bloqueo peridural porque es fundamental para la analgesia transoperatoria y se ha observado que su uso en el postoperatorio (>72 h) se ha relacionado con menor incidencia de íleo.
Se sugiere instalar una línea arterial para guiar el uso de agentes vasoactivos y control de gases arteriales, así como un monitoreo continuo de la temperatura tanto intraperitoneal como central para tratar de prevenir la hipertermia (>41°C).
Hasta el 40% de los pacientes puede presentar coagulopatía; sin embargo, la transfusión dependerá del contexto clínico de cada paciente. La presencia de acidosis metabólica no es una contraindicación para realizar una extubación temprana, por lo que es necesario evaluar todos los criterios para realizarla de manera segura.25,26
La incidencia de lesión renal se ha reportado entre 1.3 y 5.7% de los casos. Suele ser multifactorial e incidir considerablemente en los quimioterapéuticos (principalmente cisplatino y mitomicina C), por lo que es necesario optimizar el volumen intravascular, el gasto cardiaco, el suministro de oxígeno, y llevar a cabo una reanimación hídrica guiada por objetivos (se debe tratar de garantizar una diuresis mínima de 1 ml/kg/h).25,26
En conclusión, el protocolo ERAS en el contexto del paciente con cáncer requiere un abordaje perioperatorio multimodal. Su objetivo es la rápida recuperación de los pacientes sometidos a cirugía, lo cual favorece su reincorporación al tratamiento oncológico establecido.
Cuando el cáncer regresa después de un período de remisión, se considera una recurrencia. Es decir, la reproducción del tumor en el mismo sitio donde se originó o en otro lugar, después de haber desaparecido.
La cirugía es un período crítico en la supervivencia de los pacientes con cáncer. Si bien la resección quirúrgica de tumores primarios ha demostrado prolongar la vida de estos pacientes, también puede promover mecanismos asociados con la progresión metastásica. Es entonces cuando se considera que el manejo anestésico podría desempeñar un papel fundamental en el paciente oncológico que se somete a uno de los mayores estresores fisiológicos, como lo es la cirugía.28
Sin embargo, y antes de explicar acerca de la anestesia y la recurrencia, debemos recalcar que un parámetro de calidad en anestesia oncológica es el RIOT, que mide las intervenciones perioperatorias y su efecto en la recuperación funcional de los pacientes con cáncer para que puedan retomar sus terapias oncológicas dirigidas en un tiempo que puede variar con base en el tipo de cáncer a tratar y lo invasivo que haya resultado el tratamiento quirúrgico (desde un mínimo de 32 a 42 días).27
Esta guía pretende ofrecer recomendaciones en el manejo anestésico en el paciente con cáncer de acuerdo con un nivel de evidencia alto y así influir positivamente en ello. Empezaremos por revisar las ventajas y desventajas de los anestésicos más utilizados.
La lidocaína intravenosa es uno de los anestésicos más se emplean en el paciente con cáncer debido a la evidencia de propiedades antinflamatorias.29 En un ECA (ensayo controlado aleatorizado) en pacientes con cáncer de páncreas que se sometieron a pancreatectomía, se administró lidocaína intravenosa durante el intraoperatorio a razón de 2 mg/kg/h después de un bolo de 1.5mg/kg. Los resultados mostraron que los NET (trampas extracelulares de neutrófilos) disminuyeron y se redujo el consumo de opioides, pero no hubo efecto en la sobrevida o período libre de enfermedad.30
En otro ECA de pacientes con cáncer de mama que evaluaron la recurrencia con técnica anestésica regional paravertebral más propofol vs. anestesia general a base de sevoflurano + opioide se demostró diferencia en disminución de la recurrencia.31
Al respecto de propofol, la mayoría de los estudios in vitro e in vivo reportan que presenta propiedades antimetastásicas y antinflamatorias.32 Rune P. y colaboradores encontraron mayor riesgo de recurrencia en pacientes con cáncer colorrectal con anestesia inhalada que con TIVA (propofol).33
En un ECA de pacientes con cáncer colorrectal, la anestesia basada en propofol, vs. halogenado, no mostró diferencias en la circulación de células del sistema inmunológico.34 En un ensayo más, pero en pacientes con cáncer pulmonar manejados con anestesia general + bloqueo peridural, sólo disminuyó los puntajes de dolor, pero no en recurrencia.35
Los opioides forman parte del manejo anestésico y son potentes para control del dolor, por tanto se utilizan en Oncología, pero no existe evidencia que promueva o disminuya la recurrencia en el paciente con cáncer.36
La dexmedetomidina atenúa la respuesta al estrés quirúrgico37, por lo que se utiliza en algunas cirugías, excepto en cirugía de mama ya que en estudios in vivo se ha encontrado que puede promover la recurrencia.38
Como se puede observar, la evidencia disponible sugiere que la recurrencia del cáncer no resulta afectada significativamente por la anestesia regional ni por la anestesia intravenosa total o volátil; aun así se requieren más estudios aleatorizados.
La QT, RT, hormonoterapia y la cirugía curativa o paliativa son técnicas para el tratamiento del cáncer con diferentes efectos secundarios en el cuerpo humano.39
Quimioterapia
La QT puede ser neoadyuvante (antes de la cirugía), adyuvante (durante o después de la cirugía) y paliativa (para mejorar la calidad de vida).
Muchos medicamentos de QT son agentes antiproliferativos que se dirigen a las células cancerosas que se dividen rápidamente. Sin embargo, las células en división no malignas también resultan afectadas. En consecuencia, la toxicidad de las drogas deriva en efectos agudos y a largo plazo en el organismo humano, por lo que es de suma importancia que los anestesiólogos mantengan en condiciones óptimas a los pacientes con antecedentes de cáncer para la anestesia y la cirugía.40-42
Puntos clave a considerar
La peor complicación de la terapia con bleomicina es un daño pulmonar subagudo que puede derivar en fibrosis pulmonar. La progresión rápida depende de la asociación con oxigenoterapia de alta concentración inspirada.
Por lo tanto, se deben usar concentraciones de oxígeno reducidas durante la anestesia y después de la operación. La saturación de oxígeno periférico debe estar entre 88% y 92%. Además, se debe elegir ventilación con presión positiva al final de la expiración (PEEP, positive end-expiratory pressure) bajo parámetros de protección pulmonar.40,42
Las antraciclinas (doxorrubicina) son los fármacos que contribuyen a la cardiotoxicidad; de modo que es necesaria una valoración preoperatoria adecuada (ecocardiograma) en conjunto con una monitorización cardiaca apropiada.40,42
Los agentes de quimioterapia a base de platino (cisplatino, carboplatino y oxaliplatino) son nefrotóxicos, por lo que pueden causar LRA (lesión renal aguda). La optimización cuidadosa de líquidos y la dosificación de analgésicos, en específico antinflamatorios no esteroideos (AINE), son imprescindibles en el perioperatorio.42
La QT por sí sola afecta la médula ósea y las células sanguíneas periféricas, lo cual deriva en mielosupresión, que suele ser reversible dentro de las seis semanas posteriores al cese de la misma.
La anemia como respuesta secundaria a enfermedad maligna es curable, sin transfusión de sangre en un período de dos a tres semanas. No obstante, la transfusión de hemoderivados puede ser necesaria en los casos de anemia por mielosupresión y cirugía urgente.40-43
Cómo evaluar la cardiotoxicidad
Con base en el deterioro de la fracción de expulsión del ventrículo izquierdo (FEVI), se puede clasificar la cardiotoxicidad de la siguiente manera44,45:
- Grado I. Reducción de la FEVI del 10 al 20% con respecto a la basal.
- Grado II. Reducción mayor del 20% o descenso por debajo de lo normal.
- Grado III. Aparición de síntomas de insuficiencia cardíaca congestiva.
La American Society of Echocardiography y la European Association of Cardiovascular Imaging utilizan el 53% como límite normal.46,47
Una elevación de la troponina I sérica detectada con ensayos de troponina I de alta sensibilidad en pacientes que reciben antraciclinas y/o trastuzumab predice la disfunción VI posterior.48
La combinación de troponina de alta sensibilidad con GLS (strain longitudinal global) podría proporcionar mayor sensibilidad (93%) y valor predictivo negativo (91%) para predecir cardiotoxicidad futura.49-51
Radioterapia
La apoptosis celular inducida por daños en el ADN por RT libera alarminas, que activan el sistema inmunitario innato y adaptativo, lo cual resulta en una respuesta proinflamatoria que compromete el endotelio vascular.52
Las dosis superiores a 10 Gy por fracción causan daño considerable, aumentan la permeabilidad vascular, y provocan mayor riesgo de trombosis debido a la agregación plaquetaria y la fibrosis.52
La quimiorradiación para los cánceres de esófago, mama, pulmón y cabeza y cuello provoca daños en los tejidos mediante la producción de radicales libres de oxígeno. En consecuencia, pueden causar miocarditis, neumonitis, fibrosis pulmonar y una vía aérea difícil, lo cual implica un desafío del manejo de pacientes con cáncer de cabeza y cuello para los anestesiólogos.44,47
Dentro de los principales cambios patológicos cardiovasculares se identifican la pericarditis constrictiva aguda o crónica, miocardiopatía restrictiva, enfermedad valvular y coronaria, arritmias, enfermedad de las arterias carótidas y otras enfermedades vasculares.
Dichas condiciones clínicas constituyen un reto durante el transoperatorio por necesidad del uso de accesos vasculares centrales y manejo hemodinámico. El daño depende de la dosis de radiación, el volumen y la región afectada del corazón, la técnica de radiación empleada, la enfermedad cardiovascular preexistente y la toxicidad cardiovascular previa (Tabla 3).53,54
| Tabla 3. Efectos tóxicos de la radioterapia | |||
|---|---|---|---|
| Cardiovascular | Pulmonar | Cabeza y cuello | Otro |
|
|
|
|
| Modificado de Groenewold MD, 2022.52 | |||
Véase la Tabla 4 como resumen del manejo preoperatorio e intraoperatorio en pacientes tratados con QT, RT o inmunoterapia.
| Tabla 4. Manejo preoperatorio e intraoperatorio en pacientes tratados con quimioterapia, inmunoterapia o radioterapia | ||
|---|---|---|
| Sistemas de órganos | Consideraciones preoperatorias | Consideraciones intraoperatorias |
| Cardíaco | ECG de 12 derivaciones, intervalo QT, ecocardiografía, pruebas de laboratorio: troponina plasmática, NT - proBNP. | ECG de 5 derivaciones. Evitar fármacos que prolonguen el intervalo QT. |
| Pulmonar | SpO2 basal, pruebas de función pulmonar, tomografía computarizada. | Ventilación con protección pulmonar. |
| Hígado | Prueba de laboratorio: transaminasas hepáticas, INR. | |
| Riñón | Exámenes de laboratorio: urea, creatinina, tasa de filtración glomerular | Gestión equilibrada de fluidos |
| Endocrinopatías (inmunoterapia) | Exámenes de laboratorio: TSH, T4 libre, HbA 1C, ACTH, cortisol, balance electrolítico, consulta con endocrinólogo. | Fluidoterapia dirigida por objetivos. Monitoreo de electrolitos. |
| Cabeza y cuello (radioterapia) | Gestión y planificación de la vía aérea | Manejo de vía aérea difícil |
| Otros | Pruebas de laboratorio: pruebas básicas, albúmina, aumento del riesgo de trombosis. | Interacción potencial con fármacos anticoagulantes |
| ECG: electrocardiograma; NT-proBNP: péptido natriurético tipo B N-terminal; SoO2: saturación de oxígeno; INR, razón internacional normalizada; TSH: hormona estimulante de la tiroides; HbA 1 C: prueba de hemoglobina glicosilada; ACTH: hormona adrenocorticotrópica. Modificado de Groenewold MD, 2022.52 | ||
La anemia se define como la presencia de niveles de hemoglobina < 13 g/dL en hombres y 12 g/dL en mujeres.
Se estima que 39% de pacientes oncológicos presenta anemia al diagnóstico de alguna patología oncológica y que hasta 67% de los pacientes la desarrollará durante el tratamiento con QT o RT.55
La etiología de la anemia es multifactorial; puede ser secundaria a pérdidas crónicas como en caso de cánceres gastrointestinales, ginecológicos y genitourinarios, por disfunciones de las líneas celulares como en las leucemias, la asociada a RT y/o QT, que pueden ser inmunosupresores de la médula en distintos grados, por deficiencia vitamínica en pacientes anoréxicos, incluso algunos pacientes tienen anemia sin una causa identificable.
El mecanismo fisiopatológico por el cual se presenta es complejo, entre las teorías más aceptadas tenemos que las células cancerígenas, al promover un ambiente proinflamatorio, activan citocinas como el interferón-γ, la interleucina-1 y factor de necrosis tisular que, a su vez, son capaces de suprimir la producción endógena de eritropoyetina, deterioran la utilización del hierro y reducen la proliferación de precursores eritroides, lo cual inhibe la eritropoyesis.56
La importancia y el alcance de la anemia en el paciente oncológico son fundamentales, puesto que la anemia está asociada directamente con la supervivencia y mortalidad a mediano y largo plazo.
La hipoxia secundaria a anemia puede generar resistencia a las terapias de radiación y QT, afectar negativamente la calidad de vida, limitar la capacidad funcional y la capacidad para trabajar.57
Las transfusiones sanguíneas no están exentas de complicaciones, tales como la reacción transfusional hemolítica aguda o retardada, lesión pulmonar aguda relacionada con transfusiones (TRALI), enfermedad de injerto contra huésped, reacciones transfusionales febriles no hemolíticas, incremento en metástasis etc. Por ello, diversas guías han basado sus esfuerzos en optimizar al paciente de forma preoperatoria con la finalidad de disminuir el riesgo de transfusión transoperatoria.58
En consecuencia, el diagnóstico y clasificación de la anemia es vital. Se ha propuesto un algoritmo facilitado para la intervención objetiva e individualizada de la anemia en el contexto del paciente oncológico preoperatorio y se sugiere valorar al paciente con al menos cuatro semanas de antelación para abordar el manejo y dar la optimización necesaria (Figura 2).18,59
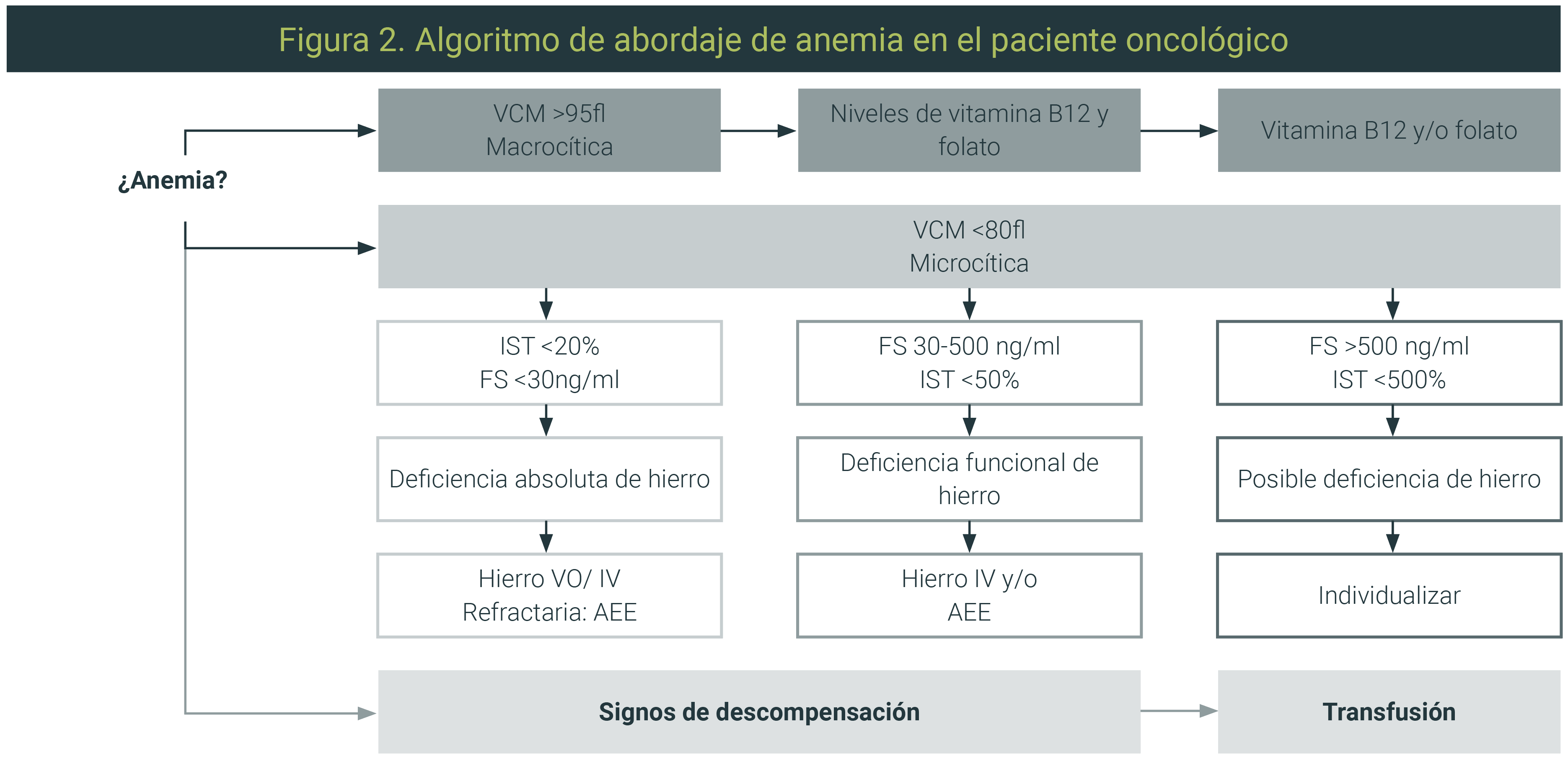
Modificado por Linda Guillén-Huerta (Anestesia Oncológica del Instituto Nacional de Cancerología) de Aapro M, 2018.59
El hierro se puede administrar por vía oral o intravenosa. La forma oral suele tener absorción intestinal irregular, sobre todo si se administra junto con inhibidores de la bomba de protones, incluso se le ha asociado con intolerancia, diarrea, vómitos y dolor abdominal.
Las presentaciones intravenosas suelen tener efectos más rápidos (1-2 semanas), incrementar los reticulocitos a partir de los 6-7 días y lograr subir la Hb hasta 0.8g/dl en una semana. La forma de hierro carboximaltosa puede ser administrada en 15 minutos; y está indicada en pacientes con mala absorción intestinal y falta de respuesta al tratamiento oral.
Los agentes estimulantes de la eritropoyesis están recomendados en pacientes con tumores sólidos y anemia sintomática bajo tratamiento con QT o quimiorradioterapia con Hb <10 g/dl o anemia asintomática con niveles de Hb < 8 g/dl. Tras corrección de los niveles de hierro no deben utilizarse en pacientes que no estén recibiendo QT.59
El manejo de la anemia debe ser estudiado minuciosamente con la finalidad de no aplazar eventos quirúrgicos, dar un tratamiento adecuado y permitir la optimización máxima del paciente para disminuir el riesgo de transfusión transoperatoria.
Fluidoterapia
El objetivo de la fluidoterapia es mantener y/o restaurar la perfusión tisular. Los procedimientos quirúrgicos condicionan pérdidas adicionales de líquidos y, en muchos casos, se agregan a deshidratación prexistente, secundaria a tiempos de ayuno prolongados.17
La tasa de distribución de las distintas soluciones utilizadas para este fin dependerá de la anestesia general, estrés, estado de deshidratación, edad y la presión arterial.17,60,61
La cinética de los líquidos administrados difiere del paciente despierto a la de aquél que se encuentra bajo anestesia general: entre el 5% y el 10% del volumen infundido se excreta dentro de las primeras dos horas durante la anestesia y el procedimiento quirúrgico, mientras que, en el paciente despierto, la eliminación oscila entre el 75% y 90%.60
Es importante reconocer el momento adecuado para la administración de líquidos, así como la cantidad y características de éstos. Recordemos que algunas de las causas de daño a la integridad de la glicocálix endotelial son la cirugía abdominal mayor y la infusión rápida de líquido, especialmente NaCl 0.9% (velocidad de infusión > a 10 ml/min), lo cual aumenta la permeabilidad transcapilar y contribuye al desarrollo de hipovolemia, edema intersticial y disfunción orgánica.60,61
Terapia guiada por objetivos
Las variables dinámicas como la variación de la presión del pulso (VPP), la variación del volumen sistólico (VVS), el ultrasonido y el análisis de variación la onda pletismográfica (VPI) proporcionan información útil adicional para guiar la terapia de fluidos. Se ha demostrado una mayor utilidad en caso de hemorragia, función cardíaca deficiente o vasodilatación secundaria a fármacos, analgesia/anestesia regional o sepsis.17
El ensayo multicéntrico FEDORA y el INPRESS mostraron reducción significativa de las complicaciones y la duración de la estancia con la implementación de una estrategia hemodinámica dirigida por objetivos. El segundo, además, mostró reducción de complicaciones en el grupo al que optimizó la volemia, seguido de la inclusión de un vasopresor para mantener la presión arterial en metas (Figura 3).61
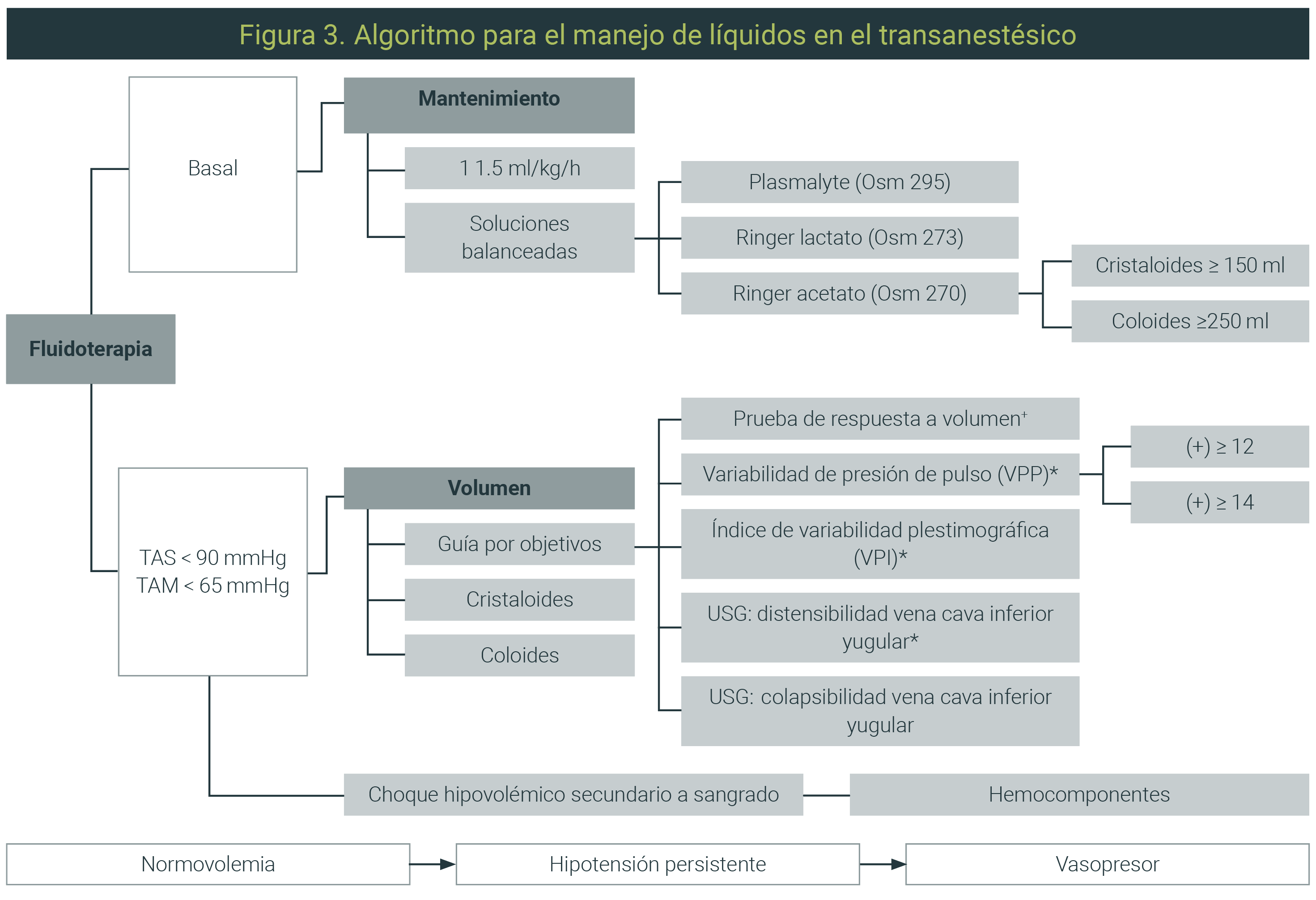
Realizado por Karla María Lara-Cuevas; Anestesia Oncológica del Instituto Nacional de Cancerología.
Transfusión
La transfusión de componentes sanguíneos se lleva a cabo dos contextos: ante hemorragia mayor o en anemia crónica con el objetivo de mejorar el suministro de oxígeno a los órganos y tejidos.55,62,63
Si bien es prioritario restablecer la perfusión tisular óptima, es importante considerar que la transfusión también se asociada con riesgos como sobrecarga de líquidos, inmunosupresión y efectos inmunomoduladores que pueden aumentar las complicaciones infecciosas y el potencial riesgo de recurrencia del cáncer.64,65
Los mecanismos relacionados con la recurrencia se dividen en dos grupos:
- TRIM (transfusion‑related immunomodulation). Regulación a la baja de la inmunidad celular y del sistema de vigilancia mediado por leucocitos residuales, citocinas, productos degradados de glóbulos rojos por almacenamiento y otras micropartículas derivadas de la célula. La respuesta del huésped es liberar factores de crecimiento como TGF-b, IL-10, inhibición de IL-2 y supresión de la actividad citotóxica de las células T NK.64
- No TRIM. Efectos de factores de crecimiento, citocinas y hemoglobina liberada de los glóbulos rojos almacenados. Una vez que los eritrocitos trasfundidos se ponen en contacto con el óxido nítrico hay mayor consumo de este vasodilatador, lesión vascular y angiogénesis.64
Al momento de decidir transfundir es importante sólo administrar los hemocomponentes necesarios (Figura 4) porque además se asocia con los siguientes efectos adversos:
- Inmediatos (24 horas). Reacción hemolítica aguda, anafiláctica, lesión pulmonar relacionada con la trasfusión (TRALI), sobrecarga de volumen, anemia hemolítica no inmune, hipotensión y fiebre.65
- Tardíos (>24 horas). Reacción transfusional hemolítica tardía, enfermedad injerto contra huésped relacionado con la transfusión, hemosiderosis transfusional.65
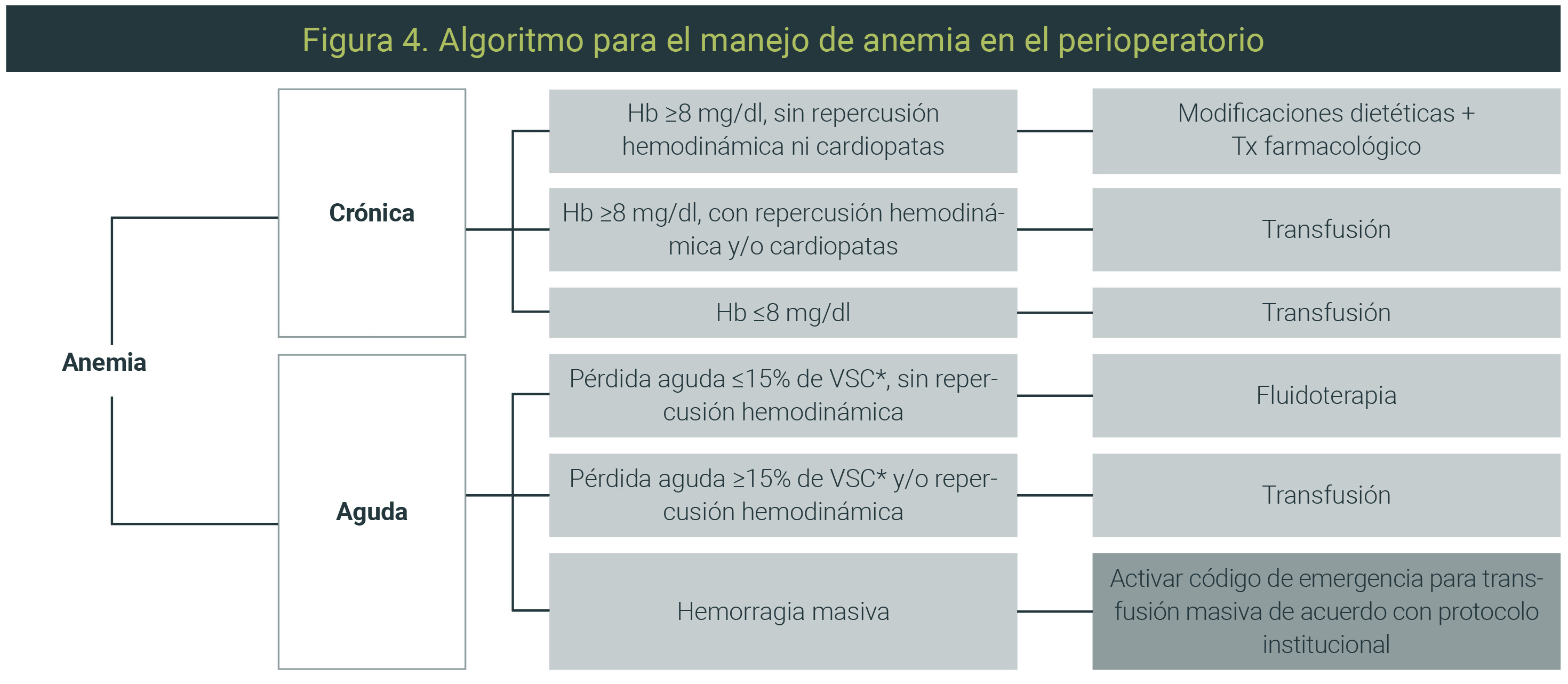
Figura realizada por Karla María Lara-Cuevas; Anestesia Oncológica del Instituto Nacional de Cancerología.
La intubación y la ventilación difícil con mascarilla están estrechamente asociadas. El mayor desafío y peor escenario en vía aérea es «no se puede intubar y no se puede ventilar».66 En los pacientes oncológicos representan un reto por las situaciones especiales a enfrentar.67
Particularidades de la vía aérea en Oncología
La evaluación perioperatoria integral de un paciente que se somete a una cirugía de cáncer de cabeza y cuello debe incluir los pasos67 que a continuación se describen.
Enfermedad primaria frente a recurrente
Para una neoplasia primaria, el efecto de masa y el cambio anatómico, para una enfermedad recurrente, el impacto sobre el tejido tisular de la vía aérea debido a las terapias anteriores contra el cáncer.67
Estadio y ubicación del cáncer
La enfermedad orofaríngea rara vez causa obstrucción significativa en la vía de intubación, pero un cáncer ubicado en la hipofaringe o la laringe tendrá más probabilidades de causar obstrucción no sólo del flujo de aire, sino también de la vía de intubación.67
Radiación de cabeza y cuello
Los problemas que afectan el manejo de la vía aérea incluyen edema agudo de las vías respiratorias (cambio temprano), edema linfático y/o grosor del tejido difuso, así como fibrosis tisular (cambio en etapas posteriores).
La pérdida de la distensibilidad tisular después de la fibrosis desafía la exposición de la glotis y aumenta el fracaso de la laringoscopia. Hay que entender que estos problemas no se pueden resolver mediante la administración de un relajante neuromuscular.67,68
Cambios anatómicos de la cirugía anterior
Experiencias clínicas indican que un sitio quirúrgico bien curado rara vez frena la ventilación de la mascarilla facial y el rendimiento de la intubación traqueal.67-69
Incapacidad de mantener la vía aérea permeable inmediatamente después de la cirugía
La manipulación de la vía aérea y la presión añadida al colgajo durante el rescate de la vía aérea pueden provocar daño o fracaso del colgajo.67
Abordaje de la vía aérea no prevista
El manejo exitoso de la vía aérea sigue siendo una competencia fundamental para el anestesiólogo, ya que se considera que dicho especialista es el más calificado para el manejo de la vía aérea. Se recomienda al lector revisar la actualización a las guías American Society of Anesthesiologists Practice Guidelines for Management of the Difficult Airway (2022).70,71
Protocolo VORTEX
El protocolo VORTEX se desarrolló con la finalidad de evitar errores de fijación en una determinada técnica o tarea, mejorar la toma de decisiones y promover el trabajo en equipo.71
La expectativa es que la herramienta impulse a un equipo clínico con las opciones para el manejo de las vías respiratorias y facilite la conciencia situacional compartida.72
La herramienta de implementación de VORTEX se basa en la premisa de que sólo hay tres «líneas de vida» de las vías respiratorias superiores («técnicas no quirúrgicas») mediante las cuales se puede establecer y confirmar el suministro de oxígeno alveolar: tubo endotraqueal (ETT), una vía aérea supraglótica (SGA) o incluso una mascarilla facial (FM).
El mejor esfuerzo en cualquiera de las tres líneas de vida en el manejo de la vía área sin poder confirmar la adecuada entrega de oxígeno alveolar, debe dar pauta al abandono de más intentos de esa línea de vida y centrarse, en su lugar, en optimizar una de las alternativas restantes.73
Cualquiera que sea el algoritmo que se quiera seguir, la finalidad es lograr el adecuado manejo de la vía área en el menor tiempo posible con algunas de las herramientas antes mencionadas. Desde luego, se debe destacar que el trabajo en equipo y el reconocimiento de las limitaciones de cada operador será la clave del éxito en el manejo de la vía área difícil no anticipada.
Intubación del paciente despierto
Una estrategia para el manejo de la vía aérea difícil es necesaria cuando se predice que la ventilación con mascarilla facial, colocación o ventilación con dispositivo supraglótico, la intubación traqueal o la inserción de una vía aérea frontal del cuello sean difíciles. Es por ello que la asociación del manejo de vía aérea difícil, DAS (Difficult Airway Society) recomienda lo siguiente74:
- La intubación traqueal en un paciente despierto debe considerarse en presencia de predictores de una vía aérea difícil.
- Se recomienda la realización de una lista de verificación, antes y durante la realización de la intubación traqueal.
- El oxígeno suplementario siempre debe administrarse durante la intubación traqueal.
- Se debe establecer y probar la topicalización efectiva. La dosis máxima de lidocaína no debe exceder 9 mg/kg de peso corporal magro.
- El uso cauteloso de sedación mínima puede ser beneficioso. Lo ideal es que sea un profesional quien lo administre, aparte del que maneja la vía aérea. La sedación no debe usarse como sustituto de la topicalización inadecuada de la vía aérea.
- El número de intentos debe limitarse a tres, con un intento más por parte de un operador más experimentado (3 + 1).
- La anestesia sólo debe inducirse después de que una verificación de dos puntos (confirmación visual y capnografía) haya confirmado la posición correcta del tubo traqueal.
- Todos los Departamentos deben apoyar a los anestesiólogos para alcanzar la competencia y mantener las habilidades en la intubación traqueal.
A pesar de los avances en los tratamientos contra el cáncer, la cirugía sigue siendo una de las terapias más importantes para los tumores sólidos. Desafortunadamente, promueve la angiogénesis, desprendimiento de células cancerosas en la circulación y suprime la inmunidad antitumoral. En conjunto, esto aumenta el riesgo de metástasis tumorales, crecimiento de micrometástasis acelerada y recurrencia del cáncer.
Después de la cirugía, las reacciones locales y sistémicas contribuyen al desarrollo de un estado proinflamatorio inicial, seguido de una fase de inmunosupresión durante la cual se reduce la capacidad del cuerpo para eliminar las células cancerosas.75-77
La anestesia regional, utilizada sola o en combinación con anestesia general, reduce la respuesta al estrés perioperatorio, el dolor perioperatorio y, por lo tanto, también los requisitos de opioides perioperatorios. Si la anestesia regional tiene una influencia directa en la recurrencia del cáncer es menos claro.
Originalmente se teorizó que la anestesia regional podría mejorar los resultados oncológicos después de la cirugía del cáncer, ya que disminuye la respuesta neuroendocrina al trauma quirúrgico, el consumo de opioides y el uso de anestésicos volátiles.
La analgesia regional induce una acción antinflamatoria sistemática, suprime la proliferación y la migración de células cancerosas, y puede ayudar a prevenir la metástasis del cáncer original.75,76
Varias revisiones sistemáticas han abordado este problema, pero no encontraron ningún efecto protector significativo de la analgesia regional. Múltiples factores clínicos y del paciente pueden influir en el efecto de la anestesia regional sobre la recurrencia del cáncer, lo que deriva en una posible heterogeneidad en diferentes poblaciones. Ello significa que algunos pacientes pueden beneficiarse más de la anestesia regional.
Un metanálisis de tres estudios controlados aleatorizados y 34 estudios de cohorte (64,691 pacientes incluidos) mostraron que la supervivencia general (SG) y el período libre de recurrencia fue similar e independiente del uso de anestesia regional, pero el estudio señala que fue realizado en pacientes con cáncer en estadios avanzados.76
La estadificación desempeña un papel fundamental en la batalla contra el cáncer porque proporciona el punto de referencia, los estándares críticos para definir el pronóstico, la probabilidad de superar el cáncer una vez diagnosticado y determina el mejor enfoque de tratamiento para controlar la enfermedad.
Anestésicos locales
El efecto de los anestésicos locales sobre el crecimiento tumoral se ha estudiado en varios estudios in vitro y en animales, pero faltan estudios clínicos.
Clásicamente se acepta que los canales de sodio tienen un papel importante en la célula cancerosa (en la movilidad celular, actividad endocítica - exocítica, regulación del Ph y en la invasividad).
La expresión de subunidades de canales de sodio dependientes de voltaje (NaVα y NaV β) se encuentra alterada en varios tipos de cáncer. Hay pruebas claras de que la expresión anormal de NaV (p. ej. NaV1.5, NaV1.6 o NaV1.7) ocurre durante la carcinogénesis y se asocia con la progresión del cáncer hacia estados metastásicos.78,79
Por lo tanto, la inhibición de NaVα en las células cancerosas representa una nueva estrategia contra el cáncer. El canal NaVβ, por su parte, también desempeña un papel importante en la biología de las células cancerosas y en la progresión del cáncer, ya que actúa como subunidades auxiliares de NaVα. Sin embargo, no ejerce una actividad registrable per se.79
Se ha promovido la administración clínica de lidocaína intravenosa durante la anestesia porque se ha observado que se asocia con menor uso de opioides, menor incidencia de náuseas y vómitos, y una recuperación más rápida del íleo postoperatorio. Además, la lidocaína tiene una potente actividad antinflamatoria mediante la modulación de IL-6, IL-8, leucotrienos y leucocitos polimorfonucleares.78
Varios estudios y ensayos in vitro en ratones han demostrado el potencial anticancerígeno de la lidocaína y otros anestésicos locales, pero a concentraciones alcanzadas por anestesia regional, ninguno de los anestésicos locales afectaría la viabilidad o la migración celular.79,82
Los anestésicos locales podrían tener un efecto benéfico, como se observa en estudios en animales e in vitro. Sin embargo, los estudios clínicos prospectivos cuestionan fuertemente tal efecto.
Bloqueo epidural ecoguiado
Se sabe que la analgesia epidural tiene un control superior del dolor perioperatorio sobre la analgesia opioide. Es un componente esencial de recuperación mejorada después de la cirugía y en anestesia oncológica es pilar fundamental dentro del manejo multimodal.80
No obstante, dentro de las desventajas se encuentra la dificultad para poder sentir la pérdida de resistencia con una sola mano y en ocasiones la necesidad de un segundo operador en el momento del procedimiento (Figura 5).80 El sitio de punción se encuentra dentro del complejo posterior.
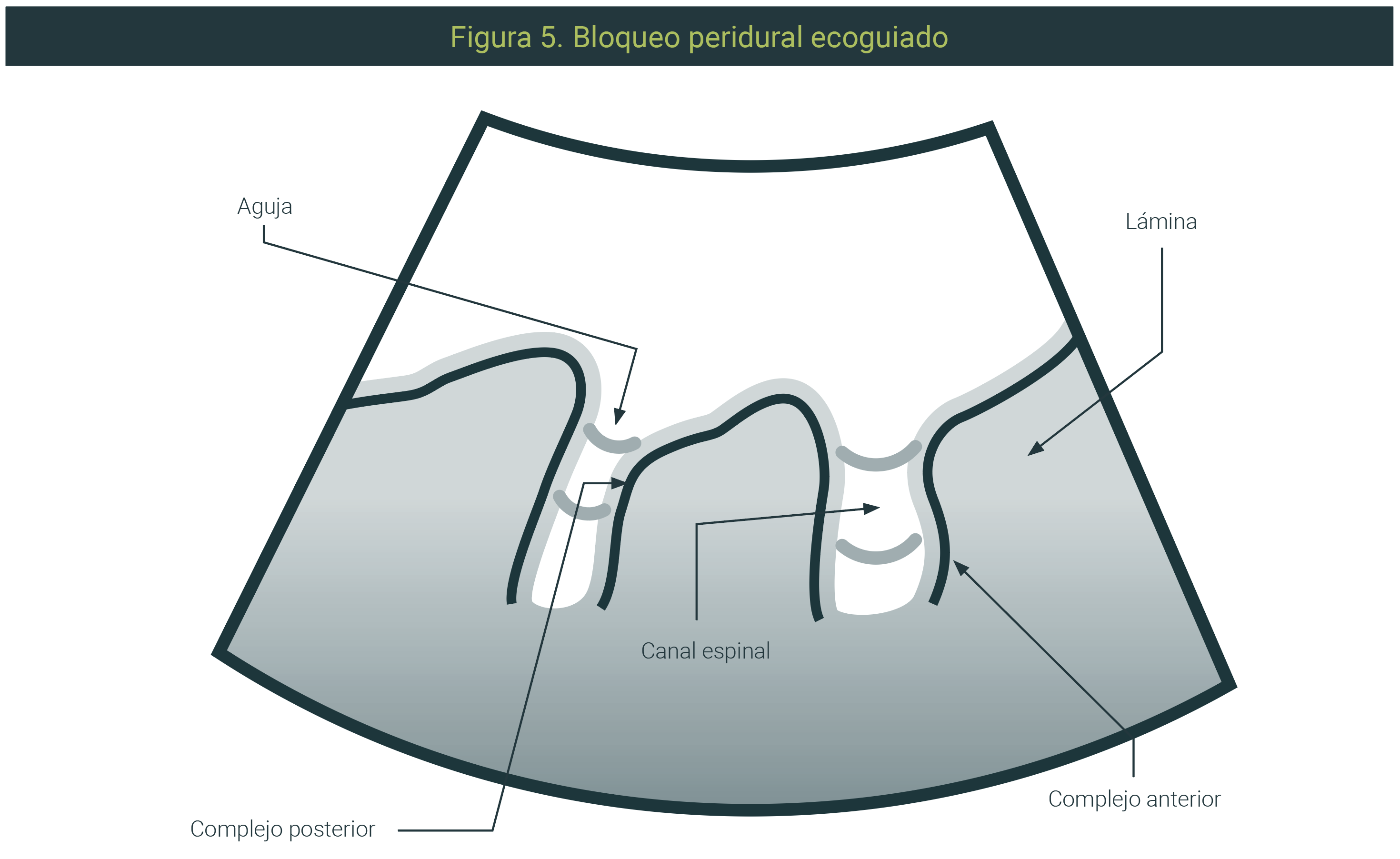
En lo que respecta a la sonoanatomía es importante reconocer el complejo posterior (complejo ligamentum amarillo-dura) y el complejo anterior (el ligamento longitudinal posterior, la superficie posterior del cuerpo vertebral y el disco intervertebral).81
A pesar de que existen numerosos estudios que intentan demostrar la utilidad de la anestesia regional y la progresión del cáncer, hacen falta más estudios que nos permitan concluir su verdadera relación. Aún es cuestionable si la anestesia regional puede ayudar a prevenir la recurrencia de la enfermedad en pacientes con cáncer.
La definición original de dolor por la IASP (International Association on the Study of Pain, Asociación Internacional para el Estudio del Dolor) fue revisada por un grupo de trabajo de expertos en 2020 y actualmente se define como «una experiencia sensorial y emocional desagradable asociada o similar a la asociada a una lesión tisular real o potencial».82
El dolor agudo postoperatorio hace referencia al dolor que aparece en el paciente tras una intervención quirúrgica, por su enfermedad previa, el procedimiento quirúrgico o la combinación de la enfermedad y el procedimiento realizado, contracturas musculares o distensión vesical e intestinal.83
El dolor o esta experiencia después de procedimientos oncológicos importantes puede ser intenso y muchas veces difícil de tratar, ya que los pacientes pueden presentarse en el quirófano con varias afecciones, incluido el dolor preoperatorio, tolerancia a los opioides y contraindicaciones para los analgésicos no opioides o la anestesia regional.
El dolor postoperatorio tratado de manera inadecuada se asocia con la activación del sistema simpático, complicaciones postoperatorias, gran uso de opiáceos perioperatorios y mayor riesgo de desarrollar dolor postoperatorio persistente (mayor a tres meses). Además, se ha teorizado que el dolor mal tratado se asocia con la recurrencia del cáncer y una supervivencia reducida.84
Intervenciones perioperatorias
Si bien existen diferentes guías de carácter internacional, los trabajos publicados en 2016 de la American Pain Society (APS) que recomiendan estrategias de reducción del dolor quirúrgico que inician en el preoperatorio y continúan hasta el egreso y días después son altamente recomendadas.
De igual forma, el esfuerzo del grupo europeo PROSPECT (Procedure Specific Postoperative Pain Magement), a diferencia de otras, es una iniciativa vigente basada en evidencia científica, mediante un abordaje perioperatorio.
Actualmente, en varios hospitales de México (entre los que figura el nuestro) se ha sumado un esfuerzo similar a PROSPECT desde la Universidad de Jena, Alemania PAIN OUT que, si bien es un registro internacional de dolor postoperatorio, funciona como un sistema de gestión mediante el benchmarking para implementar mejoras respecto a las terapéuticas frente al dolor postoperatorio. Ello ha dado lugar a recomendaciones basadas en evidencia de acuerdo con el evento quirúrgico a realizar, mismas que pueden consultarse fácilmente en su página oficial.85
Recomendaciones
De acuerdo con Garduño-López AL y cols., las pautas preoperatorias recomendadas son:
- educación
- reducción del dolor prexistente
- planificación del abordaje analgésico individualizado
- reducción oportuna de alteraciones psicológicas ya que se ha demostrado que la angustia, ansiedad o catastrofización influyen en la intensidad y la percepción del dolor postoperatorio85
En el intraoperatorio y en el postoperatorio se recomienda ampliamente hacer uso de la analgesia multimodal, que consiste en una combinación racional de fármacos con diferentes mecanismos de acción sobre el proceso de nocicepción por medio de técnicas neuroaxiales y regionales, terapias farmacológicas y terapias no farmacológicas.85
Puntos clave84
- Se recomienda la analgesia multimodal para proporcionar analgesia postoperatoria adecuada en pacientes con cáncer.
- El dolor preoperatorio se asocia con dolor persistente postoperatorio y uso de opioides.
- Los opioides siguen siendo el analgésico más fuerte disponible. Se indica un uso cuidadoso para evitar eventos adversos relacionados con los opioides.
- Los pacientes con eventos adversos del sistema nervioso central relacionados con las terapias contra el cáncer pueden ser más vulnerables a los efectos de los anestésicos y analgésicos.
Con el objetivo de lograr un mejor manejo perioperatorio de los pacientes con cáncer, prolongar la supervivencia global y libre de cáncer y disminuir las complicaciones postoperatorias se requiere de un manejo multidisciplinario donde la anestesia y los cuidados intensivos específicos de las cirugías oncológicas aporten conocimientos especializados.
La alta especialidad en oncoanestesia y los cuidados intensivos específicos de las cirugías oncológicas han permitido ampliar el conocimiento de las necesidades de pacientes con cáncer y lograr así un manejo anestésico con claros objetivos oncológicos. Se debe considerar la historia natural del cáncer, el estado nutricional y funcional actual, síntomas y problemas médicos generales agregados, así como los efectos de las terapias recibidas para lograr resultados más óptimos.
Agradecemos la coordinación y colaboración del Departamento de Anestesia Oncológica del Instituto Nacional de Cancerología y a los profesores de su Posgrado de Alta Especialidad en Medicina. Al pilar que representa la enseñanza en nuestro instituto y aquello que seguimos logrando al priorizar la Academia.
Los autores declaran no tener conflicto de interés.
| 1. | Sung H, Ferlay J, Siegel RL, Laversanne M, Soerjomataram I, Jemal A, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2021;71(3):209-49. |
| 2. | INEGI. Comunicado de prensa Núm. 591/22. 17 de octubre de 2022. Estadísticas a propósito del Día Internacional de la Lucha contra el cáncer de mama (19 de octubre) [Internet] [Consultado 3 de agosto, 2023]. Disponible en URL: https://www.inegi.org.mx/contenidos/saladeprensa/aproposito/2022/EAP_CANMAMA22.pdf |
| 3. | Jain P, Balkrishanan K, Nayak S, Gupta N, Shah S. Onco-anaesthesiology and palliative medicine: Opportunities and challenges. Indian J Anaesth. 2021;65(1):29-34. |
| 4. | Santander Ballestín S, Lanuza Bardaji A, Marco Continente C, Luesma Bartolomé MJ. Antitumor anesthetic strategy in the perioperatory period of the oncological patient: A review. Front Med (Lausanne). 2022;9:799355. |
| 5. | Thomas M. Advances in oncoanaesthesia and cancer pain. Cancer Treat Res Commun. 2021;29:100491. |
| 6. | Manzullo EF, Sahai SK, Weed HG. Preoperative evaluation and management of patients with cancer. Up To Date [Internet]. 2022. Available from URL: https://medilib.ir/uptodate/show/2793 |
| 7. | 7 Mille-Loera JE, Cuéllar-Guzmán LF, Alvarado-Pérez J, García-Velasco O, Fabela Barragán JA. Consideraciones anestésicas en el paciente con cáncer. Rev Mex Anestesiol. 2017;40(Supl 1):S132-S134. |
| 8. | Guillén Núñez MR, Plancarte Sánchez R, Hernández Porras BC, Juárez Lemus AM, Sámano García M, González Cázares AI. Oncoguía del manejo del dolor en cáncer 2023. Lat Am J Clin Sci Med Technol. 2023; 5:35-46. |
| 9. | Portenoy RK, Dhingra LK. Assessment of cancer pain. In: Drews RE, ed. UpToDate. Waltham, MA: UpToDate; 2013. |
| 10. | Sahai SK. Perioperative assessment of the cancer patient. Best Pract Res Clin Anaesthesiol. 2013;27(4):465-480. |
| 11. | Dubowitz JA, Sloan EK, Riedel BJ. Implicating anaesthesia and perioperative period in cancer recurrence and metastasis. Clin Exp Metastasis. 2018;35(4)347-58. |
| 12. | Ramesh HSJ, Pope D, Gennari R, Audisio RA. Optimising surgical management of elderly cancer patients. World J Surg Oncol. 2005;3(1):17. |
| 13. | Leun AA, McAlister FA, Rogers SO Jr, Pazo V, Wright A, Bates DW. Preoperative hyponatremia and perioperative complications. Arch Inter Med. 2012;172(19):1474-81. |
| 14. | Khorana AA, Francis CW, Culakova E, Kuderer NM, Lyman GH. Frequency, risk factors, and trends for venous thromboembolism among hospitalized cancer patients. Cancer 2007;110(10):2339-46. |
| 15. | Khorana AA. Venous thromboembolism prevention in cancer outpatients. J Natl Compr Can Netw. 2013;11(11):1431-8. |
| 16. | Fowler AJ, Ahmad T, Phull MK, Allard S, Gillies MA, Pearse RM. Meta-analysis of the association between preoperative anaemia and mortality after surgery. Br J Surg. 2015;102(11)-1314-24. |
| 17. | Scott MJ, Baldini G, Fearon KCH, Feldheiser A, Feldman LS, Gan TJ, et al. Enhanced recovery after surgery (ERAS) for gastrointestinal surgery, part 1: Pathophysiological considerations. Acta Anaesthesiol Scand. 2015;59(10):1212-31. |
| 18. | Feldheiser A, Aziz O, Baldini G, Cox BPBW, Fearon KCH, Feldman LS, et al. Enhanced recovery after surgery (ERAS) for gastrointestinal surgery, part 2: Consensus statement for anaesthesia practice. Acta Anaesthesiol Scand. 2016;60(3):289-334. |
| 19. | Gustafsson UO, Scott MJ, Hubner M, Nygren J, Demartines N, Francis N, et al. Guidelines for perioperative care in elective colorectal surgery: Enhanced Recovery After Surgery (ERAS®) Society recommendations: 2018. World J Surg. 2019;43(3):659-95. |
| 20. | Low DE, Allum W, De Manzoni G, Ferri L, Immanuel A, Kuppusamy M, et al. Guidelines for perioperative care in esophagectomy: Enhanced Recovery after Surgery (ERAS®) Society recommendations. World J Surg. 2019;42(2):299-330. |
| 21. | Nelson G, Bakkum-Gamez J, Kalogera E, Glaser G, Altman A, Meyer LA, et al. Guidelines for perioperative care in gynecologic/oncology: Enhanced Recovery after Surgery (ERAS) Society recommendations - 2019 update. Int J Gynecol Cancer. 2019;29(4):651-668. |
| 22. | Joliat GR, Kobayashi K, Hasegawa K, Thomson JE, Padbury R, Scott M, et al. Guidelines for perioperative care for liver surgery: Enhanced Recovery after Surgery (ERAS) Society recommendations 2022. World J Surg. 2023;47(1):11-34. |
| 23. | Batchelor TJ, Rasburn NJ, Abdelnour-Berchtold E, Brunelli A, Cerfolio RJ, Gonzalez M, et al. Guidelines for enhanced recovery after lung surgery: Recommendations of the Enhanced Recovery after Surgery (ERAS®) Society and the European Society of Thoracic Surgeons (ESTS). Eur J Cardiothorac Surg. 2019;55(1):91-115. |
| 24. | Melloul E, Lassen K, Roulin D, Grass F, Perinel J, Adham M, et al. Guidelines for perioperative care for pancreatoduodenectomy: Enhanced Recovery after Surgery (ERAS) recommendations 2019. World J Surg. 2020;44(7):2056-84. |
| 25. | Hübner M, Kusamura S, Villeneuve L, Al-Niaimi A, Alyami M, Balonov K, et al. Guidelines for Perioperative Care in Cytoreductive Surgery (CRS) with or without hyperthermic IntraPEritoneal chemotherapy (HIPEC): Enhanced Recovery after Surgery (ERAS®) Society recommendations — Part II: Postoperative management and special considerations. Eur J Surg Oncol. 2020;46(12):2311-23. |
| 26. | Hübner M, Kusamura S, Villeneuve L, Al-Niaimi A, Alyami M, Balonov K, et al. Guidelines for perioperative Care in Cytoreductive Surgery (CRS) with or without Hyperthermic IntraPEritoneal Chemotherapy (HIPEC): Enhanced Recovery after Surgery (ERAS®) Society recommendations — Part I: Preoperative and intraoperative management. Eur J Surg Oncol. 2020;46(12):2292-2310. |
| 27. | Onuma AE, Zhang H, Gil L, Huang H, Tsung A. Surgical stress promotes tumor progression: A focus on the impact of the immune response. J Clin Med. 2020;9(12):4096. |
| 28. | Kim BJ, Caudle AS, Gottumukkala V, Aloia TA. The impact of postoperative complications on a timely Return to Intended Oncologic Therapy (RIOT): The role of enhanced recovery in the cancer journey. Int Anesthesiol Clin. 2016;54(4):e33-46. |
| 29. | Cata JP, Guerra C, Soto G, Ramírez MF. Anesthesia options and the recurrence of cancer: What we know so far? Local Reg Anesth. 2020;13:57-72. |
| 30. | Zhang H, Qu M, Guo K, Wang Y, Gu J, Wu H, et al. Intraoperative lidocaine infusion in patients undergoing pancreatectomy for pancreatic cancer: A mechanistic, multicentre randomised clinical trial. Br J Anaesth. 2022;129(2):244-53. |
| 31. | Sessler DI, Pei L, Huang Y, Fleischmann E, Marhofer P, Kurz A, et al. Recurrence of breast cancer after regional or general anaesthesia: A randomised controlled trial. Lancet. 2019;394(10211):1807-15. |
| 32. | Wall T, Sherwin A, Ma D, Buggy DJ. Influence of perioperative anaesthetic and analgesic interventions on oncological outcomes: A narrative review. Br J Anaesth. 2019;123(2):135-50. |
| 33. | Hasselager RP, Hallas J, Gögenur I. Inhalation or total intravenous anaesthesia and recurrence after colorectal cancer surgery: A propensity score matched Danish registry-based study. Br J Anaesth. 2021;126(5):921-30. |
| 34. | Oh CS, Park HJ, Piao L, Sohn KM, Koh SE, Hwang DY, et al. Expression profiles of immune cells after propofol or sevoflurane anesthesia for colorectal cancer surgery: A prospective double-blind randomized trial. Anesthesiology. 2022;136(3):448-58. |
| 35. | Xu ZZ, Li HJ, Li MH, Huang SM, Li X, Liu QH, et al. Epidural anesthesia-analgesia and recurrence-free survival after lung cancer surgery: A randomized trial. Anesthesiology. 2021;135(3):419-32. |
| 36. | Sekandarzad MW, Doornebal C, Hollmann MW. Opiophobia in cancer biology- Justified? - The role of perioperative use of opioids in cancer recurrence. Curr Pharm Des. 2019;25(28):3020-27. |
| 37. | Wang K, Wu M, Xu J, Wu C, Zhang B, Wang G, et al. Effects of dexmedetomidine on perioperative stress, inflammation, and immune function: Systematic review and meta-analysis. Br J Anaesth. 2019;123(6):777-94. |
| 38. | Nair AS, Saifuddin MS, Naik V, Rayani BK. Dexmedetomidine in cancer surgeries: Present status and consequences with its use. Indian J Cancer. 2020;57(3):234-38. |
| 39. | Gudaitytė J, Dvylys D, Šimeliūnaitė I. Anaesthetic challenges in cancer patients: Current therapies and pain management. Acta Med Litu. 2017;24(2):121-27. |
| 40. | Sahai SK. Perioperative assessment of the cancer patient. Best Pract Res Clin Anaesthesiol. 2013;27(4):465-80. |
| 41. | Huitink JM, Teoh WHL. Current cancer therapies – A guide for perioperative physicians. Best Pract Res Clin Anaesthesiol. 2013;27(4): 481-92. |
| 42. | Allan N, Siller C, Breen A. Anaesthetic implications of chemotherapy. Contin Educ Anaesth Crit Care Pain [Internet]. 2012;12(2):52-6. Available from URL: https://www.e-safe-anaesthesia.org/e_library/11/Anaesthetic_implications_of_chemotherapy.pdf |
| 43. | Isbister JP. The three-pillar matrix of patient blood management – An overview. Best Pract Res Clin Anaesthesiol. 2013;27(1):69-84. |
| 44. | Consenso de diagnóstico, prevención y tratamiento de la cardiotoxicidad por tratamiento médico del cáncer. Versión resumida. Rev Argent Cardiol [Internet]. 2013;81(6):1-64. Disponible en URL: http://www.scielo.org.ar/scielo.php?script=sci_arttext&pid=S1850-37482013000600012 |
| 45. | Albini A, Pennesi G, Donatelli F, Cammarota R, De Flora S, Noonan DM. Cardiotoxicity of anticancer drugs: The need for cardio-oncology and cardio-oncological prevention. J Natl Cancer Inst. 2010;102(1):14-25. |
| 46. | López-Fernández T, Martín García A, Santaballa Beltrán A, Montero Luis A, García Sanz R, Mazón Ramos P, et al. Cardio-onco-hematologia en la práctica clínica. Documento de consenso y recomendaciones. Rev Esp Cardiol [Internet]. 2017;70(6):474-86. Disponible en URL: https://www.revespcardiol.org/es-cardio-onco-hematologia-practica-clinica-documento-deconsenso-articulo-S0300893216307552 |
| 47. | Plana JC, Galderisi M, Barac A, Ewer MS, Ky B, Scherrer-Crosbie M, et al. Expert consensus for multimodality imaging evaluation of adult patients during and after cancer therapy: A report from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. J Am Soc Echocardiogr. 2014;27(9):911-39. |
| 48. | Ky B, Putt M, Sawaya H, French B, Januzzi JL Jr, Sebag IA, et al. Early increases in multiple biomarkers predict subsequent cardiotoxicity in patients with breast cancer treated with doxorubicin, taxanes, and trastuzumab. J Am Coll Cardiol. 2014;63(8):809-16. |
| 49. | Sawaya H, Sebag IA, Plana JC, Januzzi JL, Ky B, Tan TC, et al. Assessment of echocardiography and biomarkers for the extended prediction of cardiotoxicity in patients treated with anthracyclines, taxanes, and trastuzumab. Circ Cardiovasc Imaging. 2012;5(5):596-603. |
| 50. | Ledwidge M, Gallagher J, Conlon C, Tallon E, O'Connell E, Dawkins I, et al. Natriuretic peptide- based screening and collaborative care for heart failure: The STOP-HF randomized trial. JAMA. 2013;310(1):66-74. |
| 51. | Thakur A, Witteles RM. Cancer therapy-induced left ventricular dysfunction: Interventions and prognosis. J Card Fail. 2014;20(3):155-58. |
| 52. | Groenewold MD, Olthof CG, Bosch DJ. Anaesthesia after neoadjuvant chemotherapy, immunotherapy or radiotherapy. BJA Educ. 2022;22(1):12-19. |
| 53. | Mansouri I, Allodji RS, Hill C, El-Fayech C, Pein F, Diallo S, et al. The role of irradiated heart and left ventricular volumes in heart failure occurrence after childhood cancer. Eur J Heart Fail. 2019;21(4):509-18. |
| 54. | van der Veen SJ, Ghobadi G, de Boer RA, Faber H, Cannon MV, Nagle PW, et al. ACE inhibition attenuates radiation-induced cardiopulmonary damage. Radiother Oncol. 2015;114(1):96-103. |
| 55. | Escobar Álvarez Y, de Las Peñas Bataller R, Perez Altozano J, Ros Martínez S, Sabino Álvarez A, Blasco Cordellat A, et al. SEOM clinical guidelines for anaemia treatment in cancer patients (2020). Clin Transl Oncol. 2021;23(5):931-9. |
| 56. | Abdel-Razeq H, Hashem H. Recent update in the pathogenesis and treatment of chemotherapy and cancer induced anemia. Crit Rev Oncol Hematol. 2020;145:102837. |
| 57. | Gilreath JA, Rodgers GM. How I treat cancer-associated anemia. Blood. 2020;136(7):801-13. |
| 58. | Anand S, Burkenroad A, Glaspy J. Workup of anemia in cancer. Clin Adv Hematol Oncol. 2020;18(10):640-646. |
| 59. | Aapro M, Beguin Y, Bokemeyer C, Dicato M, Gascón P, Glaspy J, et al. Management of anaemia and iron deficiency in patients with cancer: ESMO Clinical Practice Guidelines. Ann Oncol. 2018;29(Suppl-4):iv96-110. |
| 60. | Kang D, Yoo KY. Fluid management in perioperative and critically ill patients. Acute Crit Care. 2019;34(4):235-45. |
| 61. | Miller TE, Myles PS. Perioperative fluid therapy for major surgery. Anesthesiology. 2019;130(5):825-32. |
| 62. | Phan TD, Uda Y, Peyton PJ, Kluger R, Myles PS. Effect of fluid strategy on stroke volume, cardiac output, and fluid responsiveness in adult patients undergoing major abdominal surgery: A sub-study of the Restrictive vs Liberal Fluid Therapy in Major Abdominal Surgery (RELIEF) trial. Br J Anaesth. 2021;126(4):818-25. |
| 63. | McCullagh IJ, Begum S, Patel A, Gillies MA. Perioperative blood transfusion in major abdominal cancer surgery: A multi-centre service evaluation and national survey. BJA Open. 2022;3(100032):100032. |
| 64. | Ma X, Liu Y, Han Q, Han Y, Wang J, Zhang H. Transfusion-related immunomodulation in patients with cancer: Focus on the impact of extracellular vesicles from stored red blood cells (Review). Int J Oncol. 2021;59(6):108. |
| 65. | Ackfeld T, Schmutz T, Guechi Y, Le Terrier C. Blood transfusion reactions-A comprehensive review of the literature including a Swiss perspective. J Clin Med. 2022;11(10):2859. |
| 66. | Xu Z, Ma W, Hester DL, Jiang Y. Anticipated and unanticipated difficult airway management. Current Opin Anaesthesiol. 2018;31(1):96-103. |
| 67. | Zheng G. Airway Management in Special Situations. In: Hagberg C, Gottumukkala V, Riedel B, Nates J, Buggy D (editors). Perioperative care of the cancer patient, Elsevier; 2023, pp. 193-200. |
| 68. | Deng J, Ridner SH, Dietrich MS, Wells N, Wallston KA, Sinard RJ, et al. Prevalence of secondary lymphedema in patients with head and neck cancer. J Pain Symptom Manage. 2012;43(2):244-52. |
| 69. | Zheng G, Feng L, Lewis CM. A data review of airway management in patients with oral cavity or oropharyngeal cancer: A single-institution experience. BMC Anesthesiol. 2019;19(1):92. |
| 70. | Apfelbaum JL, Hagberg CA, Connis RT, Abdelmalak BB, Agarkar M, Dutton RP, et al. 2022 American Society of Anesthesiologists practice guidelines for management of the difficult airway. Anesthesiology. 2022;136(1):31-81. |
| 71. | Charco-Mora, P, Urtubia R, Reviriego-Agudo L. El modelo del Vórtex: una aproximación diferente a una vía aérea difícil. Rev Esp Anestesiol Reanim (Engl Ed). 2018;65(7):385-93. |
| 72. | Chrimes N, Higgs A, Sakles JC. Welcome to the era of universal airway management. Anaesthesia. 2020;75(6):711-15. |
| 73. | Chrimes N. The Vortex approach to airway management. Australas Anaesth. 2019; 3-12. |
| 74. | Ahmad I, El-Boghdadly K, Bhagrath R, Hodzovic I, McNarry AF, Mir F, et al. Difficult Airway Society guidelines for awake tracheal intubation (ATI) in adults. Anaesthesia. 2020;75(4):509-28. |
| 75. | Ramirez M, Cata JP. Anesthesia techniques and long-term oncological outcomes. Front Oncol. 2021;11:788918. |
| 76. | Zhang YL, Pei LJ, Sun C, Zhao MY, Che L, Huang YG. Regional anesthesia and cancer recurrence in patients with late-stage cancer: A systematic review and meta-analysis. Chin Med J (Engl). 2021;134(20):2403-11. |
| 77. | Buddeberg BS, Seeberger MD. Anesthesia and oncology: Friend or foe? Front Oncol. 2022;12:802210. |
| 78. | Anderson KJ, Cormier RT, Scott PM. Role of ion channels in gastrointestinal cancer. World J Gastroenterol. 2019;25(38):5732-72. |
| 79. | Lopez-Charcas O, Pukkanasut P, Velu SE, Brackenbury WJ, Hales TG, Besson P, et al. Pharmacological and nutritional targeting of voltage-gated sodium channels in the treatment of cancers. iScience. 2021;24(4):102270. |
| 80. | Lee JH, Kim DH, Koh WU. Real-time ultrasound guided thoracic epidural catheterization: A technical review. Anesth Pain Med (Seoul). 2021;16(4):322-28. |
| 81. | Yoo S, Kim Y, Park SK, Ji SH, Kim JT. Ultrasonography for lumbar neuraxial block. Anesth Pain Med (Seoul). 2020;15(4):397-408. |
| 82. | Vidal Fuentes J. Versión actualizada de la definición de dolor de la IASP: un paso adelante o un paso atrás. Rev Soc Esp Dolor [Internet]. 2020;27(4):232-233. Disponible en URL: https://scielo.isciii.es/pdf/dolor/v27n4/1134-8046-dolor-27-04-00232.pdf |
| 83. | Cuéllar-Guzmán LF, Guerra-De La Garza JM, Pérez-González OR. Manejo peri operatorio del dolor en cirugía oncológica ginecológica. GAMO. 2017;16(2):128-133. |
| 84. | Cata JP, Corrales G, Speer B, Owusu-Agyemang P. Postoperative acute pain challenges in patients with cancer. Best Pract Res Clin Anaesthesiol. 2019;33(3):361-71. |
| 85. | Garduño-López AL, Nuche-Cabrera E, Monroy-Álvarez C. Dolor postoperatorio: optimización del manejo en el contexto perioperatorio. Rev Mex Anest [Internet]. 2016;39(Suppl 1):S16-S19. |
All Rights Reserved® 2019
Latin American Journal of Clinical Sciences and Medical Technology,Publicación contínua • Editor responsable: Gilberto Castañeda Hernández. • Reserva de Derechos al Uso Exclusivo: 04-2019-062013242000-203; ISSN: 2683-2291; ambos otorgados por el Instituto Nacional del Derecho de Autor. • Responsable de la última actualización de este número, Web Master Hunahpú Velázquez Martínez,
Calle Profesor Miguel Serrano #8, Col. Del Valle, Alcaldía Benito Juárez, CP 03100, Ciudad de México, México. Número telefónico: 55 5405 1396 • Fecha de última modificación, 28 de agosto de 2024.
All Rights Reserved® 2019
Publicación contínua • Editor responsable: Gilberto Castañeda Hernández. • Reserva de Derechos al Uso Exclusivo: 04-2019-062013242000-203; ISSN: 2683-2291; ambos otorgados por el Instituto Nacional del Derecho de Autor. • Responsable de la última actualización de este número, Web Master Hunahpú Velázquez Martínez,
Calle Profesor Miguel Serrano #8, Col. Del Valle, Alcaldía Benito Juárez, CP 03100, Ciudad de México, México. Número telefónico: 55 5405 1396 • Fecha de última modificación, 28 de agosto de 2024.