| ** | Latin American Journal of Clinical Sciences and Medical Technology is an open access magazine. To read all published articles and materials you just need to register Registration is free of charge. Register now If you already have registered please Log In | ** |
aDepartamento de Tumores Mamarios, Subdirección de Cirugía, Instituto Nacional de Cancerología, Ciudad de México, México; bDepartamento de Tumores Mamarios, Subdirección de Radioterapia, Instituto Nacional de Cancerología, Ciudad de México, México; cDepartamento de Tumores Mamarios, Subdirección de Medicina Interna, Instituto Nacional de Cancerología, Ciudad de México, México; dDepartamento de Tumores Mamarios, Programa Especial de Acciones para Cáncer de Mama, Instituto Nacional de Cancerología, Ciudad de México, México.
Autor para correspondencia: , . Números telefónicos: ; e-mail: ebargallo@yahoo.com; enrique.bargallo@gmail.com
Lat Am J Clin Sci Med Technol. 2020 Jul;2:126-144.
Recibido: 12 de mayo, 2020
Aceptado: 04 de julio, 2020
Publicado: 15 de julio, 2020
Vistas: 3619
Descargas: 60
El cáncer de mama constituye un problema de salud pública a nivel mundial y en nuestro país se diagnostica generalmente en etapas avanzadas. El Departamento de Tumores Mamarios del Instituto Nacional de Cancerología desarrolló la Oncoguía de cáncer de mama 2020 con base en una metodología de consenso entre sus integrantes: oncólogos clínicos, cirujanos oncólogos, radioterapeutas, enfermeras y trabajadores sociales. El manejo multidisciplinario que dichos especialistas llevan a cabo mediante la evaluación clínica de la Unidad Funcional —y que se detalla en esta Oncoguía— se basa en cirugía, radioterapia y tratamiento sistémico que puede ser adyuvante, neoadyuvante o paliativo. En el manejo sistémico se incluye la quimioterapia, el bloqueo hormonal y la terapia biológica. También se incluyen los algoritmos para la toma de decisiones en cada etapa clínica.
Breast cancer is a world health problem, and in our country is generally diagnosed in advanced stages. Departamento de Tumores Mamarios from Instituto Nacional de Cancerología developed Oncoguía de cáncer de mama 2020 based on a consensus methodology conducted among its members: clinical oncologists, surgical oncologists, radiation therapists, nurses, and social workers. Such specialists carry out multidisciplinary management (detailed in this Oncoguía) through a clinical assessment performed by Unidad Funcional, and it is based on surgery, radiotherapy, and systemic treatment, either adjuvant, neoadjuvant or palliative. The systemic management also includes chemotherapy, hormone blockade, and biological therapy. These guidelines also include algorithms to make decisions in every clinical stage.
El cáncer de mama es un problema de salud pública no sólo en nuestro medio, sino a nivel mundial.1 De acuerdo con GLOBOCAN, en el año 2018 la prevalencia de cáncer de mama a 5 años fue de casi 7 millones, lo que representa aproximadamente el 15.7% de todos los cánceres; una incidencia mundial > 2 millones y una mortalidad de poco más de 625 mil. En México, para el mismo año, se estimó una prevalencia de 83,287 casos, mortalidad de 6,884 pacientes e incidencia de 105 mil casos¹ durante 5 años, es decir, ocupó el primer lugar en incidencia y el segundo en mortalidad entre todos los cánceres en el país.
El cáncer de mama en etapas iniciales suele ser subclínico, es decir, asintomático y sólo puede detectarse con estudios de imagen tales como mastografía, ultrasonido y/o resonancia magnética.1 A pesar de los esfuerzos realizados por los sistemas de salud en México², aproximadamente el 70% de los casos se encuentra con enfermedad localmente avanzada al momento del diagnóstico2, de modo que ya puede haber manifestaciones clínicas tales como edema, ulceración, cutánides y afección a ganglios linfáticos.
La toma de una biopsia, preferentemente con aguja de corte, es importante para determinar el tipo histológico, grado nuclear y el fenotipo de acuerdo con la expresión de receptores hormonales y HER2 evaluados mediante inmunohistoquímica. La estadificación de la enfermedad y los resultados patológicos que revela la biopsia de suma importancia ya que ofrecen información pronóstica y determinan la conducta terapéutica más adecuada.3
El tratamiento del cáncer de mama es multidisciplinario. El manejo se basa en cirugía, radioterapia y tratamiento sistémico (neoadyuvante, adyuvante o paliativo), que incluye quimioterapia, terapia con bloqueo hormonal y terapia biológica (anticuerpos monoclonales). Una vez que ha concluido un tratamiento se debe llevar a cabo un seguimiento clínico periódico (cada 3 meses los primeros 2 años, cada 6 meses del año 3 al 5 y después de manera anual) con la finalidad de detectar recaída local, regional o sistémica y la aparición de un segundo tumor primario. Como medidas generales se recomiendan el ejercicio aeróbico y evitar el desarrollo de sobrepeso y obesidad.
Para pacientes con enfermedad metastásica —clasificada en visceral (hígado, pulmón y sistema nervioso central) y no visceral (hueso, tejidos blandos)—, la supervivencia global puede variar entre 12 meses y 3-5 años, respectivamente.4
El cáncer de mama también se clasifica en riesgo de progresión bajo y alto. El riesgo es bajo si están presentes receptores hormonales positivos, HER2 negativo, período libre de enfermedad > 1 año y metástasis que se limitan a tejidos blandos y hueso. Es riesgo alto en el caso de que haya receptores hormonales negativos, HER2 positivo, período libre de enfermedad < 1 año, metástasis extensa o visceral. En consecuencia, se elige el tratamiento más activo y menos tóxico, en aras de un mayor tiempo libre de progresión.4,5
Ante este panorama, se llevó a cabo un consenso entre médicos y personal de salud de la Unidad Funcional del Instituto Nacional de Cancerología en el que se conformó la presente Oncoguía, que refleja el protocolo general de manejo de las pacientes con cáncer de mama en dicho Instituto.
Esta Oncoguía incluye sugerencias y recomendaciones para el manejo de pacientes en condiciones ideales; de modo que puede ser de utilidad para orientar otros Servicios de Oncología. No presenta razonamientos costo-eficientes, ni determinantes para compra de medicamentos.
1. Tratamiento adyuvante RH-/HER2 positivo
Inicialmente se realiza una valoración por la Unidad Funcional, conformada por cirujano oncólogo, oncólogo médico, radio-oncólogo, ginecólogo oncólogo, patólogo, radiólogo, cirujano plástico, enfermería y navegación (Figura 1).
Una vez que la evidencia postquirúrgica e histopatológica muestre pT1, pT2, pT3, pT4, pN0-N3, se procede a realizar un ecocardiograma a la paciente. En caso de FEVI <50%, debe implementarse tratamiento conjunto con cardiología.
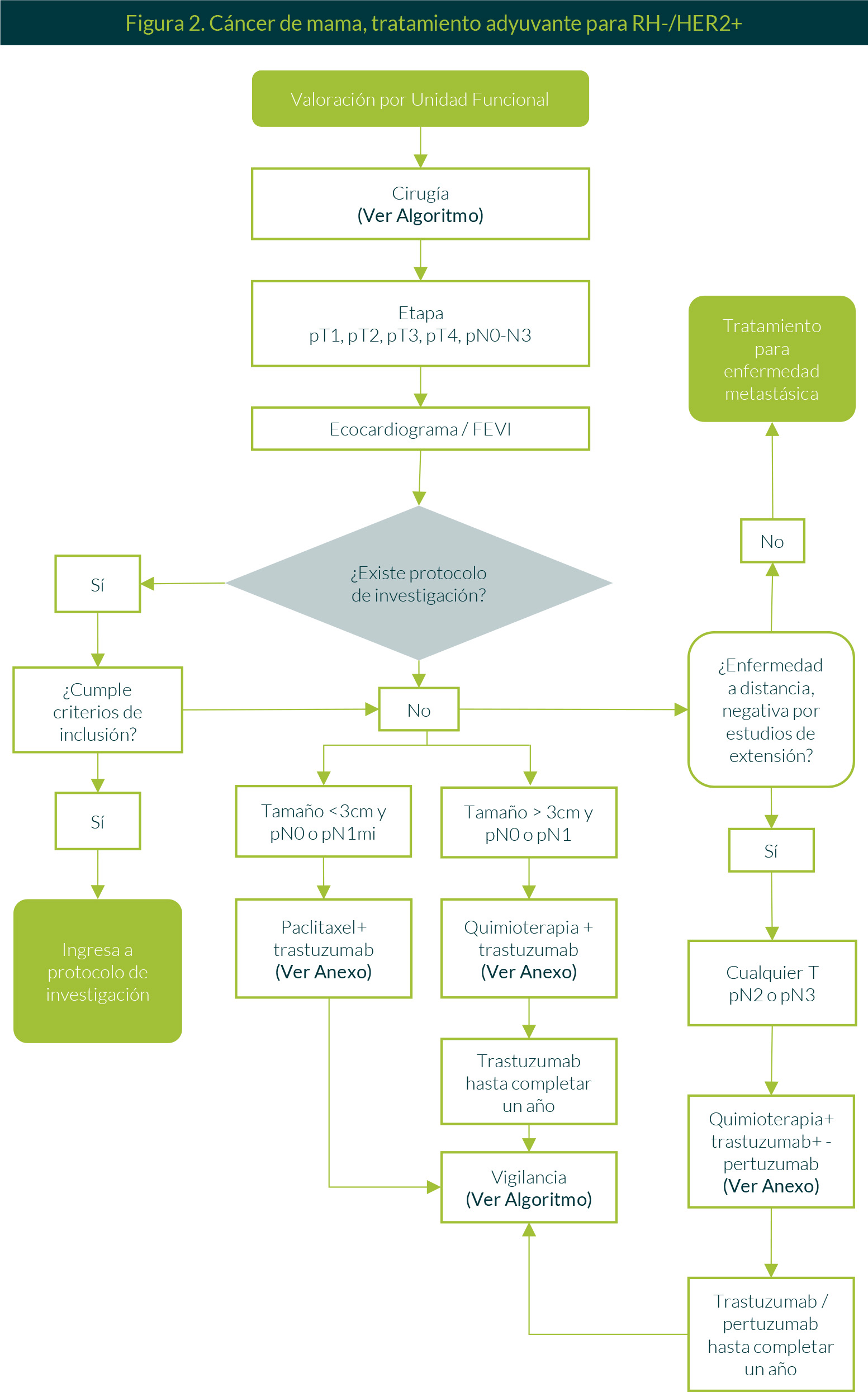
Posteriormente, si la paciente cumple con criterios de inclusión para algún proyecto de investigación que se encuentre activo, ingresará a protocolo. En caso contrario, se procederá a proponer un tratamiento sistémico (Figura 2):
- Si el tumor tiene un tamaño menor a 3 cm de diámetro y la evaluación axilar refiere pN0 o pN1mi, se administrará paclitaxel + trastuzumab semanal, seguido de trastuzumab cada 21 días hasta completar un año y, posteriormente, la paciente iniciará vigilancia.
- Si el tumor tiene un diámetro mayor de 3 cm y/o tiene pN1, se administrará quimioterapia con antraciclinas y taxanos + trastuzumab, seguido de trastuzumab cada 21 días hasta completar un año y al finalizar se someterá a vigilancia.
- Para cualquier tamaño tumoral asociado a un componente axilar patológico de pN2 o pN3, se administrará quimioterapia (secuenciación antraciclinas y taxanos) con trastuzumab + pertuzumab hasta completar un año. Al término iniciará vigilancia.
2. Tratamiento adyuvante RH+/HER2
Se realizará valoración multidisciplinaria por la Unidad Funcional.
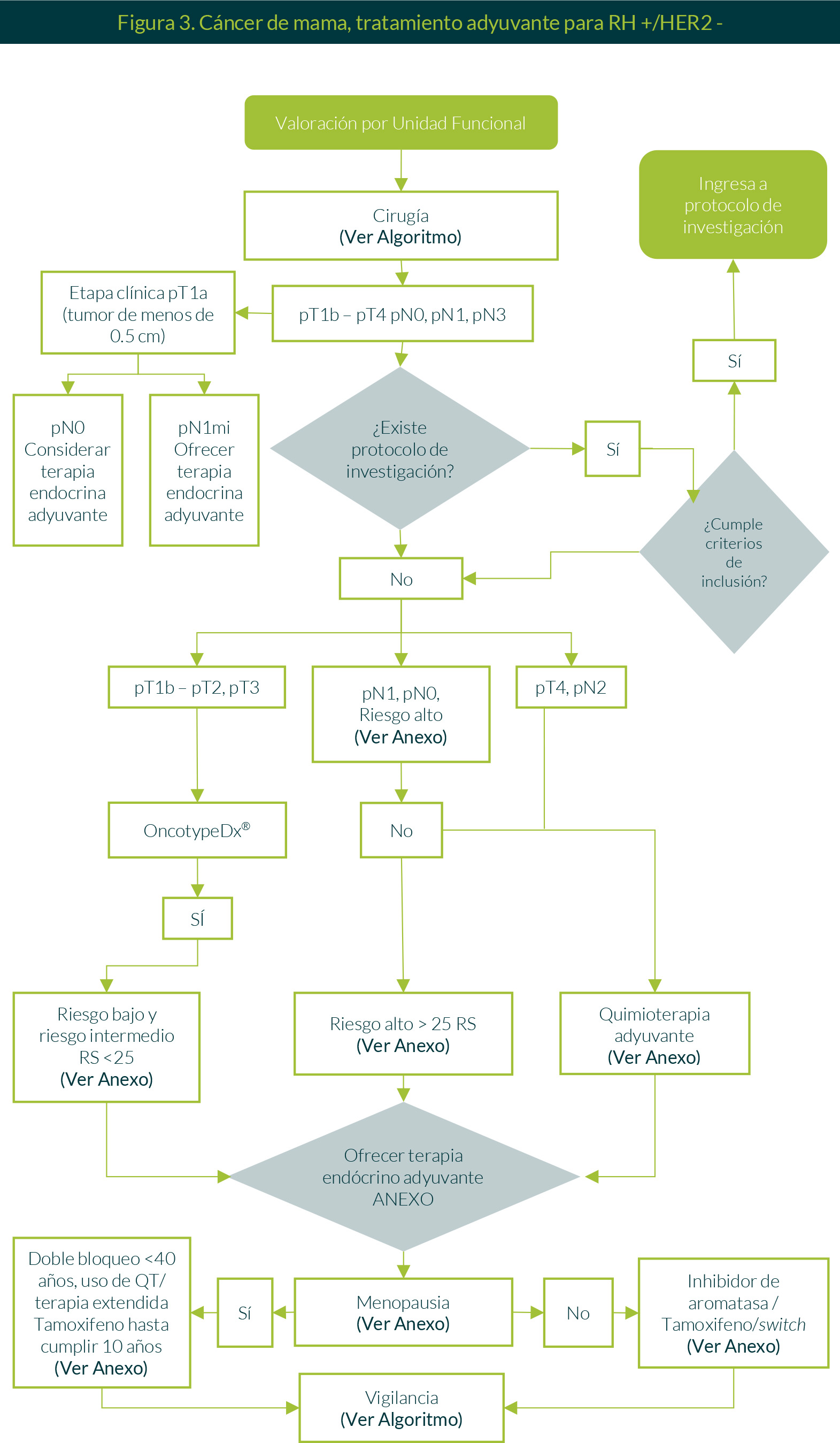
Cuando la evidencia postquirúrgica e histopatológica muestre pT1b-pT4, pN0, pN1, pN3 y la paciente cumpla con criterios de inclusión para algún proyecto de investigación activo, la paciente ingresará a protocolo. En caso contrario, se ofrecerá terapia sistémica de la siguiente manera:
- Si la etapa clínica es pT1a (tumor < 0.5 cm) y la evaluación axilar determina pN0 o pN1, se considerará un tratamiento con terapia endocrina adyuvante de acuerdo con riesgo y toxicidades.
- Si pT1b-pT2, pT3, pN0-pN1, se solicitará una prueba de OncotypeDx®:
- Si el resultado determina la presencia de riesgo bajo de recurrencia, se ofrecerá terapia endocrina adyuvante.
- Si es de riesgo intermedio, se ofrecerá terapia endocrina adyuvante a pacientes mayores de 50 años al igual que en pacientes menores de 50 años que obtengan un puntaje menor a 15.
- Se considerará quimioterapia adyuvante + terapia endocrina en pacientes menores de 50 años y que tengan un puntaje mayor o igual a 15.
- Si no se realiza la prueba de OncotypeDx®, se optará por ofrecer quimioterapia adyuvante en pacientes con axila pN1, pN0 con factores de riesgo alto de recurrencia.
En pacientes con patología pT4, pN2, se ofrecerá quimioterapia adyuvante.
En pacientes premenopáusicas se ofrecerá tamoxifeno durante 10 años. En pacientes menores de 35 años o que tengan factores de riesgo alto de recurrencia y que se considerasen candidatas a quimioterapia, se ofrecerá doble bloqueo. Ante la condición de posmenopausia se indicará inhibidor de aromatasa o tamoxifeno. En ambos casos se continuará con vigilancia (Figura 3).
3. Tratamiento adyuvante RH+/HER2+ (triple positivo)
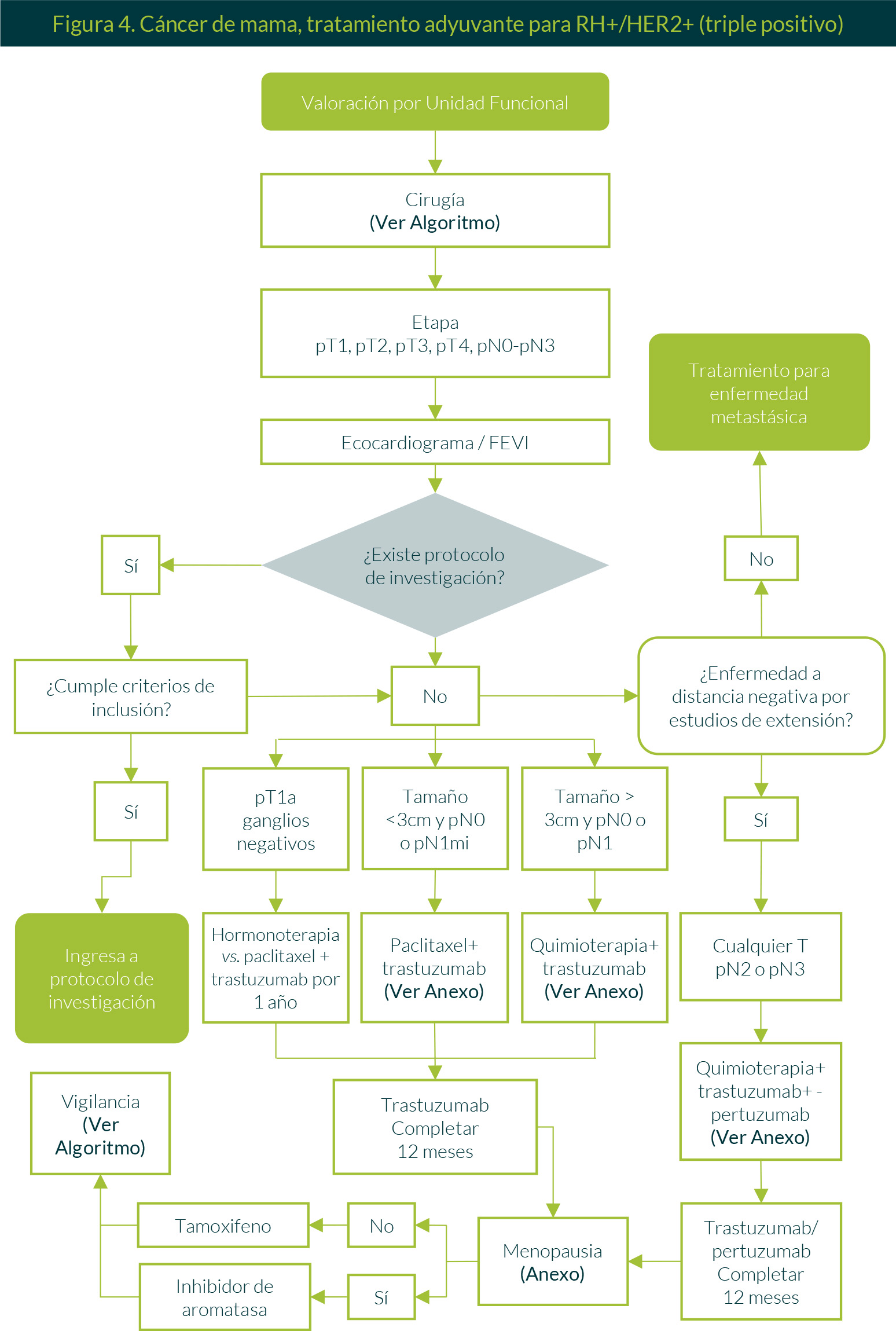
Si tras valoración por la Unidad Funcional y el evento quirúrgico se evidencia un reporte de patología con pT1, pT2, pT3, pT4 o pN0-pN3, se realizará un ecocardiograma a la paciente. En caso de existir algún proyecto de investigación y si la paciente cumple con los criterios de inclusión, se evaluará su ingreso al protocolo de investigación. En caso contrario, se realizará el manejo con base en los siguientes lineamientos:
- Si el tumor mide <3 cm y la axila presenta pN0 o pN1mi, se ofrecerá paclitaxel + trastuzumab semanal.
- Si el tamaño del tumor es >3 cm y la axila se encuentra con pN0 o pN1, se ofrecerá quimioterapia (secuenciación de antraciclinas y taxanos) + trastuzumab.
- En ambos casos se ofrecerá trastuzumab cada 21 días hasta completar 12 meses. En pacientes posmenopáusicas se agregará un inhibidor de aromatasa durante 5 años, las pacientes premenopáusicas recibirán tamoxifeno cuando menos 5 años. Posteriormente se someterá a la paciente a vigilancia.
Independientemente del tamaño del tumor, si la evaluación axilar se define como pN2 o pN3, se ofrecerá quimioterapia (secuenciación de antraciclinas y taxanos) + trastuzumab y pertuzumab hasta completar 1 año. En pacientes posmenopáusicas se agregará un inhibidor de aromatasa durante 5 años, las pacientes premenopáusicas recibirán tamoxifeno cuando menos por 5 años. Posteriormente se someterá a vigilancia (Figura 4).
4. Tratamiento adyuvante RH-/HER2- (triple negativo)
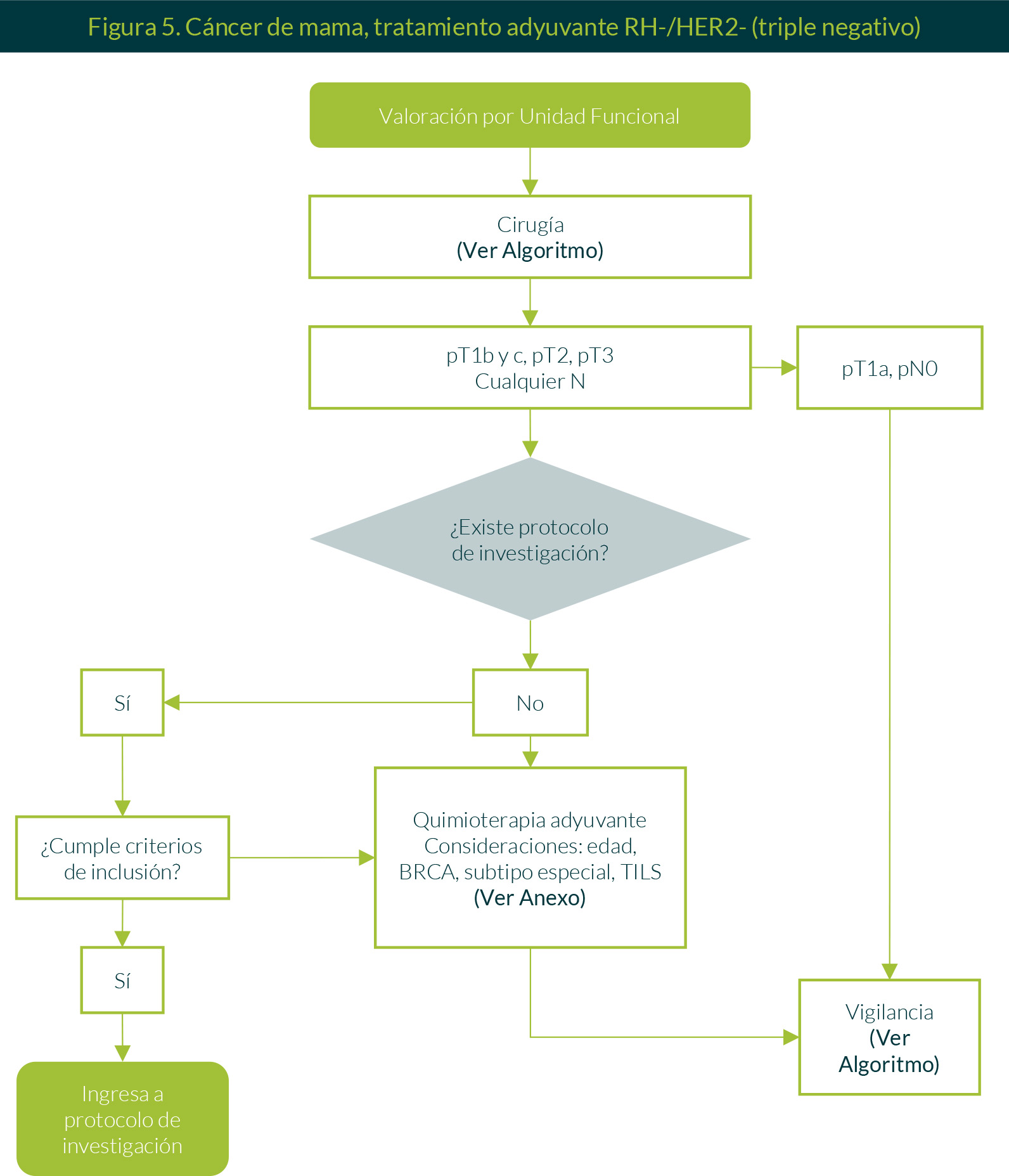
Si tras valoración por la Unidad Funcional y el evento quirúrgico se evidencia pT1b-c, pT2, pT3 y cualquier N en el reporte de patología, se evaluará la posibilidad de que la paciente pueda ser incluida en algún protocolo de investigación que se encuentre vigente, si cumple con los criterios de inclusión. De no ser así, se ofrecerá quimioterapia adyuvante (secuenciación de antraciclinas y taxanos). Una vez terminado el tratamiento adyuvante con quimioterapia, la paciente iniciará vigilancia.
Si después de la valoración integral por la Unidad Funcional y el evento quirúrgico se establece que la paciente tiene un tumor pT1a en presencia de una axila pN0, se puede proponer vigilancia (Figura 5).
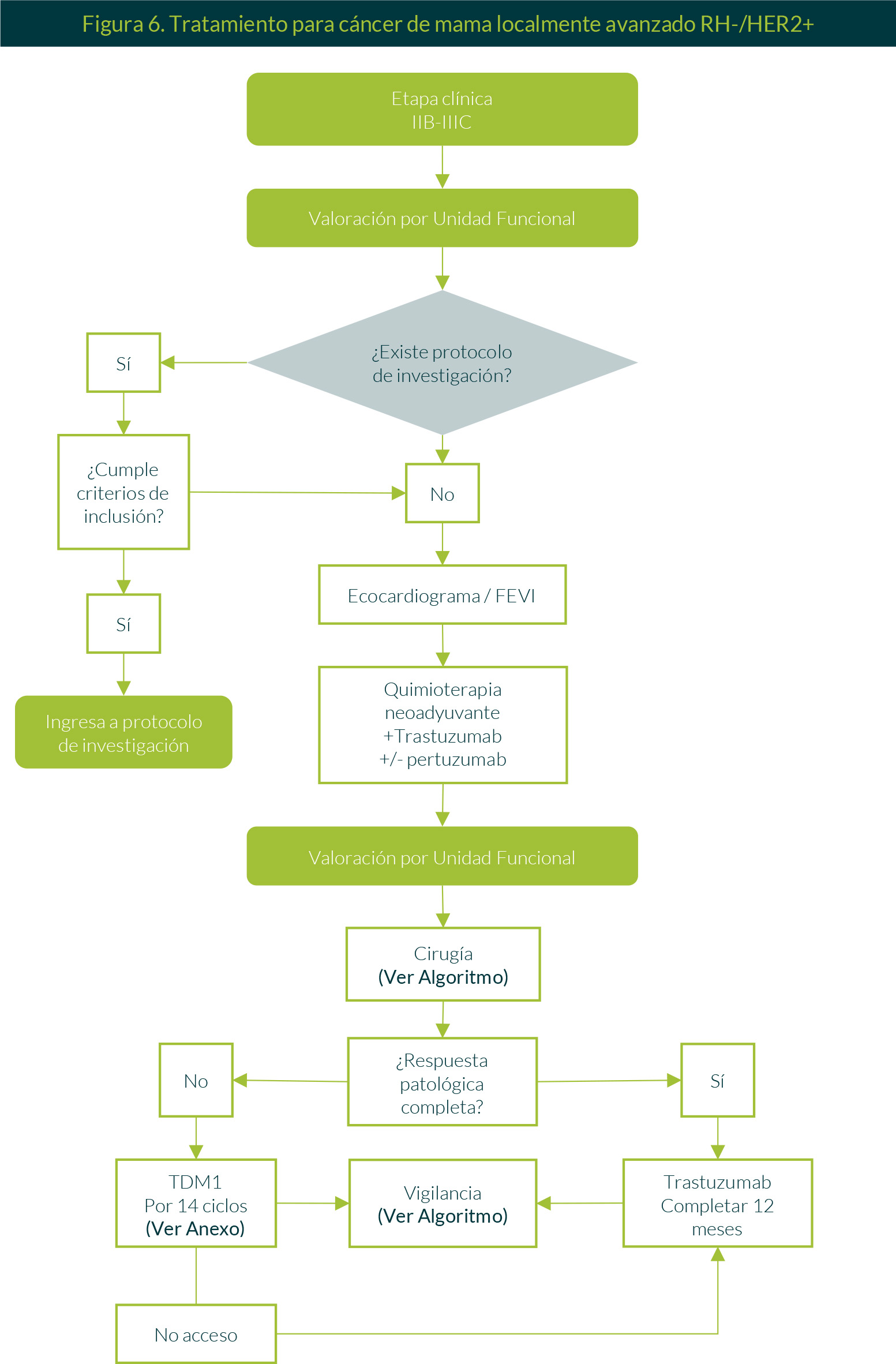
5. Tratamiento para cáncer de mama localmente avanzado RH-/HER2+
Una paciente con etapa clínica IIB-IIIC y posterior a su correspondiente valoración por la Unidad Funcional, ingresará, de ser posible, a algún protocolo de investigación vigente, si cumple con los criterios de inclusión. De no ser así, se le realizará un ecocardiograma y se ofrecerá un tratamiento neoadyuvante con quimioterapia basada en antraciclinas y taxanos + trastuzumab y pertuzumab, seguido de una revaloración y un manejo quirúrgico. En caso de que el reporte de patología de la cirugía realizada defina la presencia de respuesta patológica completa, se otorgará trastuzumab cada 21 días hasta completar 12 meses. Si el reporte de patología hace mención a enfermedad residual, la paciente puede ser candidata a recibir ado-trastuzumab emtansina (TDM1) por 14 ciclos. Una vez concluido el tratamiento complementario postquirúrgico, la paciente iniciará vigilancia. En caso de no contar con acceso a TDM1, se ofrecerá trastuzumab hasta completar 12 meses (Figura 6).
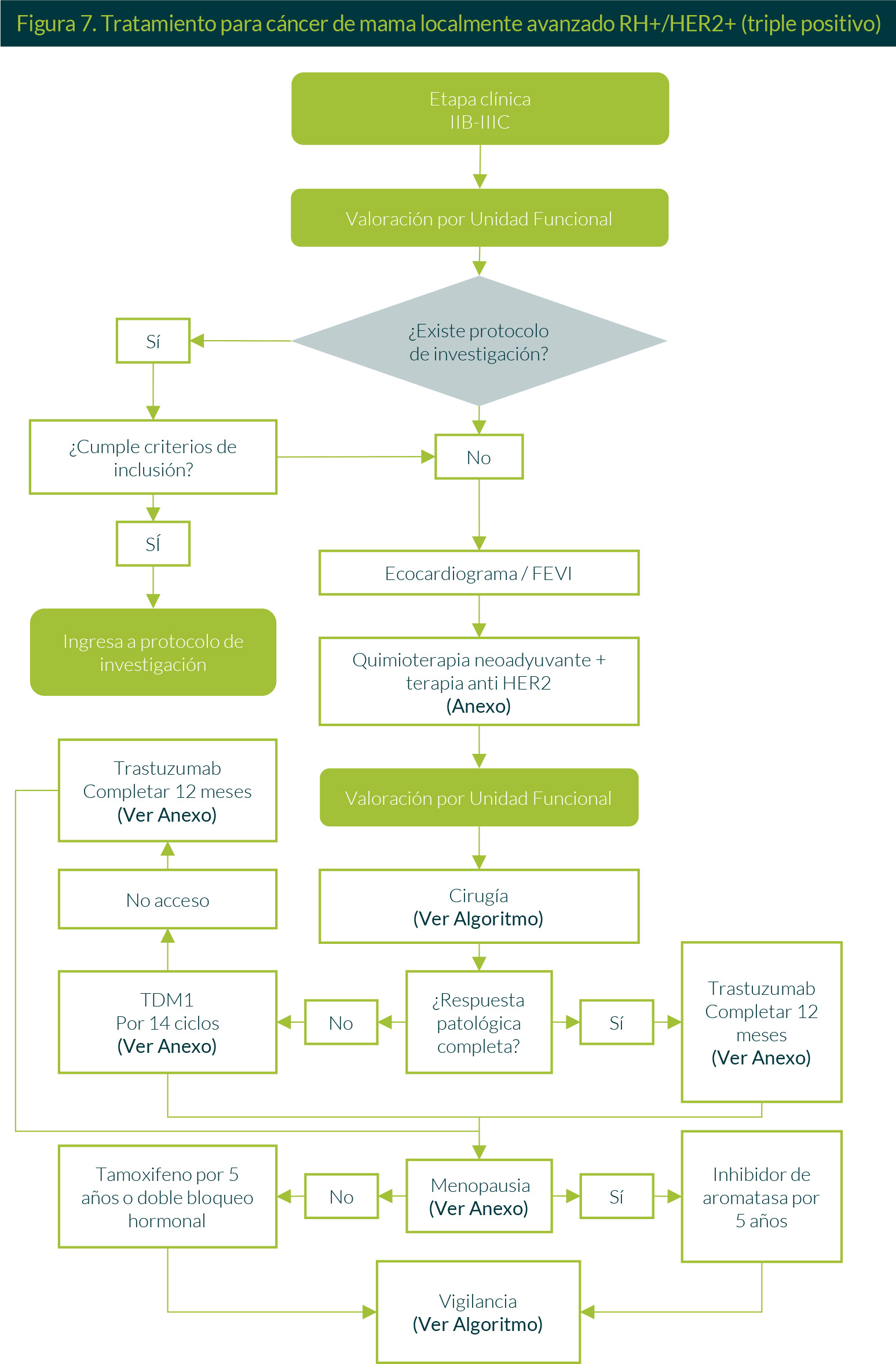
6. Tratamiento para cáncer de mama localmente avanzado RH+/HER2+ (triple positivo)
Pacientes en etapa clínica IIB-IIIC —y después de su correspondiente valoración por la Unidad Funcional— ingresarán a algún protocolo de investigación vigente si cumplen con los criterios de inclusión. De no ser así, se les realizará un ecocardiograma y se ofrecerá tratamiento neoadyuvante con quimioterapia basada en antraciclinas y taxanos + pertuzumab y trastuzumab; seguido de revaloración y el manejo quirúrgico que corresponda. En caso de que el reporte de patología de la cirugía realizada defina la presencia de respuesta patológica completa, se ofrecerá trastuzumab hasta completar 12 meses. Si el reporte de patología menciona la presencia de enfermedad residual, se dará TDM1 por 14 ciclos, si no hay acceso a tal, se ofrecerá trastuzumab hasta completar 12 meses. En ambos casos, en pacientes posmenopáusicas se indicará terapia endocrina adyuvante con un inhibidor de aromatasa por 5 años, para pacientes premenopáusicas se ofrecerá tamoxifeno cuando menos por 5 años o doble bloqueo hormonal por 5 años (Figura 7).
La vigilancia iniciará al terminar el tratamiento con terapia antiHER2.
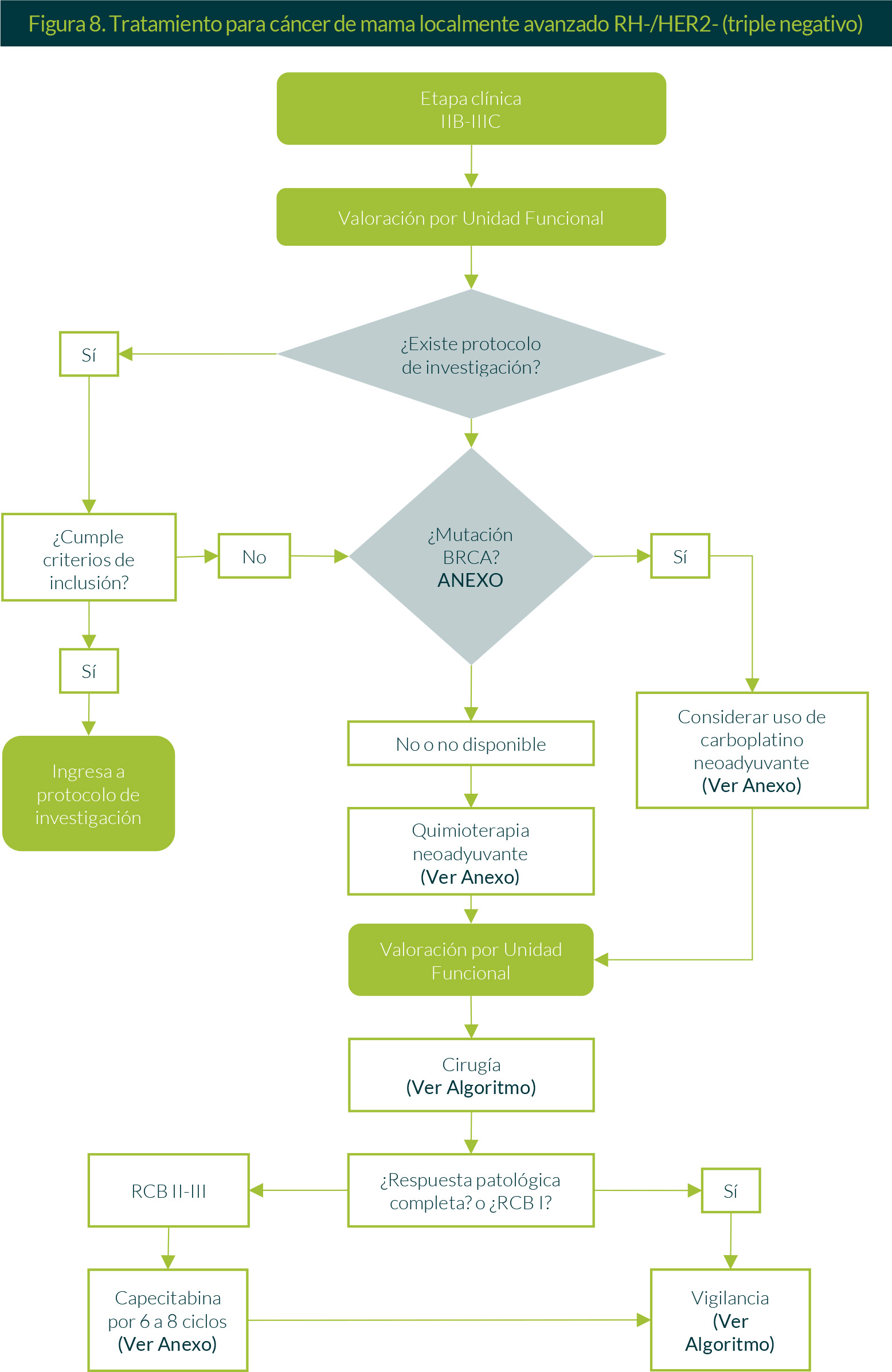
7. Tratamiento para cáncer de mama localmente avanzado RH-/HER2- (triple negativo)
En pacientes con etapa clínica IIB-IIIC y después de su correspondiente valoración por la Unidad Funcional, se valorará el ingreso a algún protocolo de investigación vigente, siempre y cuando la paciente cumpla con los criterios de inclusión.
En caso de no ser incluida en algún proyecto de investigación, la paciente será candidata a quimioterapia neoadyuvante basada en antraciclinas y taxanos.
Posteriormente, se llevarán a cabo revaloración y el manejo quirúrgico correspondiente. Es deseable contar con el estado de la mutación BRCA antes de planificar el manejo quirúrgico. Si en el reporte de patología se identifica la presencia de respuesta patológica completa o RCB 1, se someterá a vigilancia. Si el reporte de patología menciona RCB II-III, se ofrecerá capecitabina de 6 a 8 ciclos. Posteriormente, en ambos casos la paciente se someterá a vigilancia (Figura 8).
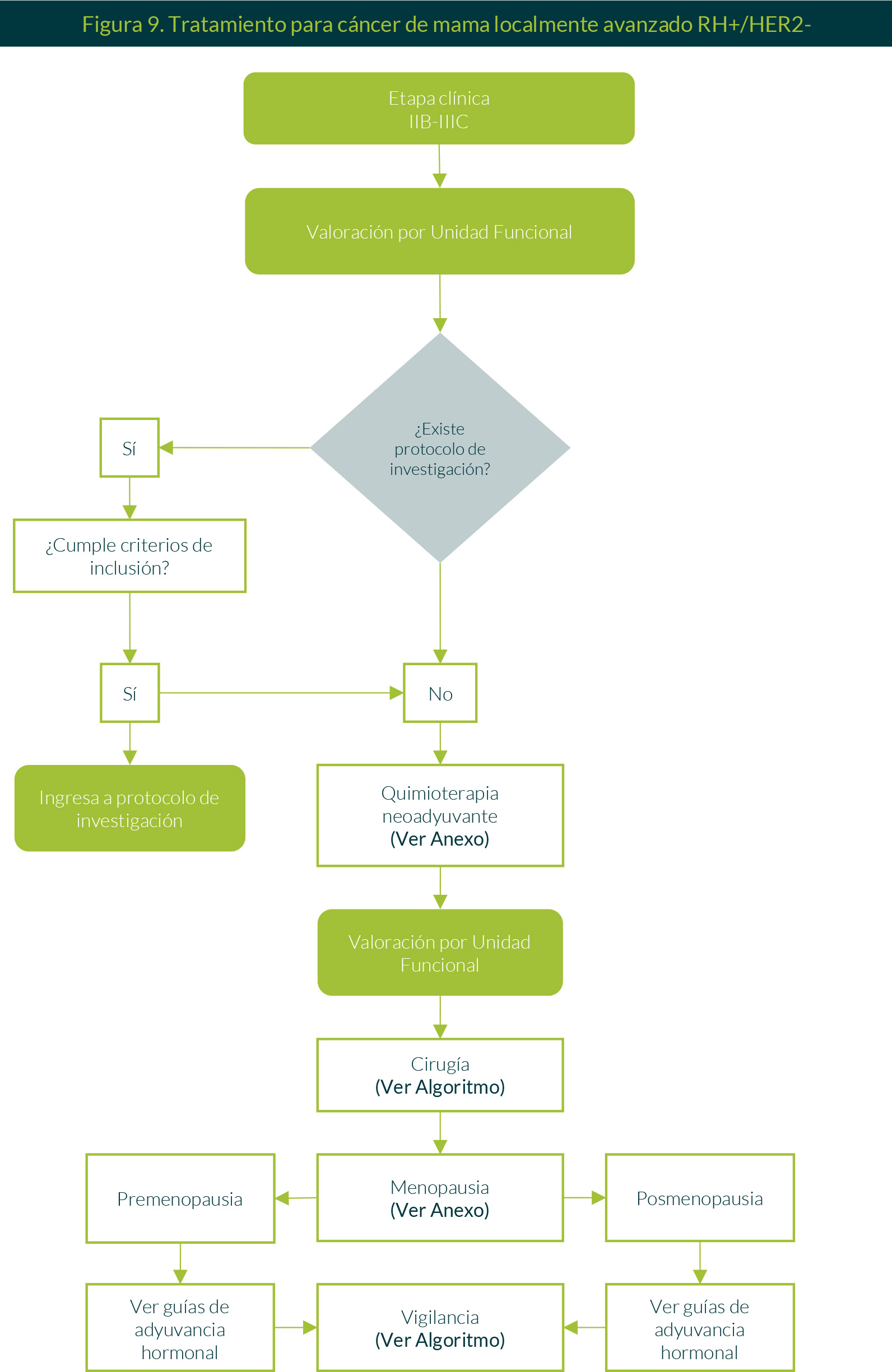
8. Tratamiento para cáncer de mama localmente avanzado RH+/HER2-
Pacientes con etapa clínica IIB-IIIC —y después de su correspondiente valoración por la Unidad Funcional— ingresarán a protocolo de investigación si cumplen con los criterios de inclusión. De no ser así, se ofrecerá quimioterapia neoadyuvante basada en antraciclinas y taxanos. Después se llevarán a cabo revaloración y cirugía. Ante la presencia de premenopausia o postmenopausia, se dará adyuvancia hormonal y, finalmente, se someterá a vigilancia (Figura 9).
9. Vigilancia y seguimiento en cáncer de mama
En cuanto a la vigilancia, se hace un examen físico cada tres meses y, si hay aparición de síntomas, se realizarán estudios. Si en dichos estudios hay negatividad de metástasis, se mantendrá en vigilancia. De haber hallazgos metastásicos se realizará biopsia.
Ante la recurrencia de cáncer, se ingresará a protocolo de investigación si cumple con los criterios de inclusión. En caso contrario, se dará tratamiento a enfermedad metastásica (Figura 10).
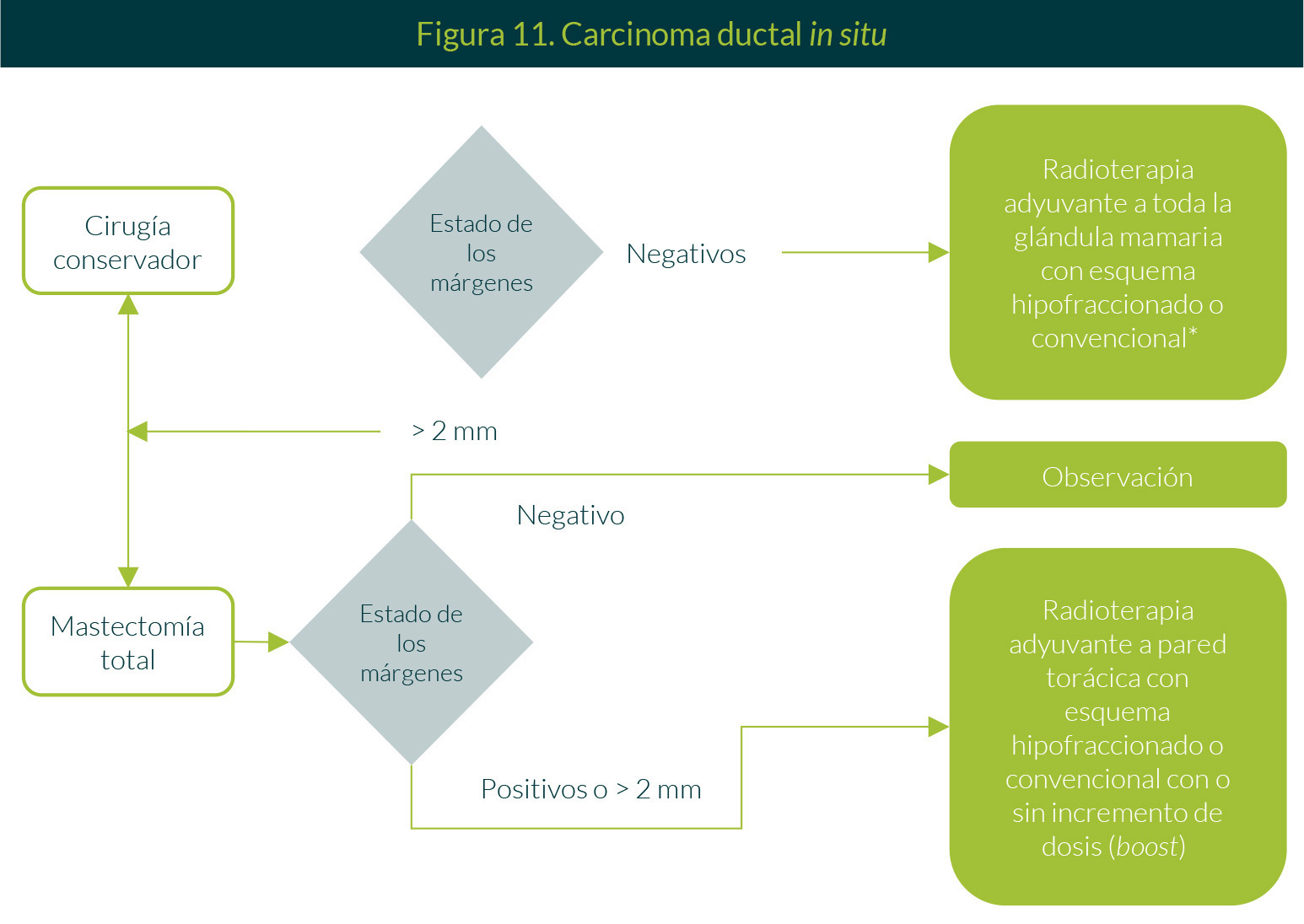
1. Carcinoma ductal in situ
Ante una tumoración >2 mm, se realizará cirugía conservadora o mastectomía total. Se verificará el estado de los márgenes. Si tras cirugía conservadora los márgenes son negativos, se dará radioterapia adyuvante a toda la glándula mamaria con esquema hipofraccionado o convencional. En el caso de mastectomía total, si los márgenes son negativos, se optará por la observación; si son positivos ó >2 mm se dará radioterapia adyuvante a pared torácica con esquema hipofraccionado o convencional, con o sin incremento de dosis (Figura 11).
Después de la mastectomía total, se verifica el estado de los márgenes.
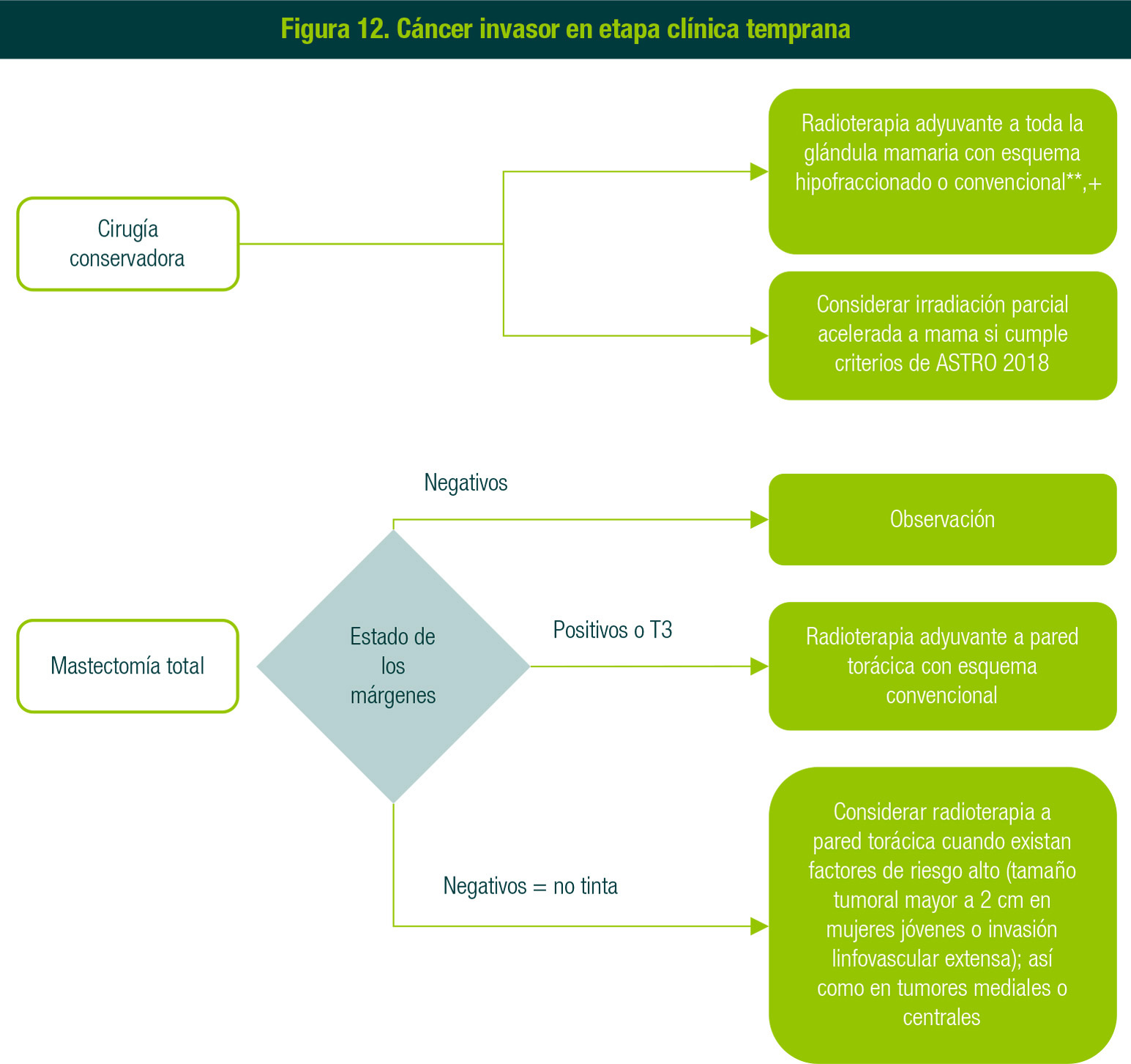
2. Cáncer invasor en etapa clínica temprana
En el marco de cirugía conservadora se dará radioterapia a toda la glándula mamaria con esquema hipofraccionado o convencional (Figura 12).
Ante una mastectomía total se verificará el estado de los márgenes y, si son negativos, se someterá a observación; si son positivos ó >2 mm, se dará radioterapia adyuvante a pared torácica con esquema hipofraccionado o convencional, con o sin incremento de dosis (boost).
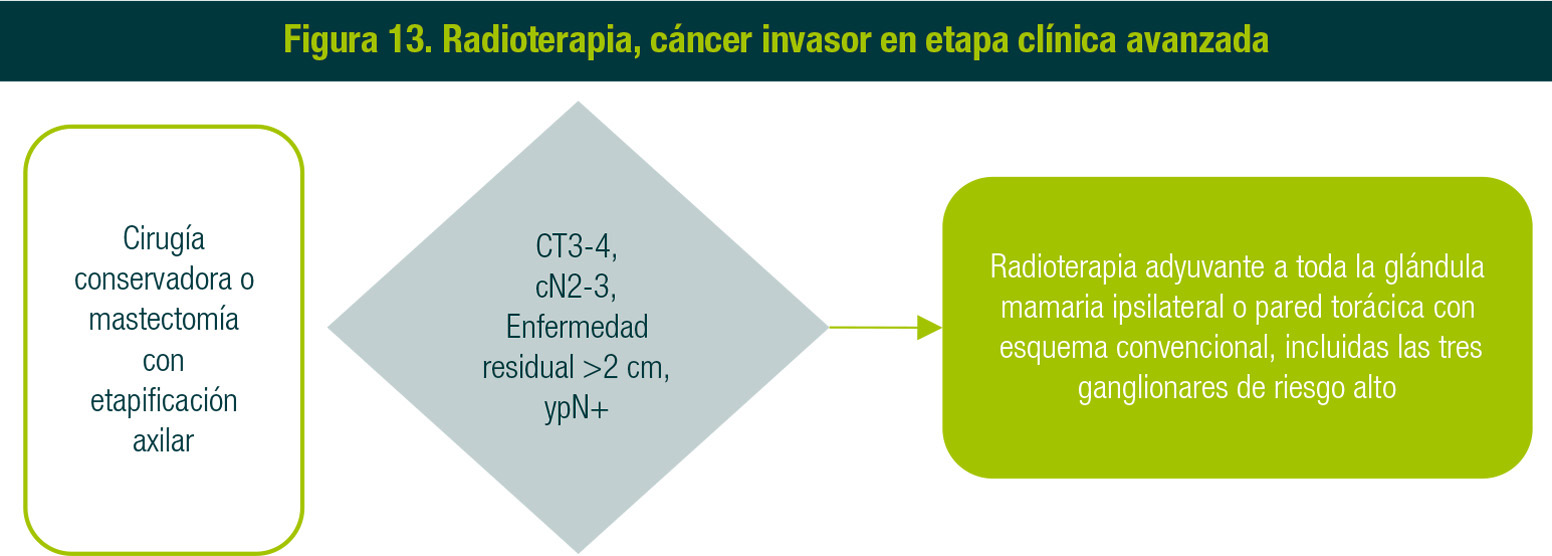
3. Cáncer invasor en etapa clínica avanzada
Ante la realización de cirugía conservadora o mastectomía, si se evidencia CT3-4, cN2-3, enfermedad residual > 2 cm, ypN+, se dará radioterapia adyuvante a toda la glándula ipsilateral o pared torácica con esquema convencional, incluidas las tres ganglionares de riesgo alto (Figura 13).
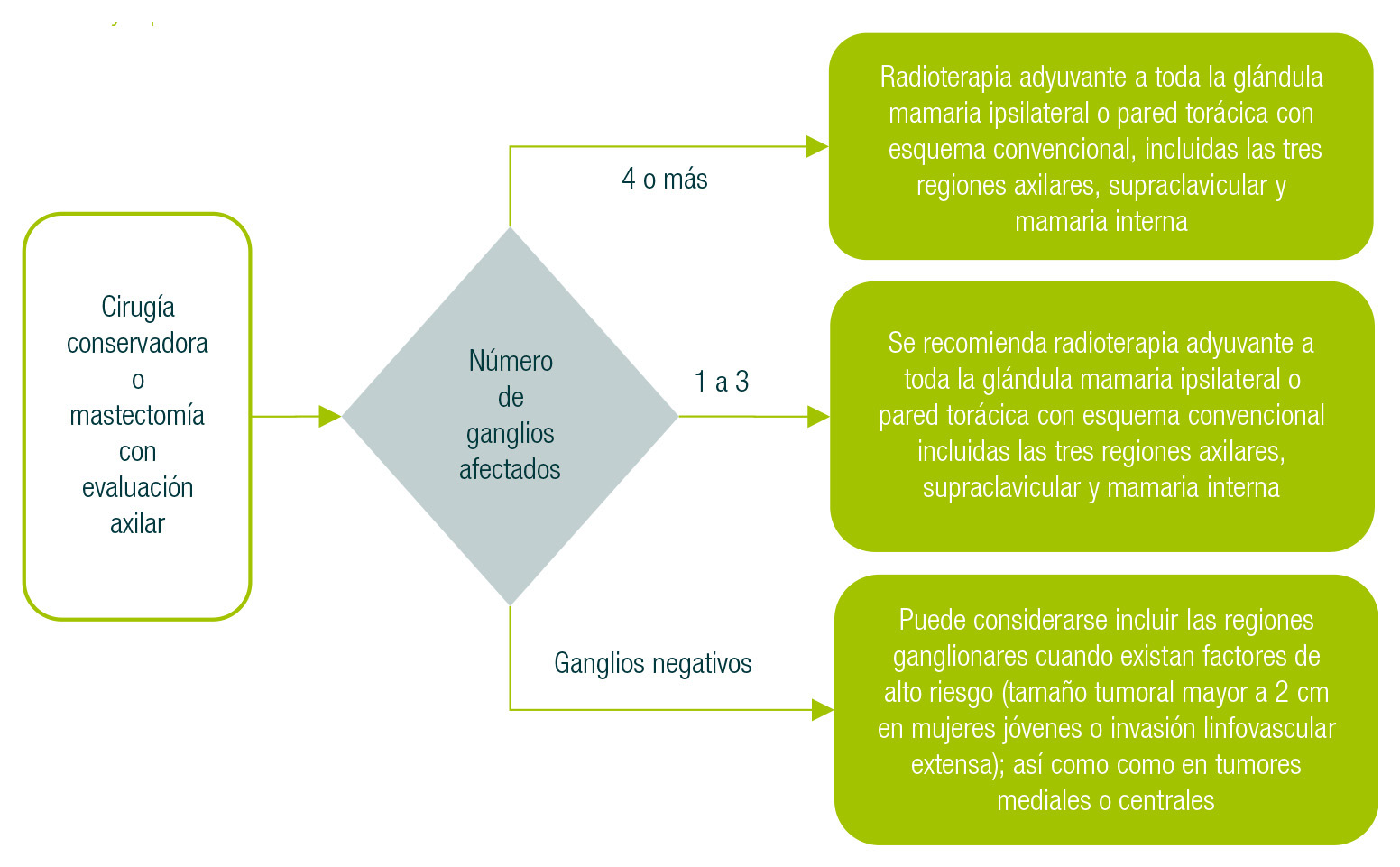
4. Radioterapia a regiones ganglionares
Tras cirugía conservadora se realizará estudio patológico, si resulta negativo se ofrecerá radioterapia adyuvante a toda la glándula mamaria con esquema hipofraccionado o convencional, sin incluir regiones ganglionares. Si el estudio patológico resulta positivo, se dará radioterapia a toda la glándula mamaria ipsilateral con esquema convencional, incluidos los tres niveles axilares y supraclaviculares.
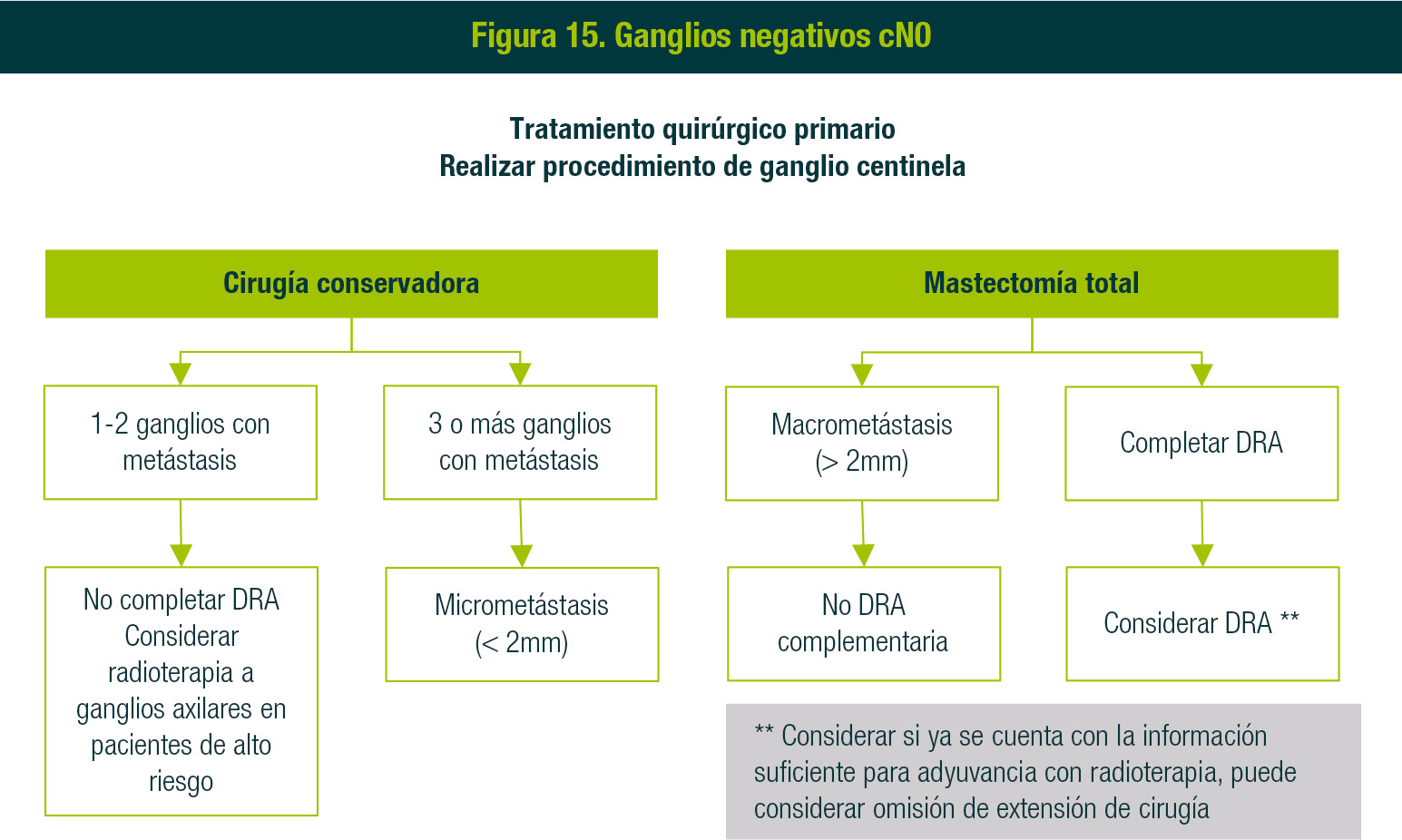
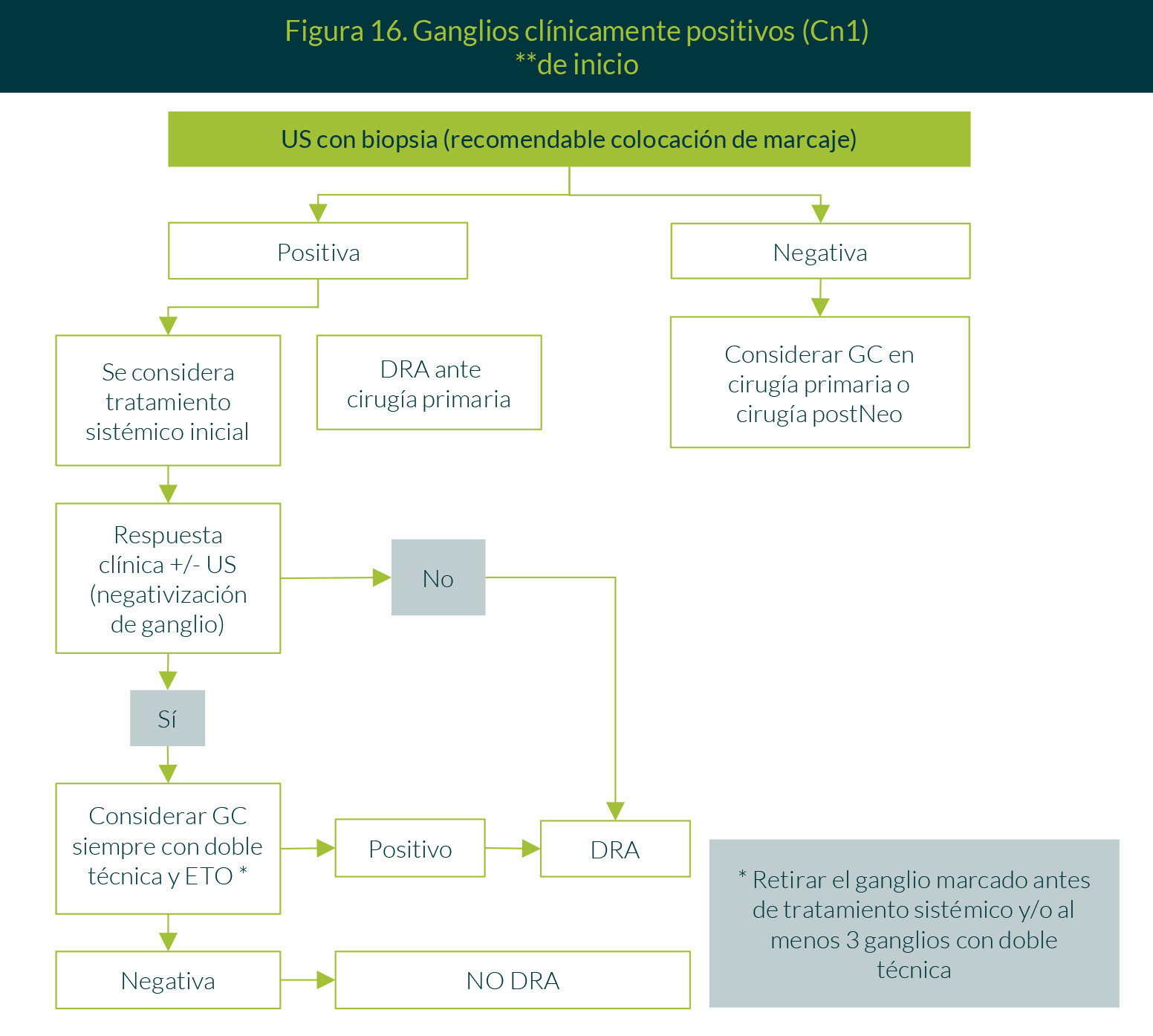
Si en el marco de una cirugía conservadora o mastectomía con evaluación axilar hay ganglios afectados, se procederá a diferente conducta, dependiendo del número de ganglios afectados. Si son cuatro o más, se dará radioterapia adyuvante a toda la glándula mamaria ipsilateral o pared torácica con esquema convencional, incluidas las tres regiones axilares, supraclavicular y mamaria interna. Si son de 1 a 3, se recomienda radioterapia adyuvante a toda la glándula mamaria ipsilateral o pared torácica con esquema convencional, incluidas las tres regiones axilares, supraclavicular y mamaria interna. Si hay ganglios negativos, puede considerarse incluir las regiones ganglionares cuando existan factores de riesgo alto (tamaño tumoral mayor a 2 cm en mujeres jóvenes o invasión linfovascular extensa), así como en tumores mediales o centrales (Figuras 14, 15 y 16).
Paciente posmenopáusica
- Mayor de 60 años
- Con ooforectomía bilateral previa
- Menor de 60 años y amenorreica por 12 meses o más en la ausencia de quimioterapia, tamoxifeno o supresión ovárica y perfil hormonal en rangos posmenopaúsicos (FSH mayor a 20 y estradiol menor a 5)
- Menores de 60 años que toman tamoxifeno y tienen un perfil hormonal en rangos posmenopáusicos
Terapia endocrina adyuvante
- Ofrecer tamoxifeno a pacientes premenopáusicas durante 10 años
- Doble bloqueo + tamoxifeno o inhibidor de aromatasa a pacientes premenopáusicas menores de 35 años, o que se consideraron candidatas a quimioterapia adyuvante
- Ofrecer preferentemente inhibidor de aromatasa (IA) a pacientes posmenopáusicas
Resultado de OncotypeDx®
- Riesgo bajo RS <11 ofrecer terapia endocrina adyuvante
- Riesgo intermedio RS 12-25
- Ofrecer terapia endocrina adyuvante a mayores de 50 años
- Considerar quimioterapia adyuvante + terapia endocrina en menor de 50 años y RS mayor o igual a 15
- Riesgo alto RS >25 ofrecer quimioterapia adyuvante + terapia endocrina
- Criterios de riesgo alto para tratamiento con quimioterapia adyuvante
- Tres o más ganglios positivos, edad menor de 40 años, permeación linfovascular, grado tumoral 3
Esquemas de quimioterapia
HER2 negativo
- Adriamicina 60 mg D1 y ciclofosfamida 600 mg D1 cada 21 días por 4 ciclos, seguidos de paclitaxel 80 mg semanales por 12 semanas.
- Adriamicina 60 mg D1 y ciclofosfamida 600 mg D1 cada 21 días por 4 ciclos, seguidos de docetaxel a 100 mg cada 21 días por 4 ciclos.
- Dosis densas: adriamicina 60 mg D1 y ciclofosfamida 600 mg D1 cada 15 días (uso de FEC), seguidos de paclitaxel 80 mg semanales por 12 semanas (considerar en pacientes jóvenes con RH negativos y ganglios positivos).
- Docetaxel 75 mg D1 y ciclofosfamida 600 mg D1 cada 21 días por 6 ciclos; considerar en pacientes con RH positivos y 1 a 3 ganglios.
- Adriamicina 60 mg D1 y ciclofosfamida 600 mg D1 cada 21 días por 4 ciclos, seguidos de paclitaxel 80 mg D1 D8 y D15 y carboplatino AUC 5 D1 cada 21 días por 4 ciclos
Esquemas de quimioterapia
HER2 positivo
- Adriamicina 60 mg D1 y ciclofosfamida 600 mg D1 cada 21 días por 4 ciclos, seguidos de paclitaxel 80 mg semanales por 12 semanas + trastuzumab, primera dosis de impregnación a 8 mg/kg seguido de 6 mg/kg cada 21 días hasta completar un año.
- Adriamicina 60 mg D1 y ciclofosfamida 600 mg D1 cada 21 días por 4 ciclos, seguidos de paclitaxel 80 mg semanales por 12 semanas + trastuzumab primera dosis de impregnación a 8 mg/kg seguido de 6 mg/kg cada 21 días, hasta completar un año + pertuzumab primera dosis de impregnación a 840 mg seguido de 420 mg cada 21 días hasta completar un año (considerar en adyuvancia en pacientes con más de 4 ganglios positivos)
- Paclitaxel a 80 mg semanales por 12 semanas + trastuzumab primera dosis de impregnación a 8 mg/kg seguido de 6 mg/kg cada 21 días, hasta completar un año (considerar en adyuvancia de pacientes con tumores menores de 3 cm y pN0, pN1mi)
- Docetaxel 75 mg D1 + carboplatino AUC de 6 D1 cada 21 días por 6 ciclos + trastuzumab primera dosis de impregnación a 8 mg/kg, seguido de 6 mg/kg cada 21 días hasta completar un año + pertuzumab primera dosis de impregnación a 840 mg seguido de 420 mg cada 21 días, hasta completar un año
- TDM1 3.6 mg iv D1 cada 3 semanas por 14 ciclos.
*En pacientes que reciben tratamiento con antraciclinas, valorar FEVI por ecocardiograma al inicio y al término y seis meses después del término. En pacientes que reciben tratamiento con trastuzumab, valorar FEVI por ecocardiograma al inicio y cada tres meses durante el tratamiento. En caso de FEVI <50% o disminución del 10%, tratamiento conjunto con cardiología.
Criterios para solicitar estudio de BRCA
Pacientes con cáncer de mama antes de los 50 años y que cumplen los siguientes criterios:
- Cáncer de mama triple negativo
- Dos primarios de mama
Paciente con cáncer de mama a cualquier edad y que cumplen los siguientes criterios:
- 1 o más familiares consanguíneos con:
- Cáncer de mama antes, desde los 50 años
- Cáncer de ovario
- Cáncer de mama en paciente masculino
- Cáncer de páncreas
- Cáncer de próstata de alto grado (Gleason mayor a 7) o metastásico
- Dos o más familiares consanguíneos con cáncer de mama a cualquier edad

Se presenta cada caso con todos los estudios solicitados en la valoración de PRECONSULTA
| ** | Ver consideraciones de cirugía para mama y flujograma de axila |
| ++ | Considerar evaluación por cáncer hereditario en: mujeres <50 años, antecedentes familiares de cáncer de mama y mutaciones, hombre |
| --- | Evaluación por programa de mujeres jóvenes para preservación de fertilidad en mujeres <40 años |


De acuerdo con el consenso de ASTRO 2018, las pacientes candidatas a radioterapia con esquemas hipofraccionados son aquéllas con cualquier etapa clínica, siempre que se planee ofrecer radioterapia a la glándula mamaria, sin incluir las regiones ganglionares, que hayan o no recibido quimioterapia; evitar que la dosis al CTV de mama sea > 105%.
Las pacientes que cumplan los criterios del consenso de la American Society for Radiation Oncology (ASTRO) 2017 y sean catalogadas como “candidata ideal” o “candidata con precaución” podrán recibir irradiación parcial acelerada de mama (IPAM) posterior a la cirugía conservadora
| 1. | Knaul F, Carrillo LL. Cáncer de mama: un reto para la sociedad y los sistemas de salud. Salud pública [Internet]. 2009;51. Available from URL: http:// www.scielo.org.mx/scielo.php?pid=S0036-36342009000800002&;script=sci_arttext&;tlng=pt |
| 2. | Reynoso-Noverón N, Villarreal-Garza C, Soto-Perez-de-Celis E, Arce-Salinas C, Matus-Santos J, Ramírez-Ugalde MT, et al. Clinical and epidemiological profile of breast cancer in Mexico: Results of the Seguro Popular. J Glob Oncol [Internet]. 2017;JGO.2016.007377. Available from URL: http://ascopubs.org/doi/10.1200/ JGO.2016.007377 |
| 3. | Cárdenas Sánchez J, Bargalló Rocha E, Erazo Valle-Solís A, Maafs Molina E, Poitevin Chacón A. Consenso Mexicano sobre diagnóstico y tratamiento del cáncer mamario. Gac Mex Oncol. 2013;12(Suppl 3):4-55. |
| 4. | Savci-Heijink CD, Halfwerk H, Hooijer GKJ, Horlings HM, Wesseling J, van de Vijver MJ. Retrospective analysis of metastatic behaviour of breast cancer subtypes. Breast Cancer Res Treat. 2015;150(3):547–57. |
| 5. | Cárdenas Sánchez J, Bargalló Rocha JE, Bautista Piña V, Cervantes Sánchez G, Erazo Valle-Solís AA, Flores Balcázar CH, et al. Consenso Mexicano sobre diagnóstico y tratamiento del cáncer mamario. Séptima revisión, Colima; 2017: 1-141. |
All Rights Reserved® 2019
Latin American Journal of Clinical Sciences and Medical Technology,Publicación contínua • Editor responsable: Gilberto Castañeda Hernández. • Reserva de Derechos al Uso Exclusivo: 04-2019-062013242000-203; ISSN: 2683-2291; ambos otorgados por el Instituto Nacional del Derecho de Autor. • Responsable de la última actualización de este número, Web Master Hunahpú Velázquez Martínez,
Calle Profesor Miguel Serrano #8, Col. Del Valle, Alcaldía Benito Juárez, CP 03100, Ciudad de México, México. Número telefónico: 55 5405 1396 • Fecha de última modificación, 28 de agosto de 2024.
All Rights Reserved® 2019
Publicación contínua • Editor responsable: Gilberto Castañeda Hernández. • Reserva de Derechos al Uso Exclusivo: 04-2019-062013242000-203; ISSN: 2683-2291; ambos otorgados por el Instituto Nacional del Derecho de Autor. • Responsable de la última actualización de este número, Web Master Hunahpú Velázquez Martínez,
Calle Profesor Miguel Serrano #8, Col. Del Valle, Alcaldía Benito Juárez, CP 03100, Ciudad de México, México. Número telefónico: 55 5405 1396 • Fecha de última modificación, 28 de agosto de 2024.